
療效可能很有限
作者:西北哽
1984年,國營保定化纖廠衛生所的夏醫生在【實用眼科雜誌】上發表了一篇正式的學術論文。
夏醫生雖然只是一個廠辦衛生所的醫生,但在1983年到1990年期間發表了12篇眼科學專業論文,恐怕能讓今天的不少大主任汗顏。夏醫生的文獻中被查閱最多的就是1984年這篇:
【間斷套用微量阿托品點眼法對調節性近視的影響】
眼科醫生之間一直流傳著一種說法:阿托品滴眼能夠緩解近視。上百年來不斷有醫生嘗試,希望驗證這種治療方法。知網上中國最早關於阿托品治療近視的論文發表於1965年。
夏醫生從1981年開始陸續給100個近視眼的小朋友嘗試用0.05%的阿托品,每周滴一次,結果發現治療2個月後有80%以上的小朋友視力恢復1行以上。於是她大膽設想:此法「適用於廣大農村及城市學校或家庭中治療調節性近視」。
(【實用眼科雜誌】論文截圖)
沒想到論文發表40年後,今年3月11日,國家藥監局真的把低濃度阿托品滴眼液批準了延緩近視進展的適應癥。
近百年的設想終於在興齊眼藥手裏變成了現實,這種魔幻的感覺,
▌就好像世界上真的有龍珠一樣。
1
阿托品最早提取自曼陀羅,是一種麻醉劑,100多年前開始人工合成。阿托品常用於驗光前的散瞳,孩子患上假性近視了需要散瞳才能達到準確的驗光效果,大人驗光是不用阿托品的。
一個上市100多年的老藥,既然歷史上早就發現有望緩解近視眼,為何國內外那麽多企業從來沒想過去開發相關適應癥,而是等到了2024年?
這個問題基本無解。只能說老外太傻,讓這潑天富貴落到了興齊眼藥手裏。
按照一些機構的測算方法:中國目前有9000萬青少年近視,假使10%的孩子用上興齊眼藥的阿托品,每年費用按最少2400元計算,至少有200億以上的銷售額;如果一半孩子用,那就是上千億。

在中國吹神藥,百億已經不夠數了,起步至少是千億。2018年PD-1還沒上市時候,就曾以萬能抗癌藥的身份配享過千億市場,如今剩下百億不到;「減肥神藥」司美格魯肽去年突然被廣泛關註,也號稱能賣千億,如今適應癥還沒批下來,競品倒是湊齊了一個排。
阿托品滴眼液論天資其實遠不如PD-1和GLP-1,因為它連創新藥都不是。興齊眼藥申報的時候,報的是新藥2.4類,指的是「含有已知活性成分的新適應癥藥品」,也就是申請新增適應癥。
但2.4類新藥有個很大的問題,必須是境內外都從未申報過的適應癥才算。偏偏好巧不巧,興齊在申報上市過程中,2021年5月中國台灣省五福化學制藥有限公司的0.05%阿托品滴眼液搶先上市,成為全球第一款宣稱能延緩近視發展的藥。
這樣一來,興齊眼藥的藥就不是「境內外都未申報過的適應癥」了,只能降級,變成3類新藥,即「已在境外上市、未在境內上市的原研藥品」的仿制藥。
▌
其實這就是個仿制藥。
2
從2.4類降到3類看似問題不大,但可能是興齊眼藥夢想和現實的分界線:
2.4類好歹算新藥,可能會有6年的專利保護;3類是仿制藥,幾乎沒有專利保護期。
興齊眼藥一直對外表達:根據【藥品試驗數據保護實施辦法(暫行)】(征求意見稿)、【藥品管理法實施條例(修訂草案征求意見稿)】等檔,臨床數據、市場獨占等都構成對產品的保護。但公司自己都不得不承認:
▌
這些檔都是征求意見稿
現行法律法規並沒有禁止其他企業開發3類仿制藥。興齊眼藥隨時會面臨強大對手的拍馬趕到。誰還不會做個3類藥呢?
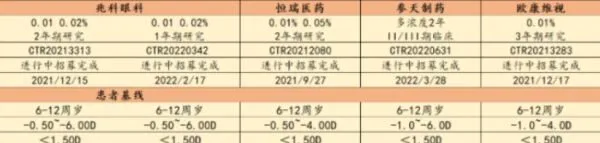
目前,恒瑞醫藥、日本眼藥水巨頭參天制藥、做OK鏡的歐康維視、以及港股上市的兆科眼科,都緊緊追在興齊眼藥後面。
這裏必須提一下長春高新的故事。當時長春高新認為自家水針生長激素獨步天下,孩子中總會有10%的小朋友比同齡人矮,是剛需。把長春高新拉下馬的,其實並不是集采,而是安科生物2019年獲批上市的水針。
氣球只要戳破一個孔,這氣球就不存在了。興齊眼藥現在最怕的應該就是這個。
而且,興齊眼藥為了趕審批進度,在臨床試驗設計上其實是有硬傷的。興齊的阿托品滴眼液目前獲批的適應癥是依據12個月的治療周期來申報的,對應的評價標準是延緩視力進展50度。

換句話說,興齊眼藥的阿托品滴眼液的療效可能很有限。
其他幾家的在研品種幾乎都是按照使用24個月、延緩進展100度為標準在做臨床,至今沒有披露結果,兆科眼科甚至在美國的臨床都失敗了。
這就回到最初探討的那個問題:阿托品滴眼液要是真的非常有效果,為何近100年來一直只是眼科醫生圈子裏的一個傳說?
必須要贊一個!!











