编者按
肝细胞癌(HCC)是最常见的原发性肝癌类型,多数患者在确诊时无法进行手术切除,系统性治疗成为这部分人群的重要治疗手段。免疫联合疗法阿替利珠单抗+贝伐珠单抗(「T+A」)因显著优于索拉非尼的总生存期(OS),成为不可切除HCC患者的新一线标准治疗。然而其在不同人群,包括不同病因HCC、Child-Pugh B级HCC和超up-to-seven标准的中期HCC患者中的疗效尚不清晰。【国际肝病】特综述近期发表的相关研究,供广大读者学习参考。
「T+A」疗法对不同病因HCC均有效
既往研究认为,HCC的生物学特性可能受到诸如病毒感染、酒精相关损伤和代谢等不同肝病病因影响,不同病因会影响免疫检查点抑制剂(ICIs)在HCC中的效果,特别是非酒精性脂肪性肝病(NAFLD)被认为存在ICI抵抗性。
最近发表的一项IMbrave150后期分析研究[1]中,在接受「T+A」治疗的意向治疗人群中选取了可获得临床数据的279名患者,依据HCC不同病因,分为NAFLD(n=47)、丙肝(HCV,n=70)、乙肝(HBV,n=108)和酒精性肝病(ALD,n=51)四组,比较「T+A」疗法在各组中是否存在疗效差异。
研究结果显示:基于RECIST 1.1标准,NAFLD、HCV、HBV和ALD四组的客观缓解率(ORR)分别为33.3%、28.8%、34.0%和23.5%,各组间无显著差异( P =0.64); 四组的中位无进展生存期(PFS)分别为9.5、8.4、6.7和7.0个月,各组间均无显著差异( P =0.97);四组的中位总生存期(OS)分别为19.2、24.6、19.1和16.9个月,同样各组间均无显著差异( P =0.41) ,详见图1。
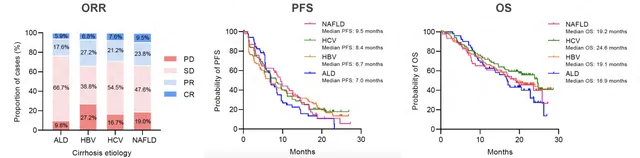
图1. 不同病因组ORR、PFS和OS[1]
进一步的多因素Cox回归分析和敏感性分析同样证实,PFS和OS在NAFLD组和其他病因组间无统计学差异。在NAFLD队列中,存在非酒精性肝损伤的38名患者的ORR、PFS和OS结果在多重比较中也没有统计学意义的差异。当采用mRECIST或imRECIST标准时,不同病因组间的PFS和ORR差异仍无统计学意义。此外,采用肿瘤细胞阳性比例分数(TPS)或联合阳性分数(CPS)评估PD-L1表达水平,不同病因组间的差异也没有统计学意义。
因此,这项研究表明,「T+A」疗法对不同病因HCC均有效,尤其值得注意的是NAFLD和非酒精性脂肪性肝炎(NASH)患者与其他病因HCC患者的疗效无显著差异。
「T+A」疗法对Child-Pugh B级晚期HCC具有一定疗效
既往观察性研究中,未治疗的Child-Pugh B 级HCC患者的中位OS仅2~5个月。Child-Pugh B级HCC患者的系统治疗选择有限,这类患者由于肝功能受损,常被前瞻性临床试验排除在外。索拉非尼是以往研究中Child-Pugh B 级HCC患者最为常用的药物,但治疗后OS也仅有 2.5~5.2个月。
最近发表的一项多中心、回顾性研究[2]探索了「T+A」疗法对Child-Pugh B级晚期HCC患者的疗效。研究纳入36名Child-Pugh B级不可切除HCC患者,并与另一组Child-Pugh A级HCC患者的独立队列(n=133)进行了比较分析。
Child-Pugh B组的基线数据如下:中位年龄为61岁,83.3%为男性,HBV感染是最常见病因(n=21,58.3%)。Child-Pugh评分为B7、B8和B9的患者比例分别为66.7%(n=24)、25.0%(n=9)和8.3%(n=3)。共有25名(69.4%)患者有肝外转移,最常见的转移部位是肺(n=15,41.7%),其次为淋巴结(n=10,27.8%)和骨(n=4,11.1%)。21名(58.3%)患者伴有大血管侵犯,基线血清甲胎蛋白(AFP)水平在21名(58.3%)患者中超过400 ng/ml。
疗效比较结果显示,Child-Pugh B级患者中,4例(11.1%)达到部分缓解(PR),17例(47.2%)达到病情稳定(SD), ORR和疾病控制率(DCR)分别为11.1%和58.3% 。中位随访时间为5.2个月(95%CI:1.9~8.4),Child-Pugh B级患者的中位PFS和OS分别为3.0个月(95%CI:1.7~4.3)和7.7个月(95%CI:4.8~10.6);Child-Pugh A级组患者的 ORR和DCR分别为34.1%和76.7%,中位PFS和OS分别为9.6个月和尚未达到(图2)。
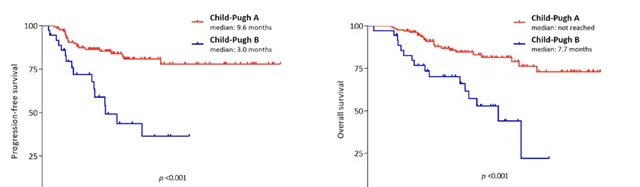
图2. Child-Pugh A级和B级患者的PFS和OS[2]
因此,这项研究表明「T+A」疗法对Child-Pugh B级晚期HCC患者也具有一定的疗效,有必要开展进一步的前瞻性研究以明确获益亚组。
TACE联合「T+A」在超up-to-seven标准的中期HCC患者中显示出初步疗效
中期HCC患者( BCLC B期)占所有HCC病例的20%~30% ,这部分患者的预后欠佳,尤其是超up-to-seven 标准的中期 HCC患者,治疗仍存在挑战。IMbrave 150研究中,接受 「T+A」治疗的中期HCC患者ORR为44%,但超up-to-seven 标准的中期HCC患者的6周ORR仅为17.7%。
经动脉化疗栓塞治疗(TACE)局部治疗联合免疫治疗能引发协同抗癌效果。我国一项多中心、单臂、回顾性研究探索了TACE联合「T+A」治疗在超up-to-seven标准的中期HCC患者中的有效性和安全性[3]。
该研究纳入了21例接受TACE联合「T+A」作为一线治疗的中期HCC患者,中位年龄为56岁,19名患者是男性,20例(95.2%)患者肝功能为Child-Pugh A级,19例(90.5%)患者mALBI分级为1/2a。中位随访时间为11.7个月(范围:7.5~15.0个月)。
据RECIST 1.1标准,ORR为42.9%,DCR为100%;据mRECIST标准, ORR为61.9%,DCR为100% (表1)。PFS与OS暂未达到, 1年PFS率为76.2%,1年OS率为90.5% (图3)。持久反应率(DRR)≥3个月者占比57.1%,DRR≥6个月者占比47.6%。联合治疗最常见的治疗相关不良事件(TRAE)为发热(71.4%),最常见的3/4级TRAE为高血压(14.3%)。
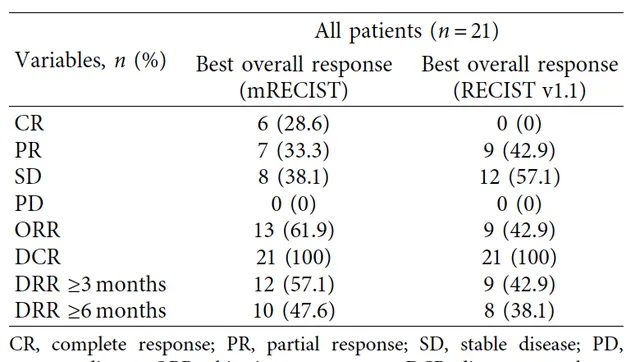
表1. TACE联合「T+A」在超up-to-seven标准的中期HCC患者中的疗效[3]
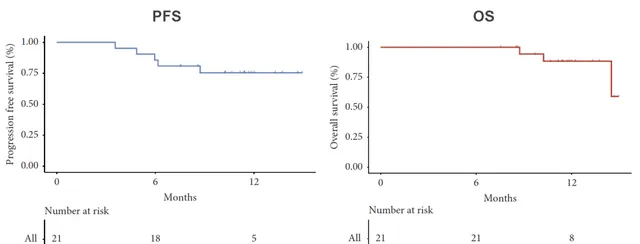
图3. 超up-to-seven标准的中期HCC患者的治疗 后PFS和OS[3]
总结
基于IMbrave 150研究的突破性进展,「T+A」免疫联合疗法已成为晚期不可切除HCC的一线标准治疗,其在真实世界不同人群中的临床数据越来越丰富。以上三项研究分别证实了「T+A」治疗在不同病因HCC中的疗效,初探了「T+A」疗法在Child-Pugh B级HCC患者中的应用,以及为「T+A」联合TACE用于超up-to-seven标准中期HCC患者提供了依据,揭示了「T+A」疗法在HCC治疗中的具有巨大潜力。未来,期待有更多的研究发现,为HCC患者带来更好的生存获益。
参考文献:
[1] Espinoza M, Muquith M, Lim M, Zhu H, Singal AG, Hsiehchen D. Disease Etiology and Outcomes After Atezolizumab Plus Bevacizumab in Hepatocellular Carcinoma: Post-Hoc Analysis of IMbrave150. Gastroenterology. 2023 Jul;165(1):286-288.e4. doi: 10.1053/j.gastro.2023.02.042.
[2] Cheon J, Kim H, Kim HS, Kim CG, Kim I, Kang B, Kim C, Jung S, Ha Y, Chon HJ. Atezolizumab plus bevacizumab in patients with child-Pugh B advanced hepatocellular carcinoma. Ther Adv Med Oncol. 2023 Jan 12;15:17588359221148541.
[3] Wang K, Zhu H, Yu H, Cheng Y, Xiang Y, Cheng Z, Li Y, Li T, Wang D, Zhu Z, Cheng S. Early Experience of TACE Combined with Atezolizumab plus Bevacizumab for Patients with Intermediate-Stage Hepatocellular Carcinoma beyond Up-to-Seven Criteria: A Multicenter, Single-Arm Study. J Oncol. 2023 Apr 15;2023:6353047.











