β受体阻滞剂在危重患者中的作用:SIAARTI专家共识声明
重症行者翻译组
摘要
背景 β受体阻滞剂在危重症中的作用已备受研究,近二十年来,文献中多次报道了β受体阻滞剂对危重症患者的保护作用。然而,危重患者使用β受体阻滞剂仍然缺乏共识和指南。本文的目的是支持临床中使用β受体阻滞剂危重患者决策过程。此文受用者包括医生、护士、医疗保健人员和参与患者护理过程的其他专业人员。
方法 意大利麻醉、镇痛、复苏和重症监护协会(SIAARTI)挑选了一组专家,要求他们明确使用β受体阻滞剂的关键要素。在此过程中,专家所采用的方法符合改进的德尔菲法和RANDUCLA法的原则。专家们以翔实的文本形式提出了陈述和支持性的理论。所有发言都经过盲投以达成协商一致意见。
结果 文献检索提示,危重患者肾上腺素能应激和心率升高与器官功能障碍和死亡率增高有关。因此,心率控制在危重病人的管理中至关重要,需要仔细的临床评估,目的是为了做好继发性心动过速的鉴别诊断和心律紊乱的治疗。此外,一旦排除了低血容量,可考虑使用β受体阻滞剂治疗持续性心动过速。静脉应用应是给药的首选途径。
结论 β受体阻滞剂对危重症患者的保护作用已经多次报道。在快速心率的急性治疗中需要了解病理生理学和相关鉴别诊断,因为所有导致心动过速的原因都应该首先排除和处理。
一、背景
重症监护病房(ICU)的危重患者可继发于原发急性疾病(如休克、创伤、感染)的不同程度交感神经溢出的影响,且常伴有心血管系统合并症。β受体阻滞剂在危重症患者中的作用备受研究,近二十年来,文献中多次报道了这些药物对危重症患者的保护作用。
β受体阻滞剂通过几种亚型的g蛋白偶联β肾上腺素能受体发挥作用,在机体细胞膜表面几乎均有表达。一般来说,β受体阻滞剂通过预防和/或调节β肾上腺素能反应来干扰儿茶酚胺和交感神经类药物作用(表1)。临床效果取决于β-受体阻滞剂所结合的受体亚型及其位置(表1)。
根据它们的药效学,β受体阻滞剂目前被用于治疗全身性动脉高压、快速心律失常和心力衰竭。此外,β受体阻滞剂通过降低后负荷来降低血压,同时降低了心肌耗氧量,改善心肌灌注和每搏输出量(SV)。β受体阻滞剂还可有效控制交感神经激活的,并且对处理心律失常的有效性,也意味着病理生理机制明确,管理此类急性心律失常可使用此治疗。
专家团体对于危重症中使用β受体阻滞剂仍缺乏共识和指南,而且脓毒症患者的管理指南从未建议在这种情况下使用β受体阻滞剂。为了弥补这一领域空缺,意大利麻醉、镇痛和重症监护协会(SIAARTI)挑选的一组重症监护专家撰写了这份关于在危重病人中使用β受体阻滞剂的良好临床实践文件。
二、方法
专家小组成员是由两个项目协调员代表SIAARTI根据证据、临床和科学经验选出的。在确定方法的初步会议后,根据一位或多位小组成员各自专长,将不同的主题分配给他们,如下:
•评估现有证据
•以解释性文本的形式提供陈述和论据
全部发言清单已按照表决方法提交表决,以表示协商一致的程度。
该文件的方法学路径由方法学家(a.c.)概述,并基于科学文献的审计原则和改进的德尔菲法[。更详细的是,文献综述是由两位主题专家在PubMed上进行的,没有明确的时间限制,使用网格词检索。
专家小组定义了四个临床问题(CQ),并在线上范围界定研讨会上提出和投票。在定义问题之后,两位主题专家定义了一个专门的文献搜索策略,然后,从搜索生成的列表中选择相关文献,并将所选的每篇论文与四个临床问题中的一个或多个相关。被选中的论文列表随后提交给小组评审。
检索的论文类型为:随机对照试验、系统综述、meta分析、指南、非随机对照试验、叙述综述、立场论文、实验研究。使用不同于英语的语言的论文被排除在外,病例报告、病例系列和会议记录也是如此。根据PRISMA 2020的原则进行了搜索,并生成了最终报告。小组成员运用主题专家的报告及其能力,起草了一份声明和理由清单,然后进行无记名投票。整个小组(不包括搜索专家和方法专家)都参加了盲投。该方法要求最多进行两轮在线投票。
根据RAND-UCLA方法,使用顺序李克特量表(ordinal Likert scale)表达意见(最低分,1 =完全不同意;最高分,9 =完全同意),该量表分为3个部分:1-3分表示拒绝/不同意(「不适当」),4-6分表示(「不确定」),7-9分表示同意/支持(「适当」)达成的协商一致意见如下:
1) 至少75%的受访者(不包括方法学家和搜索专家)给出了1-3、4-6或7-9分,分别表示拒绝、不确定和同意陈述
2) 中值在相同范围内。共识的类型是由中位数的位置决定的。因为所有的声明在第一轮就达成了共识,所以没有必要进行第二轮德尔菲赛投票。投票结果以表格形式公布。由意大利麻醉、镇痛、复苏和重症监护协会(SIAARTI)发布的意大利语文件全文于2023年4月发布,可在该协会的意大利语网站上免费获得(https:// www. siaar ti. it/ news/ 1527682)
三、问题一:纠正危重病人心动过速的基本原理是什么?
对重症患者而言,疾病急性状态增加心脏及组织氧消耗(VO2),引起肾上腺素的高度激活,肾上腺素能高度激活(Adrenergic hypertonicity)是患者常见且复杂神经内分泌反应之一,会引起氧释放和氧消耗失去最佳比例。即使引发迅速代偿的神经内分泌反应的原因得到了纠正(如贫血、低血容量、疼痛和体温过高),后续也会出现继发于血管收缩的低灌注和不可避免的与心动过速或心力衰竭相关的心肌氧消耗增加。
这种情况通常伴有心率增加,可表现为窦性心动过速或导致可能与血流动力学不稳定相关的心动过速(低血压和/或灌注不足)。
这种过度的肾上腺素能应激和心率增加与器官功能障碍和死亡率增加有关。
在这种病理生理情况下,心率控制在危重病人的管理中扮演着重要的角色,需要仔细的临床评估,评估要针对继发性心动过速进行鉴别诊断,也要针对心律节律异常的治疗。
生理上,主要的补偿机制涉及交感神经过度刺激(endogenous catecholamines with
sympathetic hyperstimulation)时内源性儿茶酚胺的释放。对于血流动力学不稳定的治疗,外源性儿茶酚胺(exogenous catecholamines)的使用也是必要的。然而,在这两种情况下,过度的肾上腺素能刺激都与器官损伤有关,导致预后恶化和死亡率增加。
心动过速的诊断框架需要对心电图示踪(electrocardiographic tracing)进行分析,并将其适当地整合到超声心动图(echocardiographic examination)检查中。心动过速定义为心率(HR)大于100 次/分。
-窦房结水平定窦性心动过速;
-心室水平,定室性心动过速,通常持续时间短,伴有重要的血流动力学改变;
-心室以上起源,通常表现为心房电活动的改变,归因于折返机制或心房肌细胞自律性的增加
心室以上起源,表现如下:
-心房扑动,规则锯齿波,180- 250次/分;
-快速型心律失常伴心房纤颤,P波被房颤波替代,伴异常QRS波
-室性心动过速,RR间期不规则,QRS波间隔及形态异常,与P波无关联
超声心动图用于诊断心动过速的起源和指导β -受体阻滞剂应用,检查时应同时关注收缩期和舒张期功能,以及容量状态。
心室-动脉耦合的计算是一项更复杂的评估,可以添加到超声心动图评估中,以了解心血管系统的效率,并在治疗后重新评估患者的生理状况。
四、问题二:在危重患者中使用β受体阻滞剂纠正心动过速的基本原理是什么?对于危重患者,应使用β阻断药物来控制心动过速
最近对包括2103名危重患者在内11项研究的荟萃分析显示,与对照组相比,使用β受体阻滞剂组,死亡率显著降低(风险比0.65,95% CI 0.53-0.79;P < 0.0001),然而,这一系统回顾和荟萃分析包括了一系列不同的研究,大多数集中在心肌缺血或接受心脏手术的患者。因此,很难就死亡率差异得出明确结论。
另一项近期的回顾性研究对204,981名接受腹部大手术的患者进行了倾向评分分析(propensity score analysis),发现在慢性治疗中接受β受体阻滞剂的患者(优势比,0.86;95% CI: 0.65-1.15;P = 0.901)和术前60天内开始用药的患者(优势比,0.90;95% CI, 0.31-2.04;P = 0.757)术后卒中发生率没有差异。
β受体阻滞剂在急性期只有在出现「心动过速」时才有保护作用,当脱离患者心动过速病情,则不会明显体现「保护效应」,为了给使用这些药物的危重患者提供可信推荐,我们需要进一步的随机对照试验来回答关于患者选择、药物选择、时机和最佳血流动力学目标的问题。
对于脓毒性休克患者,可以考虑使用β受体阻滞剂治疗持续性心动过速
继发性(每搏输出量降低)与非继发性(神经内分泌系统过度激活或心律失常)心动过速的区别,是明确哪些患者能够从β受体阻滞剂受益的主要因素。
脓毒性休克患者第一阶段,不受控制的炎症反应导致血管舒张和毛细血管通透性增加,同时心输出量(CO)减少,这与绝对和相对低血容量有关。交感神经系统过度引起激活心率(HR)增加,尽管此时前负荷低,可仍代偿性维持机体心输出量CO;然而,对于那些长期服用β受体阻滞剂的患者,其疗效可能会减弱。不论先前是否使用长期β受体阻滞剂,持续性心动过速,与高剂量内源性和外源性儿茶酚胺有关,会导致更糟糕临床结局。在脓毒症患者群体,识别具有类似血流动力学反应的患者亚群,这个目标关系到较差的预后。
β受体阻滞剂可降低心率,控制心动过速,使心肌收缩力与心率相协调,降低心肌耗氧量。
在一项随机单中心临床试验中,液体复苏后仍保持心动过速的患者中,持续注入β受体阻滞剂可改善心血管功能(心率、每搏输出量SV、全身血管阻力SVR和乳酸),没有明显不良反应即可降低血管升压药物的负荷。
此外,与其他药物(如胺碘酮amiodarone、硫酸镁magnesium sulfate、地高辛digoxin)相比,脓毒症合并心房颤动患者使用β受体阻滞剂能提供更快速的控制心率(1小时vs 6小时)。
尽管血管缺乏β1受体,输注选择性β受体阻滞剂可缓解脓毒症诱导的血管加压治疗低反应性。β受体阻滞剂可以改善血管反应性与α1受体下调相关。基于此原理,一项研究发现,使用短效β受体阻滞剂艾司洛尔治疗脓毒性休克患者,其动脉弹性有所改善,尽管心输出量(CO)降低,这或许可以解释「选择性β受体阻滞剂与血管加压药需求的降低相关」的缘由。
在最近的一项荟萃分析中,持续输注超短效β受体阻滞剂—使用低初始剂量和逐渐加量——已证明可以改善脓毒症和脓毒症休克患者的生存(降低28天死亡率,风险比0.68;95% CI,0.54-0.85),容积复苏后24 h心率持续大于95次/分,显著高于对照组(P < 0.001)。有趣的是,作者也报道了使用β受体阻滞剂后白细胞计数较低,这一发现引发了假设,即β受体阻滞剂对脓毒症患者产生免疫调节作用。
在一项分析1839篇论文的荟萃分析中纳入了14项研究(5项随机对照试验,9项非随机研究)。所有纳入的研究都显示,在1小时内,β受体阻滞剂改善HR控制,然而在6小时HR控制与其他药物相比没有显著差异,有趣的是,胺碘酮达到HR控制的时间最长。
在一项系统综述中,包括6项评估死亡率的研究,其中4项表明使用β受体阻滞剂有实质性的好处。然而,由于缺乏针对这一主题的大规模随机对照试验,需要更多的研究来确保这些研究发现的有效性及普遍化。
在一项随机对照试验中,一组脓毒性休克患者(77例)接受持续输注艾司洛尔以维持心率在80/分至94/ 分之间,而对照组(77例)接受超过96小时的标准治疗,与对照组相比,艾司洛尔组的所有患者均达到了目标心率,与对照组的-6/分(95%CI,- 14至0)相比,艾斯洛尔组前96小时心率曲线下面积(AUC)的中位数降低28次/分(四分位数间距,- 37至- 21次/分),平均减少18次/分(P < 0.001)。
高危手术患者的心率和围手术期耗氧量的控制应该通过使用β受体阻滞剂药物来实现
在这种情况下,β受体阻滞剂在围手术期的治疗中所起的作用,在近20年的时间里,围绕其引入治疗的代价/效益一直存在争议,最近在欧洲心脏病学会(ESC)指南中再次讨论了这一问题。
虽然单纯从电生理角度来看,围手术期心动过速的控制有几种治疗方案,但钙通道阻滞剂的选择并没有近期文献的支持,而胺碘酮是围手术期心房颤动相关心动过速领域中最常用的药物。
非心脏手术中,围手术期维持(口服)慢性β受体阻滞剂治疗是良好护理质量的一个标志。他们在手术后60天内开始摄入,在限制围手术期并发症方面有效,但与慢性β受体阻滞剂治疗相比,在术后卒中发生率方面没有差异。
五、问题三:在ICU患者中,处理心动过速的诊断-治疗策略是什么?在ICU的病人,有必要诊断继发性心动过速,以便能够用特定的药物治疗
心动过速是一种非常常见的临床症状,但同时也被临床医生所低估。常引起严重的血流动力学不稳定和器官灌注减少。
最危险的患者群体是败血症患者、多发性创伤患者、烧伤患者和接受心脏手术或大手术的患者。这些患者群体最容易发生血流动力学、免疫、代谢、呼吸和神经功能异常以及凝血功能变化,这些系统的失调与死亡率的增加有关。
治疗心动过速的方法应以降低心率和控制心律为基础
在治疗心动过速患者的策略中,第一步是找到原发病因进行纠原治疗并进行治疗(贫血、低血容量、肌张力障碍、应激、低氧血症、疼痛、药理学肾上腺素能过度刺激等)。
纠因治疗后,心动过速仍旧持续,考虑患者存在病理状况,应采取药物治疗管理。
在重症监护病房,心率增快,特别是与血流动力学不稳定有关时,代表需要药物控制。危重患者不仅血流动力学功能发生复杂而突然的变化,而且免疫、代谢和凝血功能也发生复杂而突然的变化,这必然意味着交感神经过度刺激激活内源性儿茶酚胺系统(endogenous catecholamine system),与器官损伤有关,并导致预后恶化和死亡率增加。心动过速诱导心肌缺血,心肌能量储备利用率显著增加,细胞及细胞外基质重构,可能是心肌功能进行性恶化,从而引起血流动力学不稳定,导致器官灌注减少的病理生理机制。
在危重患者中,β受体阻滞剂的使用应静脉滴注,最好与快速动力学药物同时使用;当肠内给药似乎可行时,应进行向其他给药途径的过渡
目前还没有专门针对重症监护患者使用β受体阻滞剂策略的研究。然而,工作组一致认为,考虑到重症患者存在血流动力学和器官功能不稳定,那么持续经静脉给予半衰期短的β受体阻滞剂滴入可以控制使用后药理效果,避免药物积聚作用。
此外,危重患者应用高度心脏选择性的β受体阻滞剂,应最小化「用后低压风险」和「器官功能的影响」(例如呼吸、内分泌)。
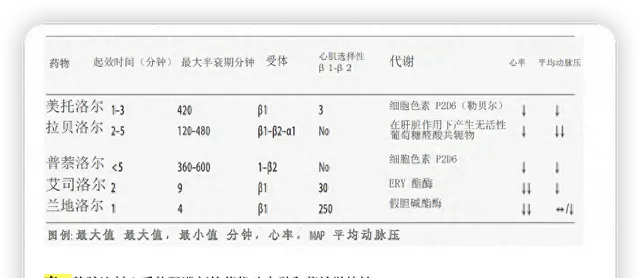
艾司洛尔和兰地洛尔通过抑制房室传导,降低心肌耗氧需求来降低心率,他们的药代动力学允许医生「滴定」用药剂量以快速调整β受体阻滞剂不同稳定水平。
短效作用与血浆酯酶的快速酶解有关,因此,它们的使用表明β受体阻滞剂对患者临床有受益,但它们必须谨慎地滴定其效果:机体内环境状态对β受体阻滞剂不敏感发挥了核心作用,这使得这些药物在调节败血症患者的血流动力学方面尚待探讨。艾司洛尔和兰地洛尔具有高度心脏选择性(兰地洛尔大约高8倍,分别为255:1和33:1),与极短的半衰期和机体内环境状态低敏感相关(艾司洛尔发挥效果需要9分钟,比4分钟更久)。
美托洛尔是另一种选择性β1受体阻滞剂,静脉使用,可以缓慢或额外的给药,一旦临床情况稳定,不再有进一步的休克风险,如果需要,可以经肠内途径给药。
脓毒症患者中,适当前负荷存在的情况下,降低心率可以改善动脉弹性,并通过确保全身灌注来改善心肌效率,这是β受体阻滞剂治疗核心。根据这个观点,如果部分患者HR降低与血流动力学恶化相关,收缩压与切迹压(SDP)之间的差异是明确这部分人群的指标。SDP阈值低于35mmHg是心率降低后血流动力学恶化的前兆。
因此,β受体阻滞剂治疗复杂的血流动力学反应需要缓慢和持续的调节,以确保最安全的心血管稳定性。
对血流动力学稳定的慢性β -阻滞剂治疗的患者,β -阻滞剂治疗不应停止
最近的ESC指南已经证实,在接受β受体阻滞剂慢性治疗的手术患者中,不应在围手术期间中断治疗。
这一理论是基于大量的研究,这些研究表明,术前中断慢性β受体阻滞剂治疗的手术患者术后死亡率增加,术后中断β受体阻滞剂治疗2天的患者发生房颤的风险可能增加两倍。
六、问题四:危重患者快速节律性心房颤动的治疗策略是什么?
开始药物治疗之前,所有引起房颤心律的可逆转因素(电解质紊乱、酸碱异常、使用β -激动剂药物、心肌缺血、低血容量、贫血、感染、疼痛和躁动)必须识别并在必要时进行治疗
只有排除可逆原因和触发心动过速的因素后,才应进行AF的药物治疗。没有研究支持这一理论;不过,工作组基于ESC指南支持这项原则。
房颤指的是一种室上来源的心律紊乱,呈阵发发作,发作后7天内自行终止或介入治疗后7天内自行终止
ESC指南将房颤分为5个亚组:首发型、阵发性、持续性、长期持续性和永久性
为了更完整,在本文档中,将不仅仅参考阵发性房颤,还将参考危重患者诊断的其他类型的房颤,尽可能确定更多的特征。
无论是否采用第一种「血流动力学」方法,复杂的危重患者都可以从多学科团队的参与中受益,该团队包括转诊专家、全科医生(用于出院后的协助)和家庭成员/护理人员
考虑到房颤的复杂性,ESC指南建议多学科治疗,目的在患者从危重区出院后的随访。
无论急性处理,从主要的血液动力学角度来看,房颤患者的管理需要深入的临床评估,包括风险和易感因素,卒中风险,取决于(或不完全取决于)急性治疗结果的抗凝治疗指征,和/或心脏介入程序(比如:左心耳封堵、心房射频消融、心室起搏器植入)。
危重患者心房颤动药物治疗用于血流动力学稳定的患者,心率控制应作为首要目标
心率节律控制策略是指试图恢复和维持窦性节律。控制策略包括治疗方法和抗凝治疗管理,治疗方法有同步电复律、抗心律失常药物的使用、心内科介入手术(如导管消融)的应用、适当控制平均心室率(心率控制vs心律控制)和抗凝治疗的管理
对于血流动力学不稳定的患者,建议进行电复律
对于血流动力学不稳定(如低血压/低灌注/心肌-DO2-VO2不匹配)的患者,应采用直流同步电复心律,因为其比药物复心律更有效,可立即恢复窦性心律。抗心律失常(antiarrhythmic)药物预处理可提高择期电复律的疗效。
伴有心房颤动的危重患者中,正常或中度左心室功能低下的患者应使用β受体阻滞剂和钙通道阻滞剂来实现心率控制,EF < 40%,应使用β受体阻滞剂和地高辛
目前尚无临床研究对重症患者心房颤动的首选治疗药物进行探讨。然而,最近的ESC指南推荐(IB)使用β受体阻滞剂和钙通道阻滞剂作为一线药物,用于房颤和射血分数> 40%的患者进行急性心室率控制。
根据2022ESC指南,在EF < 40%的情况下,应使用β阻断剂和地高辛(IB),并始终考虑到前者的负性肌力效应。
β受体阻滞剂通常是控制病情的一线药物,特别是在急性期,如重症监护病房患者房颤阵发性发作。
药物的选择取决于症状、合并症和潜在的副作用。
两项研究报告,与胺碘酮(amiodarone)相比,使用β受体阻滞剂的死亡率较低;其中一项研究,纳入39,693名脓毒症患者,60%的患者住进了重症监护病房,校正混杂因素后显示相对风险为0.67 (95% CI: 0.59-0.77)。
另一项涉及重症监护病房患者的研究显示,与美托洛尔相比,胺碘酮治疗的患者死亡率(40%)无统计学意义。
在急性情况下,临床医生必须始终考虑房颤的病因或共同原因(触发因素)(例如,贫血,感染)。β受体阻滞剂和钙通道阻滞剂优于地高辛,因为即使在交感神经系统激活的情况下,它们也能发挥更快的作用和更大的功效。药物受体选择性,特别是在左室收缩功能降低的患者,在药物剂型选择中需要考虑,仍需要在危重症患者中专门针对这些方面进一步研究。
比较不同类别药物的研究在研究设计、结果分析或患者、剂量和给药方法的异质性方面存在很大的偏倚风险。
当需要药物治疗时,危重患者的首选药物应是快速作用和机体能够快速清除的β受体阻滞剂
危重患者可能存在肝肾功能不全、既往存在的心功能不全(如慢性收缩期功能不全、舒张期功能不全伴慢性全身性动脉高压)或新发病(脓毒性心肌病,围手术期缺血性心肌损伤),选择快速作用和机体快速消除的β受体阻滞剂成为首选药物。
此外,在危重患者中使用选择性的、快速作用和短期持续的β受体阻滞剂具有易于「滴定」和快速逆转静滴本身(suspension)副作用的优点,在脓毒性休克患者,β受体阻滞剂减少心动过速和血流动力学稳定方面的优势已经有目共睹。
七、结论
文献数据表明,肾上腺素能压力负荷以及心率增快与重症患者器官功能障碍和高死亡率相关,文献中多次报道β受体阻滞剂对危重病人的保护作用。
因为我们要首先排除所有引起心动过速的原因,且排查导致心动过速的因素,所以心率增快的急性治疗应用β受体阻滞剂,需要了解基本病理生理学,也需要进行详细的鉴别诊断。本文章旨在通过提供良好的临床实践,支持医疗人员在危重患者中使用β受体阻滞剂。











