腎性貧血與多種不良預後密切相關,可增加 CKD 患者的心血管事件和全因死亡風險,導致患者整體生活質素的下降 1 。新型口服低氧誘導因子脯氨酰 羥化酶抑制劑( HIF-PHI )的出現使得腎性貧血治療進入到了新的治療階段。
自全球首個HIF-PHI羅沙司他上市以來,對於此類藥物合理使用劑量的探索一直是腎科領域的關註重點:如何在保證糾正貧血療效的同時,避免血紅蛋白水平升速超標,從而減少一些安全性事件的風險?2023 年美國腎臟病學會年會(ASN )期間公布了兩項關於羅沙司他不同起始劑量治療非透析CKD (ND-CKD )及透析依賴性(DD )人群中的有效性和安全性研究,結果顯示標準劑量與低劑量起始給藥在療效和安全性上未發現顯著差異 2,3 。
繼羅沙司他之後,恩那度司他是第二個進入中國的HIF-PHI 類藥物。剛剛結束的 中華醫學會腎臟病學分會2023 年學術年會(CSN 2023 )期間公布了一項由廣東省人民醫院余學清教授牽頭的HIF-PHI 類藥物恩那度司他中國3 期臨床研究,該研究結果提示在中國人群中套用恩那度司他可顯著提升Hb 水平,安全性良好 4 。值得一提的是,該研究中恩那度司他起始劑量為4mg QD ,這一劑量跟之前日本完成的多項3 期臨床研究不同(日本非透析人群采用2mg QD 起始) 5,6 。為什麽中日研究設計有此不同?適合中國腎性貧血患者的藥物劑量方案是什麽?本文將結合多項臨床研究數據進行分析。
兼顧日本多項臨床研究數據及中國腎性貧血指南升速要求,最終選擇4mg作為中國人群起始劑量
2021年【中國腎性貧血診治臨床實踐指南】指出ESAs初始治療時 Hb 增長速度應控制在每月10~20g/ L 1 ,以保證在有效提升Hb的同時盡可能減少由於Hb升速超標而導致的血栓、心血管事件等問題。
恩那度司他日本多項3期臨床研究數據結果顯示,對於ESA未治、ESA轉換及總體患者來說,2mg起始治療療效非劣於達依泊汀α,24周治療結束期Hb水平達到100-120g/L比例為88.6%,長期治療過程(52周)中Hb水平維持在目標範圍(100~120g/L)內 5,6 。但是,日本多項上市前臨床研究結果顯示,恩那度司他2mg起始治療ND-ESA未治人群前4周Hb升幅為3.2-5.2g/L 5-7 ,難以滿足中國腎性貧血患者初治前4周Hb上升10-20g/L的治療需求 1 。此外,日本臨床研究2mg 起始套用恩那度司他,治療期間經過劑量調整,研究結束時,患者平均使用劑量均約為3mg 5 。
綜上,研究者最終決定采取4mg 起始作為中國3 期臨床試驗的劑量最佳化方案 4 。
恩那度司他4mg起始治療在中國非透析腎性貧血患者中的表現如何?
該研究是一項隨機、雙盲、安慰劑對照、多中心臨床試驗,納入中國48 家研究中心,招募隨機前至少8 周未接受過ESA 治療的ND-CKD 貧血患者,按照2 :1 比例隨機分為恩那度司他組和安慰劑組。研究包括≤4 周篩查期、8 周雙盲期、16 周開放治療期和2 周安全隨訪期(圖1 ) 4 。

圖1 恩那度司他中國3期臨床研究設計
恩那度司他組起始劑量為4mg/ 天,固定劑量治療4 周,第5 周開始根據Hb 變化每4 周調整一次劑量,以維持Hb 在100-120g/L 範圍內。研究主要終點為第7-9 周Hb 水平較基線平均變化值,次要終點包括第7-9 周Hb ≥100g/L 的患者比例,Hb 水平及變化情況等。
雙盲治療期間, 第7-9 周恩那度司他組和安慰劑組的Hb 較基線變化分別為15.99 ±9.46g/L 和0.14 ±8.08g/L (均值±SD ),組間差異為16.0 ±1.54g/L (LSM ±SE ),P<0.001 。雙盲治療期內恩那度司他組和安慰劑組平均Hb 水平較基線變化情況如圖2 所示。 第7-9 周恩那度司他組平均Hb 水平≥100g/L 的患者比例高達85.3% ,顯著高於安慰劑組(P<0.001 )。
圖2 雙盲期平均Hb水平較基線變化情況
在Hb 升速方面,恩那度司他治療前4 周平均Hb 較基線增加11.82 ±9.56g/L ,符合2021 年【中國腎性貧血診治臨床實踐指南】要求,滿足中國人群初始治療合理升速的需求 1 。初始分配到恩那度司他組的受試者至25 周治療結束時Hb ≥110g/L 且Hb 較基線增加≥10g/L 受試者的累計比例為85.4% , 滿足長期治療Hb 保持穩定的治療需求 。
此外,研究結果亦顯示, 恩那度司他治療期間療效穩定,調藥次數少 。初始分配到恩那度司他組的受試者中,4mg 起始治療,後續使用劑量逐步減少,最終維持階段平均劑量與日本研究2mg 起始結果相似均約為3mg 。其中雙盲治療期平均日劑量為3.92 ±0.67mg ,開放治療期平均日劑量為2.98 ±1.89mg ,研究最後4 周每日平均劑量為2.92 ±2.15mg 。調藥次數方面,恩那度司他組受試者開放治療期(16 周)調整劑量次數僅為1.5 次。以上結果證實,套用恩那度司他4mg 起始治療,整體研究期間調藥次數少,無需頻繁調整劑量。
安全性方面,恩那度司他組和安慰劑組在雙盲治療期間AE 發生率分別77.7% (80/103 )和 79.2% (42/53 ),不良反應 發生率分別為18.4% (19/103 )和15.1% (8/53 ),以上數據 提示 恩那度司他4mg 起始用藥整體安全性良好,與安慰劑具有相似的安全性 。
討論時刻:恩那度司他量效關系明確,可根據個體化病情選擇合理劑量方案
多項中日臨床研究數據證實,恩那度司他量效關系明確,初始治療前4周Hb升速呈劑量依賴性(如圖3),4mg起始劑量治療初治患者Hb前4周升速範圍為9.3-11.82g/L,符合中國指南對Hb的初治升幅預期 1,4-5,8-9 。
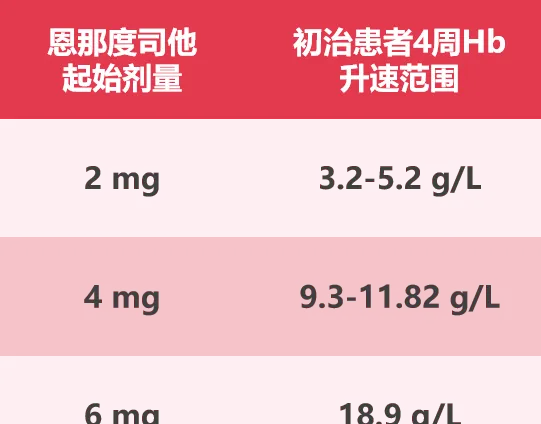
圖3 恩那度司他量效關系明確
同時,綜合中日3期臨床研究結果來看,不論恩那度司他起始治療采用4mg還是2mg,經過治療期間劑量調整,其最終維持用藥階段劑量相似,平均劑量均為3mg左右(圖4-圖5) 4,5 。
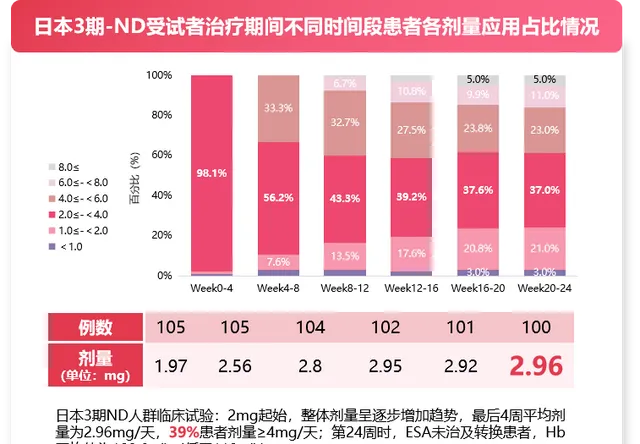
圖4 日本3期-ND受試者治療期間不同時間段患者各劑量套用占比情況

圖5 中國3期臨床試驗不同時間段各劑量套用患者占比
結語
中國3 期臨床數據證實, 恩那度司他4mg 起始治療可有效提升ND-CKD 患者Hb 水平,治療前4 周Hb 升幅為11.82g/L ,符合中國腎性貧血指南初治Hb 升速要求,且用藥整體安全性良好。 臨床上可根據患者個體化病情(Hb 基線值、CKD 分期、期望達標時間等)制訂合理的藥物劑量方案。
參考文獻
1.中國醫師協會腎臟內科醫師分會腎性貧血指南工作群組,陳香美,孫雪峰.中國腎性貧血診治臨床實踐指南[J].中華醫學雜誌,2021,101(20):1463-1502.
2.Liu Bi-Cheng, Tu Yan, Xu Yan, et al. Low vs. Standard Starting Dose Oral Roxadustat for Treating Anemia in Chinese Patients with CKD on Dialysis: A Prospective, Randomized Clinical Trial. ASN. Abstract: TH-PO981.
3.Li Ping, Cai Guangyan, Sun Xuefeng, et al. A Randomized, Controlled, Open-Label, Multicenter Study Evaluating the Efficacy and Safety of Lower Starting Dose Roxadustat for Anemia Treatment in Patients with CKD Not on Dialysis. ASN. Abstract: TH-PO1157.
4.恩那度司他片治療非透析依賴性貧血CKD患者:一項隨機、雙盲、安慰劑對照、平行、多中心III期臨床試驗. CSN 2023.PO-0743
5.Akizawa T, Nangaku M, Yamaguchi T, et al. A Phase 3 Study of Enarodustat in Anemic Patients with CKD not Requiring Dialysis: The SYMPHONY ND Study. Kidney Int Rep. 2021, 6(7):1840-1849.
6.Akizawa T, Nangaku M, Yamaguchi T, et al. Two long-term phase 3 studies of enarodustat (JTZ-951) in Japanese anemic patients with chronic kidney disease not on dialysis or on maintenance hemodialysis: SYMPHONY ND-Long and HD-Long studies. Ther Apher Dial. 2022, 26(2):345-356.
7.Akizawa T, Nangaku M, Yamaguchi T, et al. A Placebo-Controlled, Randomized Trial of Enarodustat in Patients with Chronic Kidney Disease Followed by Long-Term Trial. Am J Nephrol. 2019;49(2):165-174.
8.Fujikawa R, Nagao Y, Fujioka M, Akizawa T. Treatment of anemia associated with chronic kidney disease with the HIF prolyl hydroxylase inhibitor enarodustat: A review of the evidence. Ther Apher Dial. 2022;26(4):679-693.
9.Akizawa T, Nangaku M, Yamaguchi T, et al. A Phase 3 Study of Enarodustat (JTZ-951) in Japanese Hemodialysis Patients for Treatment of Anemia in Chronic Kidney Disease: SYMPHONY HD Study. Kidney Dis (Basel). 2021;7(6):494-502.












