本文為轉化醫學網原創,轉載請註明出處
作者:Sophia
導讀:
Von Hippel-Lindau (VHL) 蛋白在透明細胞腎細胞癌 (ccRCC) 中經常發生突變,是參與氧化應激的缺氧誘導因子 (HIF) 的主要調節因子。然而,VHL是否具有HIF非依賴性腫瘤抑制活性仍不清楚。
近日,浙江大學許大千、呂誌民及哈爾濱醫科大學雷博共同通訊在EMBO Journal 線上發表題為「VHL suppresses autophagy and tumor growth through PHD1-dependent Beclin1 hydroxylation」的研究論文,
研究證明 VHL 透過直接結合 PHD1 在 P54 羥基化的 Beclin1 並抑制 ATG14 與 Beclin1/VPS34 的結合來抑制 ccRCC 細胞中營養應激誘導的自噬。Beclin1 P54A 敲入表達消除了 VHL 介導的自噬抑制並促進腫瘤生長。
研究背景
01
Von Hippel-Lindau(VHL)腫瘤抑制基因的體細胞突變在散發性腎細胞癌(RCC)中普遍存在,其中明確細胞腎細胞癌(ccRCC)是最常見的亞型。VHL蛋白(VHL)作為一個伏林支架蛋白(CUL2)-環泛素連線酶復合物的受質辨識模組,結合到缺氧誘導因子(HIF)1/2α上。這種結合依賴於HIF1/2α中兩個保守脯胺酸殘基的水化,由脯胺酸羥化酶酶(PHD1,又稱EGLN2)、PHD2(EGLN1)和PHD3(EGLN3)催化,這些酶需要氧氣作為輔基質。因此,PHD介導的HIF1/2α水化導致VHL介導的HIF1/2α泛素化和在正常氧化條件下降解,但在低氧條件下,PHD的活性被低氧水平抑制,導致增強的HIF1/2α表達誘導下遊基因表現。VHL患者腎臟中出現的VHL缺陷病變顯示出HIF和HIF靶基因的增加,小鼠VHL–/– ccRCC異種移植實驗顯示HIF2α促進腫瘤的作用,而HIF1α限制腫瘤的作用。然而,
一些VHL–/–ccRCC細胞系不受HIF2α活性操縱的影響,一些VHL突變的ccRCC對HIF2α抑制劑治療具有抵抗性,這表明VHL缺陷透過尚未確定的和與HIF2α無關的機制促進腫瘤發展。
研究進展
02
為了進一步確定VHL介導的自噬抑制的臨床相關性,我們對具有WT-VHL表達的人ccRCC標本進行了IHC或免疫墨點分析,並顯示Beclin1 P54-OH水平與自噬水平呈負相關,如LC3B增加和p62表達降低所反映(圖6A-C)。此外,腫瘤中Beclin1 P54-OH含量低的ccRCC患者(49例)的生存時間短於腫瘤中Beclin1 P54-OH含量高的患者(41例)(圖6D)。
這些結果支持了VHL介導的自噬抑制在人ccRCC臨床行為中的作用,並揭示了Beclin1 P54-OH水平與ccRCC臨床侵襲性之間的關系。
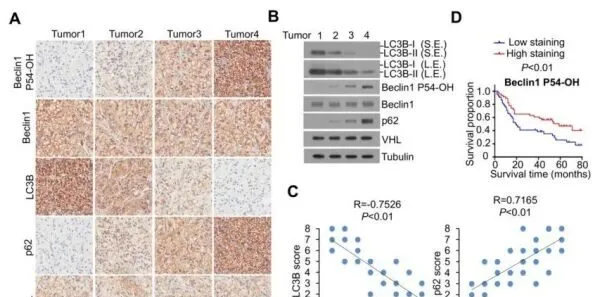
Beclin1 P54-OH 水平與人 ccRCC 中的自噬水平呈負相關,可預測患者的不良預後
研究結果
03
本研究,我們證明 VHL 抑制營養應激誘導的自噬,其在散發性 ccRCC 標本中的缺乏與自噬水平顯著升高有關,並與較差的患者預後相關。從機制上講,
VHL 在 Pro54 上發生 PHD1 介導的羥基化後,直接與自噬調節因子 Beclin1 結合。這種結合抑制了 Beclin1-VPS34 復合物與 ATG14L 的結合,從而抑制了響應營養缺乏的自噬啟動。
非羥基化Beclin1 P54A的表達消除了VHL介導的自噬抑制作用,並顯著降低了VHL的腫瘤抑制作用。此外,在表達野生型VHL的人ccRCC標本中,Beclin1 P54-OH水平與自噬水平呈負相關,並且與患者預後不良呈負相關。此外,VHL缺陷小鼠腫瘤與自噬抑制劑和HIF2α抑制劑聯合治療可抑制腫瘤生長。這些發現揭示了VHL抑制腫瘤生長的意想不到的機制,並提出了透過聯合抑制自噬和HIF2α來治療ccRCC的潛在方法。
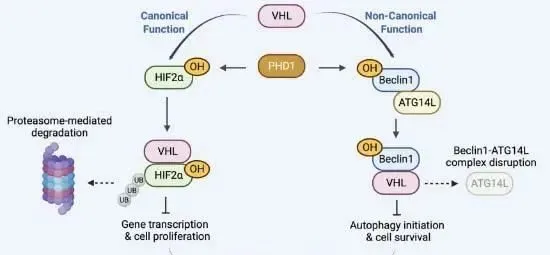
PHD1介導的脯氨酰羥基化靶向HIF-1α進行VHL依賴性泛素化,是細胞氧傳感機制的關鍵步驟。這項工作表明,PHD1 和 VHL 還抑制 Beclin1 和自噬起始,失調導致透明細胞腎細胞癌進展。
參考資料:
註:本文旨在介紹醫學研究進展,不能作為治療方案參考。如需獲得健康指導,請至正規醫院就診。











