
2 型糖尿病是(Diabetes type)一種復雜的代謝性疾病,其發病機理涉及多個層面,包括遺傳因素、環境因素以及細胞和分子水平的變化。
一、遺傳因素
2 型糖尿病具有明顯的遺傳傾向。從分子角度來看,多個基因的變異與 2 型糖尿病的發病密切相關。
1. 胰島素相關基因
- 胰島素基因的突變可能影響胰島素的合成、加工或分泌。例如,某些突變可能導致胰島素前體的折疊錯誤,使其無法正確加工為有活性的胰島素,進而影響血糖的調節。
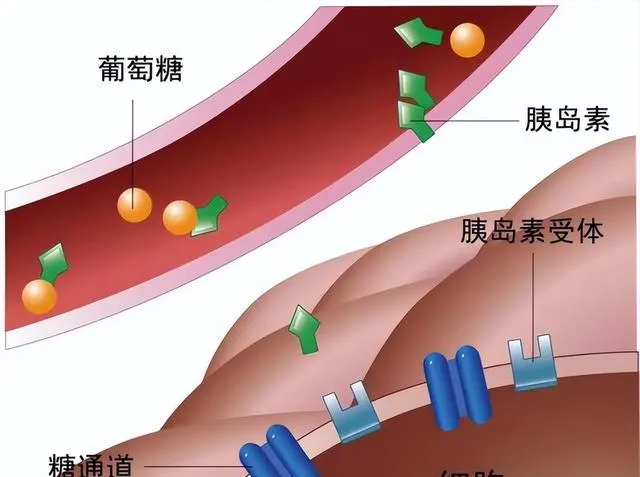
- 胰島素受體基因的變異也較為重要。胰島素受體是胰島素訊號傳導的關鍵分子,基因突變可能導致胰島素受體的結構和功能異常,使其對胰島素的親和力降低,影響胰島素訊號的傳遞,從而引起胰島素抵抗。
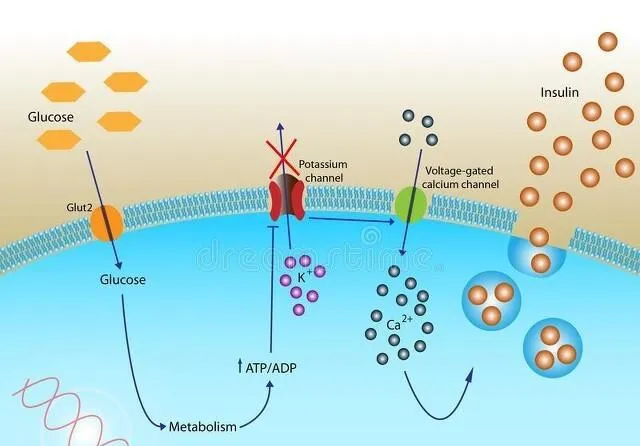
2.細胞代謝相關基因
- 與葡萄糖轉運和代謝有關的基因,如葡萄糖轉運蛋白 4(GLUT4)基因。GLUT4 負責將葡萄糖轉運到細胞內進行代謝,其基因表現或功能異常可導致細胞攝取葡萄糖的能力下降。例如,某些遺傳變異可能影響 GLUT4 的轉錄調控,使其在細胞表面的表達減少,導致細胞對葡萄糖的攝取不足,血糖水平升高。
- 參與糖原合成和分解的基因也可能影響 2 型糖尿病的發生。糖原合成酶基因的突變可能導致糖原合成減少,而糖原磷酸化酶基因的突變可能使糖原分解過度,這些都會影響血糖的平衡。
3.轉錄因子和訊號通路相關基因
- 某些轉錄因子如過氧化體增殖物啟用受體γ(PPARγ)在脂肪細胞分化和胰島素敏感性調節中起關鍵作用。PPARγ 基因的變異可能影響其對靶基因的調控,導致脂肪細胞功能異常,進而引發胰島素抵抗。
- 細胞內的訊號通路分子,如磷脂酰肌醇 3 - 激酶(PI3K)和蛋白激酶 B(Akt)等相關基因的突變,也會幹擾胰島素訊號傳導。PI3K 是胰島素訊號通路中的重要分子,它被啟用後可以磷酸化多種受質,調節細胞的代謝、增殖和存活等過程。PI3K 基因的突變可能導致其活性降低,影響下遊訊號的傳遞,使細胞無法有效地響應胰島素的作用,產生胰島素抵抗。
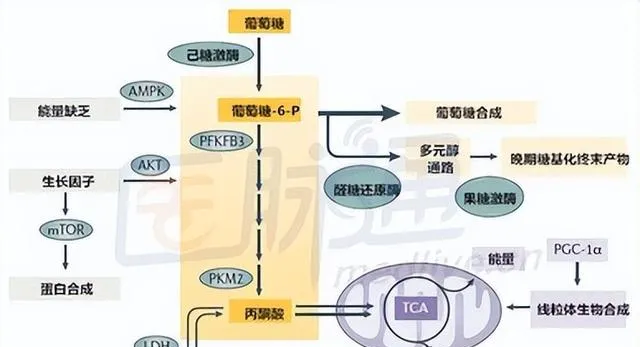
二、環境因素
1.飲食因素
- 長期高熱量、高脂肪、高糖飲食是 2 型糖尿病的重要環境誘因。從分子角度看,過多的熱量攝入,尤其是飽和脂肪和簡單碳水化合物,會導致細胞內脂質代謝紊亂。例如,過多的脂肪酸可在肌肉、肝臟等組織中沈積,形成脂毒性。
- 脂毒性可透過多種機制影響細胞功能。一方面,它可以幹擾胰島素訊號傳導。脂肪酸可以啟用一系列細胞內的訊號通路,如絲裂原活化蛋白激酶(MAPK)通路,該通路的過度啟用會抑制胰島素訊號通路。另一方面,脂肪酸可誘導細胞產生氧化應激,產生過多的活性氧(ROS)。ROS 可以損傷細胞內的蛋白質、脂質和 DNA,影響胰島素受體和下遊訊號分子的功能,導致胰島素抵抗。
- 高糖飲食可導致細胞內葡萄糖濃度過高,引起一系列代謝應激反應。例如,葡萄糖可以透過多元醇通路代謝增加,該通路的啟用會消耗還原型輔酶Ⅱ(NADPH),同時產生山梨醇等物質,山梨醇在細胞內積累可導致細胞滲透壓升高,損傷細胞功能。此外,高糖還可以促進晚期糖基化終末產物(AGEs)的形成。AGEs 可以與細胞表面的受體結合,啟用一系列細胞內訊號通路,導致炎癥反應和氧化應激,進而損害細胞功能,引起胰島素抵抗。
2. 缺乏運動
- 缺乏運動可導致肌肉組織對葡萄糖的攝取和利用減少。從分子水平來看,運動可以啟用一系列訊號通路,促進 GLUT4 從細胞內轉位到細胞膜表面,增加細胞對葡萄糖的攝取。而缺乏運動時,這些訊號通路活性降低,GLUT4 轉位減少,細胞攝取葡萄糖的能力下降。
- 此外,缺乏運動還會導致脂肪堆積,尤其是腹部脂肪的增加。脂肪細胞會分泌多種脂肪細胞因子,如瘦素、脂聯素等。在肥胖狀態下,瘦素抵抗和脂聯素水平降低較為常見。瘦素是一種由脂肪細胞分泌的激素,它可以調節食欲和能量代謝。當發生瘦素抵抗時,大腦對瘦素的訊號不敏感,導致食欲增加和能量攝入過多。脂聯素具有抗炎、增加胰島素敏感性等作用,其水平降低會削弱機體對胰島素的敏感性,促進胰島素抵抗的發生。
3. 長期精神壓力
- 長期精神壓力可透過神經內分泌系統影響血糖代謝。在應激狀態下,下丘腦 - 垂體 - 腎上腺軸(HPA 軸)被啟用,導致腎上腺皮質分泌過多的糖皮質激素。糖皮質激素可以透過多種分子機制影響血糖代謝。它可以促進肝臟的葡萄糖新生,增加葡萄糖的輸出;同時,糖皮質激素還可以抑制肌肉和脂肪組織對葡萄糖的攝取和利用,導致血糖升高。
- 此外,精神壓力還可以引起自主神經系統功能紊亂。交感神經興奮會釋放去甲腎上腺素等神經遞質,這些神經遞質可以透過啟用細胞內的訊號通路,如 cAMP - 蛋白激酶 A(PKA)通路,抑制胰島素訊號傳導,導致胰島素抵抗。

三、胰島素抵抗與胰島β細胞功能缺陷
1. 胰島素抵抗
胰島素抵抗是 2 型糖尿病的早期關鍵特征。在分子水平上,胰島素與胰島素受體結合後,會啟用胰島素受體受質(IRS),進而啟用 PI3K - Akt 等訊號通路。在胰島素抵抗狀態下,IRS 的酪胺酸磷酸化減少,而絲胺酸/蘇胺酸磷酸化增加。絲胺酸/蘇胺酸磷酸化會幹擾 IRS 與胰島素受體的結合以及下遊訊號的傳遞。例如,炎癥細胞因子如腫瘤壞死因子 -α(TNF -α)、白細胞介素 - 6(IL - 6)等可以啟用一系列激酶,導致 IRS 的絲胺酸/蘇胺酸磷酸化增加。
此外,胰島素抵抗還與細胞內脂質代謝異常密切相關。過多的脂肪酸及其代謝產物可以抑制胰島素訊號傳導。例如,二酰甘油(DAG)可以啟用蛋白激酶 C(PKC),PKC 可以磷酸化 IRS 等分子,抑制胰島素訊號通路。同時,脂肪酸氧化產生的乙酰輔酶 A 可以進入細胞核,調節基因表現,影響與糖脂代謝相關酶的合成和活性,進一步加重胰島素抵抗。
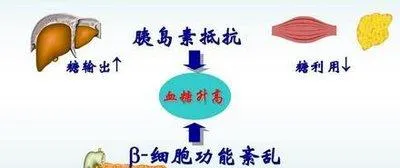
2.胰島β細胞功能缺陷
- 隨著胰島素抵抗的持續存在,胰島β細胞需要代償性地增加胰島素分泌來維持血糖正常。然而,長期的高負荷工作會導致胰島β細胞功能逐漸減退。從分子角度來看,長期高血糖可透過多種機制損害胰島β細胞功能。例如,高血糖可引起氧化應激,產生過多的 ROS,損傷胰島β細胞內的線粒體功能,影響能量產生和細胞代謝。
- 高血糖還可以啟用一系列應激訊號通路,如未折疊蛋白反應(UPR)。當細胞內未折疊或錯誤折疊的蛋白質積累時,UPR 被啟用,試圖恢復細胞內的蛋白質穩態。但如果應激持續存在,UPR 可能會誘導細胞雕亡。此外,長期高血糖可導致胰島β細胞的基因表現發生改變,影響胰島素的合成和分泌相關基因的表達。同時,胰島素抵抗狀態下,脂肪細胞和肌肉細胞分泌的一些細胞因子,如脂聯素、抵抗素等,也可以透過旁分泌或內分泌的方式影響胰島β細胞的功能。
綜上所述,2 型糖尿病是遺傳因素和環境因素相互作用的結果,其發病機理涉及多個分子層面的變化,包括基因變異導致的細胞功能異常、環境因素引起的代謝紊亂以及胰島素抵抗和胰島β細胞功能缺陷等。深入理解這些發病機理對於 2 型糖尿病的預防、診斷和治療具有重要意義。未來,隨著對 2 型糖尿病分子機制研究的不斷深入,有望開發出更加有效的治療方法和策略,以更好地控制血糖,預防並行癥的發生。











