上一篇我们介绍了TMB的定义、检测技术以及临床意义,尽管2020年我国颁布了【肿瘤突变负荷检测及临床应用专家共识(2020版)】(以下简称「共识」),认可了TMB对于免疫治疗的预测作用,但同时也指出了一些不足,本篇就来聊一聊 当下基因检测市场上的TMB检测究竟存在哪些问题 。
1
tTMB与bTMB的一致性
既往TMB的检测都是基于组织样本检测,随着近年来「液态活检」概念的兴起,将血液样本用于基因检测也越来越常见,根据使用样本的不同,TMB也进一步细分为 使用组织样本的tTMB和使用血液样本的bTMB 。两者的检测与计算方式基本一致,但由于样本本身的区别,因此即便是同一个患者的样本也会有不同结果。
2017年由Koeppel等通过WES分析了32名不同肿瘤患者组织样本及血液样本计算TMB数据,结果发现血液样本计算TMB的灵敏度仅为组织样本的53%,推断可能是因为血液中ctDNA的总量影响了检测及计算结果 [1] 2019年的ESMO会议上发表一则简报,纳入39例不同癌种患者对比bTMB与tTMB及疗效的关系,31例患者用血液检测,21例患者用组织检测,结果bTMB中位值为5(1-53)mut/Mb,而tTMB中位值则为6(2-124)mut/Mb,其中有16例患者的血液及组织样本都检测了,发现TMB值存在一定相关性(r=0.67; p < 0.01)。然而2021年陆续有研究结果 [2、3] 表明其对应的bTMB中位值要高于tTMB中位值,且bTMB与tTMB可能存在正相关。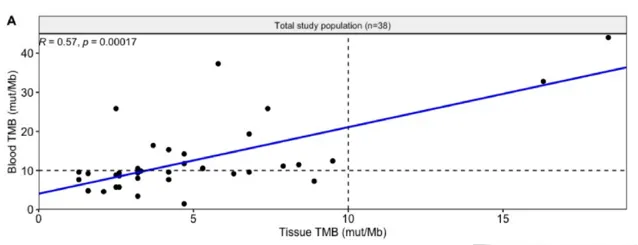
另外,MYSTIC研究中提及血液检测TMB的成功率高于组织样本, 导致组织样本检测失败的主要原因包括:
(1)组织中肿瘤细胞/肿瘤DNA不足,占66.2%;
(2)DNA提取量不足,占12.3%;
(3)建库质量不合格,占21.5%。
归根结底,虽然目前的研究表明 患者的bTMB与tTMB存在相关性 ,但bTMB的计算结果可能高于或低于tTMB,两者并不是完全相等。【共识】第三条也认可了两者的相关性,并且也提出bTMB检测目前缺乏统一标准。
2
很多病友也做过许多功课,知道 无论癌种,TMB-H人群使用免疫治疗的有效率都比较高 ,那么问题来了,究竟多高才属于TMB-H呢?对于这种数值类的指标,我们通常会设定cut-off值(或阈值)用于划分高、中、低三档,但【共识】第七条提出「不同靶向测序Panel的TMB检测体系之间TMB阈值不能通用」(注:这里的「靶向测序Panel」即通俗所说的「大Panel」或「全基因」)。
实际上不仅仅是不同「靶向测序Panel」间的TMB阈值不能通用,即便同样使用WES检测,在不同研究中划定的阈值也有不同。
2018年Translational Lung Cancer Research上发表了一篇NSCLC中组织样本及血液样本TMB计算的综述,该综述回顾了既往临床研究中TMB检测的方式、样本及cut-off值。
结果可以看到,Keynote-001、CheckMate-026以及CheckMate-012三大研究均采用WES方式检测且均使用肿瘤组织样本。然而三个研究的cut-off值却完全不同,Keynote-001设置200 mut以上;CheckMate-026则更细致的设置100以下为低,100-242之间为中等,242以上为高;CheckMate-012则又划定高于158即为高。
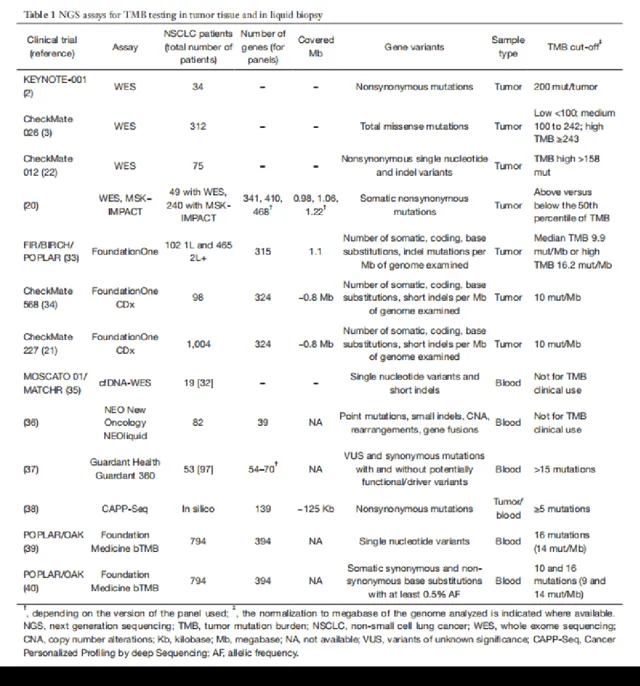
WES(全外显子)作为TMB检测的金标准,在不同的临床研究中cut-off值尚有不同,不同检测公司的全基因检测Panel连包含基因数量、Panel大小以及TMB计算方式都有不同,其cut-off值更加不能通用。甚至上表中,同为Foundation Medicine公司的检测Panel——FoundationOne与FoundationOne CDx两款套餐,前者包含315个基因,后者包含324个基因,两者的TMB阈值设置也完全不同。

样本类型也同样会影响阈值划分,毕竟我们刚才已经说过即便同一个病人的bTMB与tTMB都不完全相同,bTMB也需要采用适合自身的阈值,如Foundation Medicine bTMB检测包含394个基因,阈值划分又与前两个套餐不同。
归根结底,TMB毕竟是人为定义的统计学概念,所谓TMB-L、TMB-M以及TMB-H也是人为划定, 缺乏统一规范 ,不同检测Panel、不同样本、结果都不相同,与基因突变不同,后者是客观存在、有客观标准的。
目前国内市场上基因检测公司层出不穷,为了区别于其他竞争公司,每家公司的全基因套餐包含的基因数量都不同,那么必然带来TMB阈值不统一的问题,各家公司都有各自的划分标准, 因此可能存在同一个病人经不同公司检测,一家判定TMB-H另一家则不是的尴尬情况,从而影响对于免疫治疗收益的预测。
另外目前多数关于TMB的研究基于欧美人群较多, 缺乏中国人群数据,不便建立中国人群统一的TMB阈值, 即便部分公司的检测Panel与WES金标准一致性高,也暂不推荐作为中国人群统一标准。从这一点出发, 目前国内大多数的TMB-H人群划分是有些混乱的 。

图片来源:摄图网
预测作用存在局限,
TMB-H就等于免疫治疗获益吗?
2020年,FDA批准「K药」用于TMB-H(≥10 mut/Mb)的成人与儿童实体瘤患者,很多患者正是通过这条资讯认识了TMB与免疫治疗的关系(补充一点,此处TMB阈值划分是基于FoundationOne CDx,并非通用标准)。
「K药」的这项适应症是基于Keynote-158研究的亚组分析结果,有1050例不同癌种的患者是截止日期前至少26周纳入研究的,有足够的观测随访时间,其中有790例检测计算了TMB值,102例为TMB-H(≥10 mut/Mb),结果表明TMB-H组的ORR为29%,非TMB-H组的ORR仅为6%,TMB-H组的两年PFS率为22%,而非TMB-H组则为7%,由此可以看到, TMB-H组人群接受免疫治疗的有效率相对更高,获益可能性相对大一些 。
除了Keynote-158以外,还有多项研究发现TMB-H人群可能从免疫治疗中获益,而我们前面已经提到过不同研究、不同检测Panel计算得到的TMB与其阈值都是不同的,这也就意味着虽然TMB-H人群可能从免疫治疗中获益,但我们却没有通用的方式可以找出这部分人群,有可能因为TMB阈值划定的不同,导致一部分潜在获益的人群被遗漏,也可能出现一部分获益较小的人群被纳入。
另外,2019年的一项回顾性分析综合了Keynote-021、Keynote-189以及Keynote-407等研究,分析了TMB对于「K药+化疗」组合的疗效预测。研究者选取了PFS及OS(数据来源Keynote-189以及Keynote-407),还有ORR(数据来源Keynote-021),并以TMB≥175 mut/exome为界限划定阈值来。
结果令人意外,无论TMB高还是低,PFS、OS以及ORR均未表现出显著差异,换句话说, TMB可能对于「K药+化疗」乃至免疫治疗联合化疗这种治疗模式的预测价值有限 。

做个简单归纳,由于检测Panel的多样化,导致TMB的计算与阈值划分不统一,即便TMB-H人群可能从免疫治疗中获益,却难以真正精准区分潜在获益人群,并且随着免疫治疗联合化疗模式的普及,TMB的预测作用也在变小甚至可能无法预测。
4
总结
虽然TMB被当成推荐做诸多「全基因」大Panel检测的理由,也有很多的研究及文献报道表明TMB可能预测免疫治疗的效果,但深入了解后,我们可以看到关于TMB的检测从样本类型、阈值划定以及预测效果上仍存在很多需要讨论的,还未形成统一通用规范。

1
组织样本与血液样本检测得到的
结果之间不能直接换算
组织样本及血液样本均可用于TMB的检测,需采用NGS技术做大Panel,两种样本之间存在一定相关性且均可用于预测免疫治疗的效果,但需要注意的是 组织样本得到的tTMB与血液样本检测得到的bTMB之间并不能直接换算 。
这意味着,我们在实际治疗中,可以用血做「全基因」计算TMB,但需要注意并不能简单的以组织样本的标准来衡量bTMB的高低,这里较为考验检测所自身的水平。
2
TMB值受基因检测公司自身算法
影响较大
衡量TMB高低需要划定阈值,然而不仅是不同样本检测后的阈值不同,检测Panel内包含的基因数量不同也需要划定不同的阈值,且目前各Panel划定的阈值间并不相同。
这就是说各位即便在市场上各家公司的「全基因」检测得到TMB值,
其高低划分也只代表该公司自身算法下的高低,并不能直接套用现有研究中的划分标准
,那么自然也不能直接套用现有研究结论去指导免疫治疗获益情况。
3
TMB值预测免疫治疗联合化疗方案
作用不明显
多个研究的结论证明了TMB可用于预测免疫治疗的获益,但
仅限于单独使用免疫治疗的情况
,当采用免疫治疗联合化疗的方案时,TMB的预测作用则并不显著。由于真实治疗中免疫治疗的有效率比较尴尬,目前很多病友在选择治疗方案时都会直接考虑免疫治疗联合化疗,也让TMB对于这部分病友的价值下降很多。
综上所述,TMB虽然作为免疫治疗的生物标志物已经得到专家及指南的认可,但在实际使用中仍面临诸多潜在问题, 缺乏统一的规范使得实际中各检测公司TMB的参考价值下降 ,加之做TMB检测需选择「全基因」大Panel价格不菲, 各位在选择时可根据自身情况考虑,不必强求 。

参考文献
[1].Koeppel, Florence, et al. "Whole exome sequencing for determination of tumor mutation load in liquid biopsy from advanced cancer patients." PloS one 12.11 (2017): e0188174.
[2].Araujo, D. V., et al. "Blood-based TMB (bTMB) correlates with tissue-based TMB (tTMB) in a multi-cancer phase I IO cohort." Annals of Oncology 30 (2019): v512.
[3].Park, Jewel, et al. "Exploring real-world concordance of tissue mutation burden (TMB) from blood and tissue in patients with solid tumors." medRxiv (2021): 2021-05.











