
撰文丨王聰
編輯丨王多魚
排版丨水成文
乙型肝炎病毒(HBV)是一種嗜肝性、非細胞病變的DNA病毒,因其能夠引起持續性感染而聞名,最終可能導致肝硬化和肝細胞癌。 HBV具有獨特能力,能夠逃避宿主固有免疫系統的檢測,因此在調節急性感染的消退過程中,適應力細胞免疫和體液免疫反應占據了中心地位。尤其是CD8 + T細胞,透過產生抗病毒細胞因子和清除感染的肝細胞,在病毒清除過程中發揮了關鍵作用。然而,在大多數新生兒/圍產期感染和一小部份成年人感染者中,HBV的持續存在凸顯了適應力免疫反應的失敗。
逆轉功能失調的CD8 + T細胞對於治療慢性乙型肝炎至關重要,但具體的分子靶點尚不明確。
2024年6月18日,意大利IRCCS聖拉斐爾科學研究所的研究人員在國際頂尖學術期刊Cell上發表了題為:Therapeutic potential of co-signaling receptor modulation in hepatitis B 的研究論文。
該研究探索了功能失調的HBV特異性CD8 + T細胞的行為和潛在的治療靶點,發現肝細胞啟動可誘導功能失調的CD8+T細胞中的關鍵共訊號受體,長時間的HBV抗原刺激產生一個自我更新的、長壽命的、異質性的T細胞庫,在慢性HBV感染中, 啟用4-1BB(一種T細胞共刺激免疫檢查點分子) 顯示出最高潛力的恢復功能受損的CD8+T細胞。 這項研究提示我們,靶向所有功能受損的T細胞,有望治療慢性HBV感染。

HBV研究中的一個未解之謎是,在感染過程中T細胞何時以及在何處被啟動。傳統的免疫學觀點認為,未成熟淋巴細胞首先在次級淋巴器官中接觸抗原。然而,在HBV感染新生小鼠模型的最新實驗中,提出了一個引人註目的新觀點——肝臟本身可能是初始HBV特異性CD8 + T細胞的主要啟動地點。這種不尋常的環境是由肝血竇的獨特解剖結構所促進的,這可能對隨後的免疫反應產生深遠影響。
值得註意的是,CD8 + T細胞的肝細胞啟動會觸發局部啟用和增殖,但不會將其導向效應細胞。相反,它啟動了一個獨特的分化程式,最終導致T細胞表型失調。盡管這些細胞似乎對IL-2、IL-4、IL-6、IL-7有反應,但利用各種協同抑制受體阻斷或激動性共刺激逆轉這種功能障礙的潛力尚未得到充分探索。考慮到PD-1阻斷的初步臨床試驗結果令人失望,這項研究的意義更加深遠。
近期的研究已經發現了慢性感染和癌癥中存在的多種T細胞亞群,這些T細胞亞群在前進演化上相關聯,對治療性共訊號受體調節的反應各不相同。然而,這種異質性在多大程度上是由肝細胞啟動的,以及由此對每種T細胞亞群對免疫治療幹預的反應產生的影響尚不明確。
新生兒/圍產期的HBV感染通常會經歷一個高病毒復制、低肝臟炎癥的初始階段,這一階段之前被稱為「免疫耐受期」。然而,最近的研究挑戰了這一觀點,揭示了即使在該階段也存在活躍的HBV特異性T細胞反應和肝癌發生事件,因此這一階段被重新命名為「高復制、低炎癥期」(HRLI)。這凸顯了對於HBV感染者盡早開始治療的必要性。
由於抗病毒藥物在感染初期的效力有限,因此,免疫調節成為一種有潛力的補充策略,以增強抗病毒效果。遺憾的是,我們對年輕患者免疫反應的有限了解限制了新型免疫療法的發展。
該研究旨在解決這些不足之處,探索HBV感染導致肝細胞啟動所引起的T細胞功能障礙的特性,並評估逆轉這種功能障礙的治療方法。
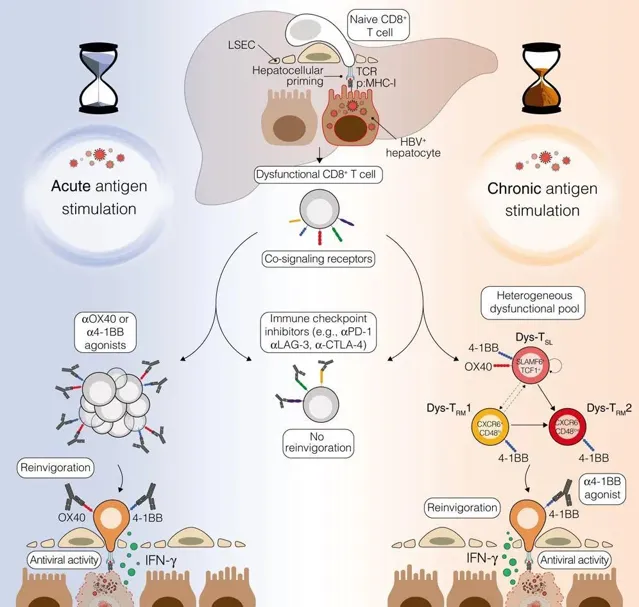
該研究分析了肝細胞啟動期間的共訊號受體,並追蹤了功能受損的HBV特異性CD8 + T細胞的軌跡和命運。早期,這些細胞上調PD-1、CTLA-4、LAG-3、OX40、4-1BB和ICOS的表達。雖然阻斷共抑制受體的效果微乎其微,但啟用4-1BB和OX40將它們轉化為抗病毒效應器。長時間的抗原刺激導致一個自我更新、長壽命、異質性T細胞群體,具有獨特的轉錄組特征,這包括功能受損的祖細胞/幹細胞樣T細胞 (TSL) 和兩種不同的功能受損的組織駐留記憶T細胞(T RM )。雖然4-1BB表達在所有細胞中都得到維持,但OX40表達僅限於T SL 細胞。在慢性感染情況下,只有4-1BB刺激才具有抗病毒活性。
在乙型肝炎E抗原陽性 (HBeAg+) 慢性患者中,4-1BB啟用顯示出最高潛力的恢復功能受損的CD8 + T細胞。這些結果表明,靶向所有功能受損的T細胞,而不是僅靶向T SL 細胞,有望治療慢性HBV感染。
論文連結:
https://www.cell.com/cell/fulltext/S0092-8674(24)00582-8











