
撰文:步步先生
來源:幹細胞者說
● ● ●
衰老是大多數人一生的必經之路。無論你是居廟堂之高,還是處江湖之遠,到了一定年齡,你都要面臨衰老。衰老到底是什麽?如何延緩衰老?人類對衰老的探索和對長壽的追求便從未止步。
當機體衰老了,那麽在衰老過程中會發生哪些明顯的變化呢? 2023年1月,國際頂級學術期刊 Cell 上發表了一篇裏程碑綜述長文 Hallmarks of aging: An expanding universe ,介紹了機體衰老的十二大特征。今天,我們試著解讀一下。
- 01 -
衰老與衰老特征的標準
衰老的特征是 生理完整性的漸進性喪失,導致功能受損和死亡風險增加 。這種衰退是主要人類疾病 (癌癥、糖尿病、心血管疾病和神經退行性疾病等 ) 的主要危險因素。「特征」之間的區別本質上是分散的,因為它們相互作用,彼此不是獨立的。
衰老的特征應滿足以下三個標準:
(1)與年齡相關
(2)可透過實驗可加速衰老,
(3)透過治療幹預,可幹預減緩、停止,甚至逆轉衰老。

圖1:衰老的十二大特征
早在2013年,同樣的本文作者撰寫的經典綜述 The Hallmarks of Aging ,就列舉了代表不同生物體衰老的九大共同特征,特別強調了哺乳動物的衰老。現在,在原有的基礎上,又增加了三個特征,共計十二大特征。
在這篇經典綜述中,作者建議對衰老的十二大特征進行區分,分為五個主要特征: 基因組不穩定,端粒磨損,表觀遺傳改變,蛋白質穩態喪失,巨自噬功能失活 ;三個拮抗特征: 營養感知失調,線粒體功能障礙,細胞衰老 ;還有四個綜合特征: 幹細胞耗竭、細胞間通訊改變、慢性炎癥和生態失調 。
- 02 -
五個主要特征
1
基因組不穩定
衰老有一個共同點:基因損傷在整個生命過程中都存在積累 。基因組的完整性和穩定性,普遍受到外在因素 (包括化學因素、物理因素和生物因素等 ) 和內在因素 (包括DNA復制錯誤、染色體分離缺陷、氧化以及自發水解等) 兩個方面影響。基因組損傷引起的廣泛的遺傳基因病變 (包括點突變、缺失、易位、端粒縮短、單鏈和雙鏈斷裂、染色體重排、核結構缺陷以及病毒或轉座子整合引起的基因破壞) 。

圖2. 基因組不穩定
基因 的改變和 基因組嵌合,都有可能導致衰老的發生。盡管,生物體已經前進演化出復雜的DNA修復和維持機制,用以處理核DNA和線粒體DNA (mtDNA )復制過程 造成的基因損傷。但是,過度的損傷往往會引起基因修復跟不上,衰老便發生了。 基因組穩定系統包含三個方面:核DNA、線粒體DNA、核結構。
一句話: 基因損傷在整個生命過程中都存在積累,一旦修復跟不上損傷,衰老便發生了。
2
端粒磨損
端粒磨損 (染色體末端的DNA) 是衰老發生的原因之一。復制型 DNA聚合酶無法最終完成端粒復制。經過幾輪細胞分裂後,端粒隨之大振幅縮短,導致基因組不穩定,從而導致細胞雕亡/衰老。
端粒縮短可透過增強端粒酶 (端粒酶是一種活性的核糖核蛋白,可延長端粒以保持足夠的長度) 的逆轉錄酶活性來預防 。然而,大多數哺乳動物體細胞不生成端粒酶,這就導致端粒序列的進行性和累積性侵蝕。有例子表明,端粒磨損可透過限制惡性細胞的復制壽命來減弱癌變發生。基因組不穩定有利於腫瘤的發生,而端粒磨損則可能對抗惡性腫瘤。因此,我們認為 端粒磨損是衰老的一個特征,獨立於「 基因組不穩定性 」這一特征 。
▉ 端粒酶活化減緩衰老和治療端粒疾病
人類端粒酶缺乏與某些疾病 (肺纖維化、再生障礙性貧血和先天性角化不良等) 的過早發展有關,影響組織的再生能力。 哺乳動物的正常衰老伴隨著端粒磨損。端粒磨損率受年齡、遺傳變異、生活方式和社會因素的影響。 短端粒長度與衰老相關疾病有因果關系,可進行幹預。例如,啟用端粒酶可對肺纖維化和再生障礙性貧血小鼠模型,有一定治療效果。
一句話: 正常衰老伴隨著端粒磨損,而端粒酶活化可減緩衰老。
3
表觀遺傳改變
隨著年齡增長,細胞 也會發生各種表觀遺傳改變 (包括DNA甲基化模式的改變、組織蛋白的轉譯後修飾、染色質重塑和非編碼RNA的失調功能 ) 。 表觀遺傳的改變通常會影響基因表現和其他細胞過程,從而導致多種與衰老相關疾病 (例如癌癥、神經變性、代謝症候群和骨病 ) 的發展和進展。

圖3. 表觀遺傳改變
表觀遺傳模式的產生和維持需要大量的酶參與 (包括DNA甲基轉移酶、組織蛋白乙酰化酶、去乙酰化酶、甲基化酶和去甲基化酶,以及與染色質重塑或ncRNA合成和成熟有關的蛋白質復合物) 。
一句話: 表觀遺傳改變,可能造成衰老,進而影響整體健康狀況,甚至壽命。
4
蛋白質穩態喪失
對於錯誤折疊或老化蛋白質的降解,機體 是分兩種途徑介導的,分別是 蛋白水解酶和自噬 。

圖4.蛋白質穩態失調和巨自噬功能喪失
衰老和與衰老相關病 (如肌萎縮性側索硬化癥(ALS)、阿爾茨海默病、帕金森病和白內障 ) ,與蛋白質穩態或蛋白質穩態受損有關,導致錯誤折疊、氧化、糖基化或泛素化蛋白質的積累,這些蛋白質通常形成聚集體 (如細胞內包涵體或細胞外澱粉樣斑塊) 。 由於錯誤轉譯、錯誤折疊或不完整蛋白質的生產增強,細胞內的蛋白質平衡可能被破壞。
另一種導致蛋白質穩態網絡崩潰的機制是,蛋白質的轉譯伸長減慢和分健康蛋白質 氧化損傷累積 。 許多與衰老相關的神經退行性疾病 (包括漸凍癥和阿爾茨海默病) ,都可能是由蛋白質突變引起的,這些蛋白質突變在本質上容易發生錯誤折疊和聚集,從而使維持健康狀態所需的蛋白質修復、清除和周轉機制飽和。
一句話: 蛋白質穩態喪失,一是因為蛋白水解酶缺少,二是因為巨自噬功能發生障礙。
5
巨 自噬功能喪失
巨自噬 (自噬分為巨自噬、微自噬和分子伴侶介導的自噬。巨噬也稱自噬、大自噬。 ) 涉及環節包括:將細胞質包裹在雙膜囊泡中,形成自噬體,隨後與溶酶體融合以消化管腔內容物。 自噬不僅參與蛋白質穩態,還影響非蛋白質大分子 (如異位胞質 DNA、脂質囊泡和糖原) 和整個胞器 (包括線粒體自噬靶向的功能失調線粒體,其他胞器以及網狀噬菌體) 以及入侵的病原體。
與衰老相關的自噬下降,是胞器更新減少的最重要機制之一 。舊的不去,新的就不來!自噬作為衰老的新特征是合理的。需要註意的是,參與自噬過程的基因和蛋白質也參與其他降解過程,例如LC3相關的細胞外物質吞噬作用和以外球體形式排出細胞內廢物 (例如,功能失調的線粒體) 隨後被巨噬細胞清除。換句話說,自噬的核心過程也與衰老相關。
一句話: 自噬作用恢復或增強,有效延緩衰老。
- 03 -
三大拮抗特征
1
營養感應失調
營養感應網絡 ( 包括細胞外配體,如胰島素和胰島素樣生長因子、酪胺酸激酶,以及細胞內訊號級聯 ) 在前進演化過程中高度保守。雷帕黴素復合物1 (mTORC1) 的機制靶標,對營養物質 (包括葡萄糖和胺基酸) 和壓力源 (例如缺氧和低能量) 作出反應,從而調節包括轉錄因子 (例如SREBP和TFEB) 在內的多種蛋白質的活性。
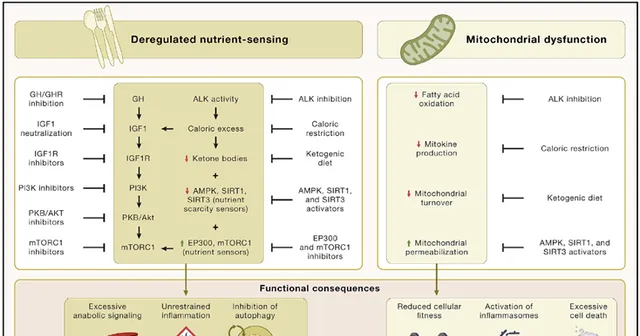
圖5.營養感應失調和線粒體功能障礙
營養感應網絡是細胞裏各種活動 (包括自噬、mRNA 和核糖體生物發生、蛋白質合成、葡萄糖、核苷酸和脂質代謝、線粒體生物發生和蛋白酶體活性) 的中央調節器 。如果營養物質存在且壓力較低,則透過啟用合成代謝來響應營養和壓力狀態,或透過誘導細胞防禦途徑來響應壓力和營養短缺。營養感應網絡組分的基因活性降低,可以延長不同動物模型的壽命和健康壽命。
表觀遺傳年齡 (步步先生註:也就是我們通常說的看起來的年齡) ,也與人體細胞的營養感知有關。 在青年時期,營養感應網絡促進有益合成代謝,但在成年時期反而促衰老。
2
線粒體功能障礙
線粒體功能障礙,一直是衰老 研究 的主要方向 。 線粒體不僅是細胞的動力源,而且也是炎癥觸發因素 (當活性氧或mtDNA從線粒體中泄漏時,分別導致炎癥小體或DNA傳感器的啟用) 和細胞死亡因素 (當半胱天冬酶的活化劑、核酸酶或其他致命酶從膜間隙中釋放出來) 。
隨著年齡的增長,線粒體會因某些機制 (包括線粒體DNA突變的積累、蛋白質穩態不足、胞器周轉減少和線粒體動力學變化) 而出現功能障礙。線粒體功能障礙,損害了線粒體對細胞生物能量的貢獻,增強了活性氧的產生,並可能引發線粒體膜的高度通透性,導致炎癥發生和細胞死亡。
線粒體功能正常對於維持健康至關重要,線粒功能障礙會導致衰老 。
3
細胞衰老
細胞衰老,通常定義為細胞周期的穩定停滯,同時伴隨著表型變化 。細胞衰老是由急性或慢性損傷引起的反應。在人類中,衰老細胞以不同速度在多個組織中積累。當年輕 (<35 歲) 和老年 (>65 歲) 比較 時,衰老細胞速度差異可高達2-20 倍, 衰老主要 影響成纖維細胞、內皮細胞和免疫細胞 。
事實上,即使是緩慢增殖的組織 (如大腦或心臟) ,也可能含有衰老細胞。在許多疾病中,都會發生局竈性或組織特異性衰老細胞積聚。細胞衰老和機體衰老有一定的因果關系,衰老細胞的消除,可延長自然衰老小鼠的健康壽命。 衰老細胞的消除,具有治療衰老相關癥狀的作用 ,並且至少3項臨床試驗已經完成,15項臨床試驗正在進行或計劃針對各種適應癥的衰老。

圖6.細胞衰老
- 04 -
五大綜合特征
1
幹細胞耗竭
組織再生能力下降是衰老最明顯的特征之一 。 幹細胞耗竭,是多種衰老特征的綜合結果,很可能也是組織衰老的罪魁禍首之一。研究表明,透過幹細胞逆轉衰老表型 (步步先生註:這裏的方法之一就是采用「局部重編程 」) ,可以讓返老還童成為一種可能。

圖7.幹細胞耗竭
在衰老與穩定狀態下,組織更新減少與損傷後組織修復受損有關,每個器官都有自己獨特的更新和修復策略 。例如在骨骼肌中的衛星細胞,負責骨骼肌更新和修復。 在高度更新的表皮中,存在諸多幹細胞壁龕 (特別是與毛囊相關的幹細胞壁龕) ,每個壁龕都會產生其後代和區域。一旦表皮受傷,在很大程度上是由非常活躍的幹細胞 (通常稱為「成體幹細胞」或「組織幹細胞」) 更新。相比之下, 其他器官 (如肝臟、肺或胰腺 ) ,具有較低更新頻率的細胞 (如神經元和肌肉纖維) 是由非常稀有的幹細胞群體再生的。
幹細胞對組織穩態,起著至關重要的作用 。 事實上,組織修復在很大程度上依賴於損傷誘導的細胞「去分化 」和「可塑性 」起作用 (例如在腸、腦和肺中,組織損傷會誘導非幹細胞去分化,從而重新啟用通常沈默的「幹性 」轉錄程式,從而獲得組織修復所需的可塑性) 。
相對於正常穩態條件,損傷誘導的可塑性 (可塑性隨著衰老逐漸喪失) 可能與衰老更相關。 「細胞重編程 」,是應對幹細胞衰老的基本策略。 這個過程被認為以細胞自主的方式作用於多種細胞類別;然而,由於其長期影響,它對幹細胞和祖細胞的影響被認為具有更高的相關性。
2
慢性炎癥
衰老相關慢性炎癥,指的是 隨著年齡增長而發展的低度慢性炎癥狀態 。它的 特點是血清中存在高濃度的炎性因子 ,如C反應蛋白 (CRP) 、IL-6、IL-8和TNF。
圖8.慢性炎癥
炎癥發生與衰老相關的多種疾病的發生和死亡率的風險增加有關 。 盡管,炎癥發生最初被認為是衰老相關疾病的生物標誌物,但很多證據表明炎癥發生與衰老相關組織退化之間存在因果關系。臨床試驗表明,一些非甾體抗炎藥以及IL-1和TNF的中和作用可以延緩心血管疾病的發展。
血漿中升高的IL-6水平,是慢性炎癥的預測性生物標誌物 。隨著炎癥的加劇,免疫功能下降,這種現象可以透過組織血液中的骨髓和淋巴細胞進行高維監測來捕捉。
T細胞群的變化,可導致促炎性Tp和Tp7細胞 功能亢進、免疫監視缺陷 (對病毒感染、惡性或衰老細胞的消除有負面影響 ) 、 自身耐受性喪失 (導致自身免疫疾病中年齡相關的增加) 以及 生物屏障的維持和修復減少 ,從而導致全身性炎癥的發生。
盡管,全身性炎癥在機制上與衰老有關,但炎癥本身就是一個特征。事實上,對炎癥和免疫系統的特定操作,可以加速或減緩不同器官系統的衰老過程。
3
細胞間通訊改變
衰老與細胞間通訊改變有關,這會損害穩態和激素調節 。因此,衰老涉及神經、神經內分泌和激素 (包括腎上腺素能、多巴胺能和基於胰島素/IGF1 和腎素-血管緊張素系統,以及性激素 ) 訊號通路的缺陷。
雖然,細胞間通訊改變的主要原因是細胞內在驅動的,但這些紊亂最終歸結為一個特征。這個特征包括炎癥反應的增加,免疫監視能力下降,以及人類基因組和菌群交流的改變,最終導致生態失調。
衰老研究都集中在尋找具有促衰老或延長壽命的血液因素、細胞間不同通訊系統的作用,以及對衰老過程中ECM破壞的功能相關性的評估。
4
生態 失衡
腸道菌群,已成為多種生理過程的關鍵因素 。例如營養消化和吸收、抵禦病原體以及產生必需代謝物 (包括維生素、胺基酸衍生物、次級膽汁酸和短鏈脂肪酸) 。
 圖9.腸道菌群生態失衡
圖9.腸道菌群生態失衡
腸道菌群還會向外周和中樞神經系統,以及其他遠處器官發出訊號,並對宿主健康的整體維持產生至關重要的作用。 腸道菌群生態失調與許多疾病有關,例如肥胖、2 型糖尿病、潰瘍性結腸炎、神經系統疾病、心血管疾病和癌癥 。
對百歲老人腸道菌群代謝組學和功能分析表明, 在某些特定細菌中Alistipes putredinis 和 Odoribacter splanchnicus 富集。其中一些細菌,能產生特定的次級膽汁酸,對革蘭氏陽性多藥耐藥病原體 (如艱難梭菌和糞腸球菌) 具有強大的抗菌作用。因此,特定的膽汁酸代謝可能參與降低致病菌感染的風險並有助於腸道穩態,從而降低對與衰老相關的慢性疾病的易感性。
- 05 -
文末小結
「逝者如斯夫」,隨著年齡不斷增長,人類總會與衰老不期而遇。 衰老的所有十二個特征都彼此密切相關 。 文章上面也提到了,衰老的特征可分為三個類別:
主要特征有五個:基因組不穩定性、端粒磨損、表觀遺傳改變、 蛋白質穩態喪失、巨自噬能力的喪失 。這五大主要特征是 基本特征 。
拮抗特征有三個:營養感知失調,線粒體功能障礙,細胞衰老。這三大次要特征是可逆的特征,其功能隨年齡變化可能出現相反的情況。
綜合特征有四個:幹細胞耗竭、細胞間通訊改變、慢性炎癥和生態失衡。這四大特征更具體化,直接造成衰老,這些共同決定了衰老的速度。

圖10.衰老特征在功能上相互關聯
在實驗性延緩衰老幹預水平上,衰老的十二大特征密切關系 也很明顯,通常幹預會同時針對幾個特征。因此,SIRT活化劑 (包括NAD+前體 ) 減弱了基因組的不穩定性 (透過DNA修復) ,表觀遺傳改變 (透過組織蛋白去乙酰化) ,蛋白質平衡的喪失 (透過蛋白質聚集物的去除) ,失活的宏自噬 (透過自噬增強) ,營養感應失調 (透過啟用營養缺乏傳感器) ,以及線粒體功能障礙 (透過增加線粒體依賴的質素控制) 。而腸道菌群的代謝物亞精胺與DNA形成復合物 (可抵消基因組不穩定性) ,會影響蛋白轉譯 (避免蛋白質穩態的喪失) ,刺激巨自噬,逆轉淋巴細胞衰老,防止肌肉幹細胞衰竭,維持晝夜節律,抑制炎癥,刺激癌癥免疫監測。
健康長壽是人類的終極目標,而健康長壽意味著要對抗衰老和疾病 。 最後,作者假設存在八個健康特征,其中包括空間劃分的組織特征 (屏障的完整性和局部擾動的遏制) ,隨著時間的推移維持體內平衡 (迴圈和周轉,電路整合和節奏振蕩) 。毫無疑問,衰老與健康的這八個特征的逐漸退化有關,這意味著維持空間劃分能力隨著衰老在不斷下降。這種下降影響了器官組織的所有八個層次,跨越不同類別的 分子 (如DNA、RNA、蛋白質和代謝產物) 、 胞器 (如細胞核、線粒體和溶酶體) 、 細胞類別 (如實質細胞、基質細胞和免疫細胞) 、構成器官最小功能實體的 超細胞單位 、解剖邊界內的 整個器官 、 器官系統 (如胃腸道、呼吸道和泌尿道) 、 系統回路 (內分泌、神經、淋巴和血管連線) 以及 元生物 (包括菌群) 。
評估延緩衰老幹預措施, 第一個臨床試驗必須涉及預防或減輕與衰老相關的病理,而不是衰老本身 。 衰老特征的新方向,可能為制定旨在延長健康壽命的有效幹預措施提供了一個改進的框架。 衰老研究是一條任重而道遠的路。
參考文獻:
[1]https://www.cell.com/cell/fulltext/S0092-8674(22)01377-0
[2]https://www.cell.com/cell/fulltext/S0092-8674(13)00645-4
註:本文旨在介紹醫藥健康研究進展,不是治療方案推薦。如需獲得治療方案指導,請前往正規醫院就診。
【自然 · 綜述】:T細胞在衰老中的角色
— END —
- 科普 情懷 責任 -











