上一篇我們介紹了TMB的定義、檢測技術以及臨床意義,盡管2020年中國頒布了【腫瘤突變負荷檢測及臨床套用專家共識(2020版)】(以下簡稱「共識」),認可了TMB對於免疫治療的預測作用,但同時也指出了一些不足,本篇就來聊一聊 當下基因檢測市場上的TMB檢測究竟存在哪些問題 。
1
tTMB與bTMB的一致性
既往TMB的檢測都是基於組織樣本檢測,隨著近年來「液態活檢」概念的興起,將血液樣本用於基因檢測也越來越常見,根據使用樣本的不同,TMB也進一步細分為 使用組織樣本的tTMB和使用血液樣本的bTMB 。兩者的檢測與計算方式基本一致,但由於樣本本身的區別,因此即便是同一個患者的樣本也會有不同結果。
2017年由Koeppel等透過WES分析了32名不同腫瘤患者組織樣本及血液樣本計算TMB數據,結果發現血液樣本計算TMB的靈敏度僅為組織樣本的53%,推斷可能是因為血液中ctDNA的總量影響了檢測及計算結果 [1] 2019年的ESMO會議上發表一則簡報,納入39例不同癌種患者對比bTMB與tTMB及療效的關系,31例患者用血液檢測,21例患者用組織檢測,結果bTMB中位值為5(1-53)mut/Mb,而tTMB中位值則為6(2-124)mut/Mb,其中有16例患者的血液及組織樣本都檢測了,發現TMB值存在一定相關性(r=0.67; p < 0.01)。然而2021年陸續有研究結果 [2、3] 表明其對應的bTMB中位值要高於tTMB中位值,且bTMB與tTMB可能存在正相關。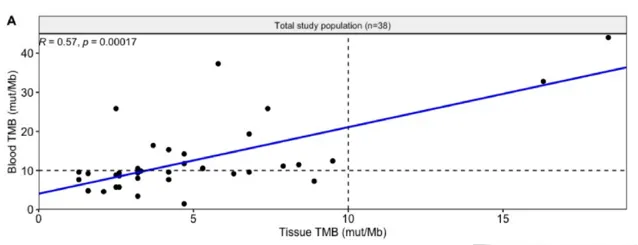
另外,MYSTIC研究中提及血液檢測TMB的成功率高於組織樣本, 導致組織樣本檢測失敗的主要原因包括:
(1)組織中腫瘤細胞/腫瘤DNA不足,占66.2%;
(2)DNA提取量不足,占12.3%;
(3)建庫質素不合格,占21.5%。
歸根結底,雖然目前的研究表明 患者的bTMB與tTMB存在相關性 ,但bTMB的計算結果可能高於或低於tTMB,兩者並不是完全相等。【共識】第三條也認可了兩者的相關性,並且也提出bTMB檢測目前缺乏統一標準。
2
很多病友也做過許多功課,知道 無論癌種,TMB-H人群使用免疫治療的有效率都比較高 ,那麽問題來了,究竟多高才屬於TMB-H呢?對於這種數值類的指標,我們通常會設定cut-off值(或閾值)用於劃分高、中、低三檔,但【共識】第七條提出「不同靶向測序Panel的TMB檢測體系之間TMB閾值不能通用」(註:這裏的「靶向測序Panel」即通俗所說的「大Panel」或「全基因」)。
實際上不僅僅是不同「靶向測序Panel」間的TMB閾值不能通用,即便同樣使用WES檢測,在不同研究中劃定的閾值也有不同。
2018年Translational Lung Cancer Research上發表了一篇NSCLC中組織樣本及血液樣本TMB計算的綜述,該綜述回顧了既往臨床研究中TMB檢測的方式、樣本及cut-off值。
結果可以看到,Keynote-001、CheckMate-026以及CheckMate-012三大研究均采用WES方式檢測且均使用腫瘤組織樣本。然而三個研究的cut-off值卻完全不同,Keynote-001設定200 mut以上;CheckMate-026則更細致的設定100以下為低,100-242之間為中等,242以上為高;CheckMate-012則又劃定高於158即為高。
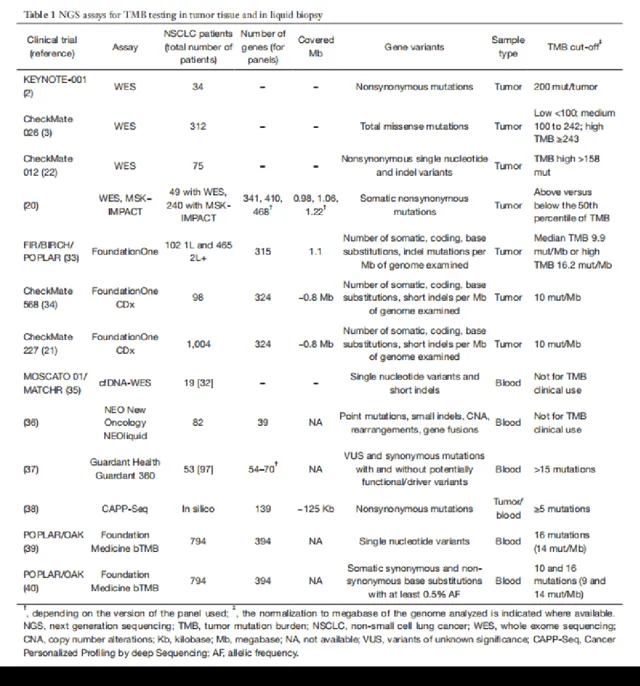
WES(全外顯子)作為TMB檢測的金標準,在不同的臨床研究中cut-off值尚有不同,不同檢測公司的全基因檢測Panel連包含基因數量、Panel大小以及TMB計算方式都有不同,其cut-off值更加不能通用。甚至上表中,同為Foundation Medicine公司的檢測Panel——FoundationOne與FoundationOne CDx兩款套餐,前者包含315個基因,後者包含324個基因,兩者的TMB閾值設定也完全不同。

樣本類別也同樣會影響閾值劃分,畢竟我們剛才已經說過即便同一個病人的bTMB與tTMB都不完全相同,bTMB也需要采用適合自身的閾值,如Foundation Medicine bTMB檢測包含394個基因,閾值劃分又與前兩個套餐不同。
歸根結底,TMB畢竟是人為定義的統計學概念,所謂TMB-L、TMB-M以及TMB-H也是人為劃定, 缺乏統一規範 ,不同檢測Panel、不同樣本、結果都不相同,與基因突變不同,後者是客觀存在、有客觀標準的。
目前國內市場上基因檢測公司層出不窮,為了區別於其他競爭公司,每家公司的全基因套餐包含的基因數量都不同,那麽必然帶來TMB閾值不統一的問題,各家公司都有各自的劃分標準, 因此可能存在同一個病人經不同公司檢測,一家判定TMB-H另一家則不是的尷尬情況,從而影響對於免疫治療收益的預測。
另外目前多數關於TMB的研究基於歐美人群較多, 缺乏中國人群數據,不便建立中國人群統一的TMB閾值, 即便部份公司的檢測Panel與WES金標準一致性高,也暫不推薦作為中國人群統一標準。從這一點出發, 目前國內大多數的TMB-H人群劃分是有些混亂的 。

圖片來源:攝圖網
預測作用存在局限,
TMB-H就等於免疫治療獲益嗎?
2020年,FDA批準「K藥」用於TMB-H(≥10 mut/Mb)的成人與兒童實體瘤患者,很多患者正是透過這條資訊認識了TMB與免疫治療的關系(補充一點,此處TMB閾值劃分是基於FoundationOne CDx,並非通用標準)。
「K藥」的這項適應癥是基於Keynote-158研究的亞組分析結果,有1050例不同癌種的患者是截止日期前至少26周納入研究的,有足夠的觀測隨訪時間,其中有790例檢測計算了TMB值,102例為TMB-H(≥10 mut/Mb),結果表明TMB-H組的ORR為29%,非TMB-H組的ORR僅為6%,TMB-H組的兩年PFS率為22%,而非TMB-H組則為7%,由此可以看到, TMB-H組人群接受免疫治療的有效率相對更高,獲益可能性相對大一些 。
除了Keynote-158以外,還有多項研究發現TMB-H人群可能從免疫治療中獲益,而我們前面已經提到過不同研究、不同檢測Panel計算得到的TMB與其閾值都是不同的,這也就意味著雖然TMB-H人群可能從免疫治療中獲益,但我們卻沒有通用的方式可以找出這部份人群,有可能因為TMB閾值劃定的不同,導致一部份潛在獲益的人群被遺漏,也可能出現一部份獲益較小的人群被納入。
另外,2019年的一項回顧性分析綜合了Keynote-021、Keynote-189以及Keynote-407等研究,分析了TMB對於「K藥+化療」組合的療效預測。研究者選取了PFS及OS(數據來源Keynote-189以及Keynote-407),還有ORR(數據來源Keynote-021),並以TMB≥175 mut/exome為界限劃定閾值來。
結果令人意外,無論TMB高還是低,PFS、OS以及ORR均未表現出顯著差異,換句話說, TMB可能對於「K藥+化療」乃至免疫治療聯合化療這種治療模式的預測價值有限 。

做個簡單歸納,由於檢測Panel的多樣化,導致TMB的計算與閾值劃分不統一,即便TMB-H人群可能從免疫治療中獲益,卻難以真正精準區分潛在獲益人群,並且隨著免疫治療聯合化療模式的普及,TMB的預測作用也在變小甚至可能無法預測。
4
總結
雖然TMB被當成推薦做諸多「全基因」大Panel檢測的理由,也有很多的研究及文獻報道表明TMB可能預測免疫治療的效果,但深入了解後,我們可以看到關於TMB的檢測從樣本類別、閾值劃定以及預測效果上仍存在很多需要討論的,還未形成統一通用規範。

1
組織樣本與血液樣本檢測得到的
結果之間不能直接換算
組織樣本及血液樣本均可用於TMB的檢測,需采用NGS技術做大Panel,兩種樣本之間存在一定相關性且均可用於預測免疫治療的效果,但需要註意的是 組織樣本得到的tTMB與血液樣本檢測得到的bTMB之間並不能直接換算 。
這意味著,我們在實際治療中,可以用血做「全基因」計算TMB,但需要註意並不能簡單的以組織樣本的標準來衡量bTMB的高低,這裏較為考驗檢測所自身的水平。
2
TMB值受基因檢測公司自身演算法
影響較大
衡量TMB高低需要劃定閾值,然而不僅是不同樣本檢測後的閾值不同,檢測Panel內包含的基因數量不同也需要劃定不同的閾值,且目前各Panel劃定的閾值間並不相同。
這就是說各位即便在市場上各家公司的「全基因」檢測得到TMB值,
其高低劃分也只代表該公司自身演算法下的高低,並不能直接套用現有研究中的劃分標準
,那麽自然也不能直接套用現有研究結論去指導免疫治療獲益情況。
3
TMB值預測免疫治療聯合化療方案
作用不明顯
多個研究的結論證明了TMB可用於預測免疫治療的獲益,但
僅限於單獨使用免疫治療的情況
,當采用免疫治療聯合化療的方案時,TMB的預測作用則並不顯著。由於真實治療中免疫治療的有效率比較尷尬,目前很多病友在選擇治療方案時都會直接考慮免疫治療聯合化療,也讓TMB對於這部份病友的價值下降很多。
綜上所述,TMB雖然作為免疫治療的生物標誌物已經得到專家及指南的認可,但在實際使用中仍面臨諸多潛在問題, 缺乏統一的規範使得實際中各檢測公司TMB的參考價值下降 ,加之做TMB檢測需選擇「全基因」大Panel價格不菲, 各位在選擇時可根據自身情況考慮,不必強求 。

參考文獻
[1].Koeppel, Florence, et al. "Whole exome sequencing for determination of tumor mutation load in liquid biopsy from advanced cancer patients." PloS one 12.11 (2017): e0188174.
[2].Araujo, D. V., et al. "Blood-based TMB (bTMB) correlates with tissue-based TMB (tTMB) in a multi-cancer phase I IO cohort." Annals of Oncology 30 (2019): v512.
[3].Park, Jewel, et al. "Exploring real-world concordance of tissue mutation burden (TMB) from blood and tissue in patients with solid tumors." medRxiv (2021): 2021-05.











