本文最精彩的部分:

摘要
心肌损伤是手术患者在接受非心脏手术后常见的并发症,其发生与围手术期死亡率密切相关。虽然术中麻醉相关死亡的情况极为罕见,但 约有1%接受非心脏手术的患者在术后30天内死亡 。鉴于每年进行的手术数量,手术后死亡已成为美国第二大死亡原因。 非心脏手术后心肌损伤( MINS )被定义为术后 30 天内肌钙蛋白浓度升高 ,尽管通常没有症状,但MINS患者会遭受心肌损伤,并在术后30天内面临10%的死亡风险,且在术后第一年持续存在过高的死亡风险。
许多导致MINS发生的因素是不可改变的,例如先前存在的冠状动脉疾病。目前仍缺乏预防措施、系统的监测方法和治疗标准,但许多因素是可以改变的,在临床实践中应予以考虑:如血流动力学控制的重要性、充足的氧气供应、代谢稳态、围手术期药物的使用(如他汀类药物、抗抑郁药物、抗凝药、β-受体阻滞剂或抗炎剂),以及有关选择麻醉镇静剂和镇痛剂的一些证据。
此外,随着年龄和手术患者合并症人群增加,迫切需要识别有MINS风险的患者并制定预防和治疗策略。在这篇综述中,我们将概述当前的筛查标准和围手术期有前景的预防方案,并解决需要进一步调查的知识差距。
关键词:
心肌损伤,术后心脏并发症,术后死亡率,术后并发症
1.前言
在过去的几十年里,麻醉相关的术中死亡率持续下降,最近的报道显示为0.00082%。然而, 重大非心脏手术后30天内的术后死亡率约为1%,1年后的死亡率约为5%。 每年全球有超过3.12亿的患者接受手术,其中重大非心脏手术后30天的死亡率是美国第二大死因。许多死亡原因与心血管并发症有关。
为了评估围手术期心血管并发症的患者比例,一项名为VISION的前瞻性队列研究招募了15133名年龄≥45岁且接受重大非心脏手术的患者。该研究要求术后前3天必须每日进行心肌肌钙蛋白(cTn)监测。结果显示约12%的患者心脏肌钙蛋白T(cTnT)值升高至20ng/l以上,并且与30天死亡率增加相关。在cTnT峰值升高介于30至290ng/l之间的患者中,死亡率为9%,而在cTn升高>300ng/l的患者中,死亡率接近17%。
在一项使用当代高敏肌钙蛋白(hsTn)检测的大型前瞻性研究中,MINS患病率更高,并且仍然与术后死亡率相关。据随后的荟萃分析显示, 死亡风险的增加不仅在短期内持续存在,而且在术后1年后仍然存在。 在VISION队列的二次分析中,只有16%cTn值升高的患者报告有胸痛,这是非手术环境下心肌梗塞(MI)的主要症状。58%的患者不符合定义MI的诊断标准(存在缺血症状、缺血性心电图变化或存活心肌丧失的影像学证据),因此可能会被遗漏。此外,如果没有常规cTn监测,许多并发症可能会被忽视。
因此,一种新的综合征——「非心脏手术后心肌损伤——MINS」被提出。这一发现对于评估患者的手术风险、改善患者预后以及指导临床实践具有重要意义。
1.1. MI 和 MINS 的定义
心肌梗死(MI)被定义为缺血引起的心肌梗塞,伴有缺血症状、新的缺血性改变或心电图上的病理性Q波、超声心动图检测到的新的室壁运动异常,或冠状动脉内成像或尸检检测到的冠状动脉血栓。 (表1)MI可以根据具有临床和预后意义的缺血机制的病理学差异进行分类: 1 型 MI : 由动脉粥样硬化血栓性冠状动脉疾病( CAD )引起的 MI 。 相反, 2 型 MI: 是在没有不稳定动脉粥样硬化斑块的情况下, 机体 心肌氧供需 失调 引起的 。
非心脏手术后心肌损伤 (MINS) 是指可能由缺血引起的急性心肌损伤,有或没有临床体征或症状,通过术后 30 天内 cTn 水平升高超过第 99 个百分位来诊断。 (表 1)MINS 的病理生理学尚不清楚,尽管它可能与MI有共同的病理生理学基础。炎症激活和手术应激反应可能导致先前存在的动脉粥样硬化斑块发生破坏,随后导致血栓性冠状动脉闭塞和肌钙蛋白释放。另外,许多 MINS 患者在稳定 CAD 的情况下心肌氧供需不匹配,这是由围手术期心脏、呼吸、血液和代谢生理学的变化引起的。 事实上,在大多数情况下,MINS可能是非缺血性的,例如由于围手术期急性失代偿性心力衰竭患者的心室牵张所致。
表 1. 心肌梗塞和非心脏手术后心肌损伤 (MINS) 的定义
|
心肌梗塞 |
非心脏手术后心肌损伤 (MINS) |
|
cTn 浓度上升和/或下降,至少有一个值高于第 99 个百分位 |
至少有一项术后 cTn 浓度超过第 99 个百分位数 * |
|
and |
With/without |
|
任何临床相关的症状 |
任何临床相关的症状 |
|
胸痛 |
手术后30天内 |
|
呼吸短促 |
|
|
心电图出现新的 ST 段抬高或 Q 波 |
|
|
局部室壁运动异常 |
|
|
心肌梗塞的第四个通用定义 |
非心脏手术后心肌损伤患者的诊断和治疗:美国心脏协会的科学声明 |
*对于第四代cTnT检测(采用Roche的Elecsys TnT检测法),其结果应大于或等于30ng/L。对于hsTnT检测(采用Roche的Elecsys hsTnT检测法),其结果应在20至65ng/L之间,且绝对变化应大于或等于5ng/L,或者结果大于或等于65 ng/L。对于hs-cTnI检测(采用Abbot实验室的检测法),其结果应大于或等于60 ng/L。
1.2. 肌钙蛋白测定及临界值
肌钙蛋白是由心肌细胞产生的细胞质调节蛋白,它由三个亚基组成,分别是cTnC、cTnI和cTnT。其中,cTnI和cTnT在临床实践中被常规用于检测心肌损伤。 高敏肌钙蛋白T/I(hsTnT/I)是目前检测心肌损伤最准确、最灵敏的诊断工具。当肌钙蛋白水平高于第99个百分位数参考上限(特定于所用测定,表1)时,被认为是病理性的。 尽管肌钙蛋白对检测MI很敏感,但多种情况可能导致其浓度升高,包括心动过速、低血压、休克、脓毒症、心力衰竭、肺栓塞、胸部钝性创伤、慢性肾病或急性中风。另外,多种生理参数(例如估计的肾小球滤过率、低密度脂蛋白胆固醇、C-反应蛋白)在不同程度上进一步影响肌钙蛋白的测定。因此, 需要连续测量肌钙蛋白来区分急性和慢性升高。 美国心脏协会(AHA)科学声明提供了与预后相关的特定肌钙蛋白阈值来定义MINS:第四代cTnT≥30ng/L(Roche第四代Elecsys TnT测定),hsTnT20至<65ng/L,绝对变化≥5ng/L,或hsTnT≥65ng/L(Roche Elecsyshs TnT测定)或hscTnI≥60ng/L(Abbot实验室)。
1.3流行病学
MINS是一种常见且与死亡率相关的病症。根据前瞻性VISION队列的亚项分析,15065名患者中,有8%(1200人)接受非心脏手术符合MINS的诊断标准。其他研究也表明,这种情况的发生率甚至更高,几乎在接受大手术的患者中达到20%。值得注意的是,84%的MINS患者没有出现临床体征或症状。然而,发生MINS的患者在30天的死亡率、1年的死亡率以及总体死亡率均有所增加。多种与患者相关的因素,例如年龄、肾功能或性别、是否存在心血管疾病(CVD)、糖尿病、阻塞性睡眠呼吸暂停或充血性心力衰竭以及手术环境(紧急或择期)和外科专业(肝脏或肾脏移植可能会根据人群差异改变MINS的发病率。因此,应该充分考虑这些因素,以确保患者的安全和预后。
1.4筛选和预测工具
表2.美国心脏协会 (AHA)、欧洲心脏病学会和加拿大心血管学会关于围手术期心肌肌钙蛋白 (cTn) 监测的指南(主要差异以粗体字母突出显示)。BNP(脑钠肽)、CVD(心血管疾病)、RCRI(修订后的心脏风险指数评分)。
|
|
AHA |
欧洲心脏病协会 |
加拿大心血管协会 |
|
建议 / 指南 |
建议高危患者术后48至72小时内测量cTn |
考虑接受高危或中危非心脏手术的高危患者术前和术后 48 至 72 小时的 hsTn 测量以及 BNP 测量 |
强烈建议高危患者每天进行术后 cTn 测量,持续 48 至 72 小时 |
|
高危患者的定义 |
年龄 ≥ 65 岁 |
存在心血管危险因素(例如年龄≥65岁) |
术前 BNP升高 |
|
|
或年龄 ≥ 45 岁,患有冠状动脉或外周动脉粥样硬化性心血管疾病 |
已知的CVD |
或修正心脏风险指数评分 (RCRI) ≥1 |
|
|
|
存在提示 CVD 的症状 |
或年龄 ≥ 65 岁 |
|
|
|
|
-或45至64岁之间患有严重心血管疾病 |
美国心脏协会(AHA)、欧洲心脏病学会和加拿大心血管学会建议对高危患者进行围术期心肌缺血cTn筛查。(表2)约94%的cTn升高是在术后前2天内检测到的。由于MINS很常见,可以显著改变医疗结局,并且可以通过临床实践的变化进行管理,因此 建议在以下情况下监测cTn:术后前2至3天。 检测方法应该是高度灵敏、特异且经济高效的。
一些术前生物标志物,包括BNP、NT-proBNP、脂蛋白相关磷脂酶 A2、血清 α-羟基丁酸脱氢酶以及肽素,显示出对预测MINS和死亡风险的潜力。修订后的心脏风险指数 (RCRI) 等评分系统与某些人群的MINS风险具有相关性。然而,使用此类评分在识别>45岁患有 MINS12名患者时,仍有可能会漏掉1名患者。来自多个专业的数据整合,例如手术阿普加评分 (SAS)(术中心率、最低MAP和估计失血量),甚至通过整合实验室值、临床体征和生物标志物,可能是实现最佳效果的有前途的工具。在不久的将来进行个性化预测和治疗决策。
2.管理策略
根据定义, 心 肌缺血是MINS的潜在机制(例如机体氧供需失调或动脉粥样硬化血栓形成引起)。 除了患者或手术相关因素(表3)外,多种生理变化可能导致术后cTn升高。 在围手术期,即术前、术中和术后早期,炎症、血流动力学变化(例如血压波动或心动过速)、高凝状态或贫血可能导致心脏不良事件的风险增加。 其中许多是可改变的危险因素,可以作为预防 MINS 的临床目标(见图 1):
表3. 根据 AHA 关于非心脏手术后心肌损伤患者诊断和管理的科学声明改编的 MINS 风险因素。
|
MINS 发生的风险因素 |
|
患者相关的危险因素: |
|
人口统计学特征:年龄增加、性别(男性) |
|
心血管危险因素:吸烟、血脂异常 |
|
心血管合并症:高血压、糖尿病、冠状动脉/外周血管疾病,脑血管疾病 |
|
其他心血管疾病:心房颤动、心力衰竭 |
|
其他合并症:未经治疗的严重阻塞性睡眠呼吸暂停、慢性肾功能不全 (eGFR <60 ml⋅min−1⋅1.73 m−2) |
|
相关风险指数及术前检查结果: |
|
修订后的心脏风险指数评分 |
|
STOP-Bang 风险评分 |
|
随机血糖浓度、利钠肽浓度、中性粒细胞与淋巴细胞比率 > 4、网状血小板浓度、运动后心率恢复、心肌灌注测试的可逆性 |
|
功能能力:Duke活动状态指数得分 |
|
手术相关的危险因素: |
|
紧急大手术 |
|
周围血管或主动脉和大血管手术 |
|
需要大量液体输入或需要输血的长时间手术 |
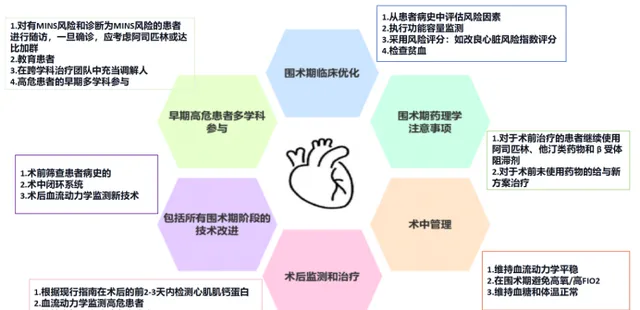 图
1.
目前管理有
MINS
风险的患者的围手术期注意事项
图
1.
目前管理有
MINS
风险的患者的围手术期注意事项
2.1.血流动力学管理
2.1.1.低血压
术中全身性低血 压会降低器官灌 注,并与术后器官损伤、MINS和死亡率独立相关。 即使只是短暂的全身性低血压,也可能产生巨大的影响。 例如,MINS与基线相比变化30%或平均动脉压(MAP)小于65mmHg时,负相关关系明显。当考虑到低血压的持续时间时,这种影响会加剧, 即使是几分钟的MAP为55mmHg,也可能会损害健康患者和慢性高血压患者的心脏供应。 目前,对于普遍的血压阈值尚未达成共识,因为三项随机对照试验(RCT)的结果难以解释。INPRESS试验研究了298名高危患者,报告称, 如果收缩压维持在>80mmHg,风险可降低约25% , 而基线则为±10%。Wanner等人将458名高危患者随机分为MAP≥60mmHg与MAP≥75mmHg,POISE3将7500名患者随机分为避免低血压(目标MAP≥80mmHg)与避免高血压(目标MAP≥60mmHg)术中策略,但每项试验都报告称,严格控制血压并没有带来任何好处。由于缺乏关于影响程度的详细报告,对这两项研究结果的解释变得复杂而难以理解。因此,目前几乎没有试验证据支持任何特定的伤害阈值。观察分析中的伤害阈值似乎大致为MAP<65毫米汞柱或收缩压<90毫米汞柱维持约15分钟。
在麻醉诱导和手术切皮期间,大约三分之一的低血压事件会发生,这凸显了在该时期仔细选择合适的麻醉诱导药物以及针对个体患者适合剂量的重要性,同时必须严格且持续地监测血压。此外, 术后低血压的情况较为常见,且难以被及时发现,尤其是在门诊手术及普通病房中,血压监测往往被忽视。 有数据显示,几乎四分之一的外科病房患者会经历未被发现的低血压发作,平均动脉压低于70 mmHg,且持续时间约为半小时。由于术后48小时内发生MINS的风险最高,因此术后早期是优化监测的重要时期。综上所述,保持整个围手术期的血压稳定是麻醉优化的重要目标。
2.1.2.心动过速
心动过速会减少冠状动脉的舒张期充盈,从而减少心肌灌注,这可能会导致心肌氧供需失调,这是MINS最可能的病理基础。几项研究报告了心动过速的严重程度和持续时间作为 MINS 和死亡的关键危险因素的重要性,特别是当低血压同时存在时。评估MINS和死亡率与术中心动过速评分的综合严重程度和持续时间之间的关系(通过使用心率上方的面积)的大型队列研究中存在相互矛盾的数据,导致缺乏明确的建议关于术中控制心率。在术后期间,长时间的心动过速可能会促进 MINS 的发展。例如,可以通过整个围手术期的综合疼痛管理策略来减轻这种风险。
主要信息:
1. 血压管理的危害阈值似乎大致为 MAP < 65 mmHg 收缩压 < 90 mmHg 维持约 15 分钟。
2. 三分之一的低血压发作发生在麻醉诱导和手术切开之间。
3. 心动过速可能会增加发生 MINS 的风险,有心脏风险的患者应避免心动过速,但危害阈值仍不清楚。
2.2氧供
2.2.1.围手术期贫血
血液的携氧能力主要取决于血红蛋白的水平,血红蛋白是主要的氧输送介质。贫血患者的健康红细胞数量减少,因此氧供应受损,可能导致心肌梗死。最近有报道称, 术前血红蛋白水平低于12.2g/dl与MINS风险升高相关,而与MINS相比,中度至重度贫血(血红蛋白<11g/dl)与MINS的相关性更显着 。轻度贫血,轻度贫血的发生率为18.6%,中度至重度贫血的发生率为28.6%。术后情况下,贫血与MINS发生率也有关联,其中血红蛋白值<11g/dl与较高的MINS发生率相关。另一项包括POISE-2、ENIGMA-II、VISION和BALANCED研究报告称,术后血红蛋白低至8g/dl的患者发生率高达9%。 当血红蛋白值<11g/dl时,血红蛋白每减少1g/dl,发生心肌梗死、不稳定心绞痛或死亡的几率就会增加1.46倍 (95%置信区间:1.37-1.56;P<0.001)。然而,更严格的输血策略与宽松的输血策略的比较仍然存在争议,并且需要进行大规模的前瞻性试验,因为输血毕竟可能会对心脏功能产生负面影响。
2.2.2.术中高氧
吸入氧浓度增高,可以增加细胞氧浓度,这种机制可能通过吞噬作用期间的「呼吸爆发」介导中性粒细胞的氧化杀伤作用,从而降低手术部位感染的一小部分发生率。然而,一项涵盖了1386名患者的回顾性分析报告指出,高氧血症与MI、急性冠状动脉综合征以及死亡风险增加之间存在一定的关联。另外,在两项分别纳入260名和600名手术患者的随机对照试验中,高氧血症与手术后3天内心肌损伤或NT-proBNP释放风险增加并无确切关联。此外,对1617名手术患者进行的回顾性分析也报告称,高氧血症与MINS之间并未发现明确关联。总之,虽然数据存在一些矛盾,但高氧不太可能显著增加MINS的风险。
2.3.代谢管理
2.3.1.体温
低温下的肾上腺素能和代谢反应可能会干扰心肌的氧供需平衡,从而引发心肌缺血。 1997年的一项实验将患者随机分组,接受额外的术中加温或不加温,实验结果显示, 保持正常体温可以降低心脏骤停、心肌梗死或不稳定心绞痛的发生率。 最近,PROTECT(非心脏手术期间积极的术中加温与常规体温管理)试验发现,积极加温至37°C的目标核心温度并不会增加非致命性心脏并发症(心脏骤停、心肌损伤或死亡)的发生率,相比之下,维持常规体温管理在35.5℃的目标则无此效果。因此, 手术期间应保持机体核心温度高于35.5°C 。
2.3.2.血糖控制
围手术期高血糖可能引发炎症性生理变化,并导致心血管发病率上升。 当血糖水平升高至超过180mg/dl时,已证明与围手术期心肌损伤(MINS)存在关联。 通过术前使用葡萄糖-胰岛素-钾进行血糖控制,对心脏手术患者术后发生心肌梗死(MI)具有预防作用。 在患有冠心病(CAD)和运动诱发的缺血症状的患者中,运动前给予葡萄糖-胰岛素-钾可改善运动耐量测试及超声心动图显示的缺血严重程度,优化心肌灌注不足的可逆性,从而促进再灌注恢复。 这种心脏保护作用可能对接受非心脏手术的高风险MINS患者产生积极影响。然而,目前尚缺乏评估非糖尿病患者接受手术后的这种影响的研究,因此亟需开展相关研究。
2.3.3.远程缺血预处理
需要在预期的心肌缺血损伤之前,对非心脏的外周组织(例如手臂)施加短暂的缺血。理论上,这样可以激发体液反应,从而预防心肌缺血再灌注损伤(MINS)。虽然动物模型显示此方法前景广阔,但两项随机分配人类进行远程缺血预处理与常规护理的试验却产生了不同的结果。其中一项较大规模的研究,即择期血管手术前心脏远程缺血预处理 (CRIPES) 研究,纳入了201名患者,结果显示各组之间的发生率没有差异。因此,根据目前可用的证据,我们不推荐使用远程缺血预处理来降低MINS的发生率。
主要信息:
1.术前和术后贫血与 MINS 发生率较高相关,且血红蛋白值 < 11 g/dl具有分级模式。因此,鼓励心脏病风险较高的患者术前治疗贫血。
2.补充氧气确实会稍微降低手术部位感染的风险,但不会增加包括 MINS 在内的心血管并发症的风险。
3.整个围手术期应保持体温正常(核心体温> 35.5°C)和血糖正常(血糖≤180 mg/dl)。
2.4.药物
2.4.1.降脂药:他汀类药物
鉴于MINS与动脉粥样硬化性心血管疾病之间的紧密联系,他汀类药物被认为对患有MINS或具有患MINS风险的患者可能有益。然而,2016年的一项试验中,虽然招募了648名未接受过他汀类药物的患者,并按随机分配的方式在手术后18小时内接受了大剂量的阿托伐他汀,但该药物并未表现出减少MINS或MI的心脏保护作用。尽管该研究参与人数较少,但这一结果提示,在 手术前以较长时间间隔施用他汀类药物的负荷剂量可能会有更大的益处。 同时,考虑到MI的常见病理生理学途径,MINS患者术后开始使用他汀类药物可能有助于减少进一步的并发症。观察性研究显示,诊断为MINS的患者出院时服用他汀类药物可降低一年死亡率。然而,这项研究存在潜在的无法测量的混杂因素风险,例如大多数出院后服用他汀类药物的患者在术前已经服用了他汀类药物,并且他汀类药物组死亡率的降低主要是由于非心血管死亡。因此,观察到的效果可能是由于更好的整体药物治疗。目前仍缺乏他汀类药物在外科手术中的大型多中心试验,因此我们缺乏证据支持术前服用他汀类药物以保护患者免受MINS的影响。尽管如此,他汀类药物在围手术期仍具有许多潜在益处。
2.4.2.抗血栓药:达比加群和阿司匹林
在大型的POISE-2RCT试验中,研究者发现 术前服用阿司匹林以及术后30天的疗程并未降低发生 MI 的风险,反而增加了出血的风险。 然而,在POISE-2的亚组分析中, 对于患有冠心病(CAD)以及既往接受过冠状动脉支架治疗的患者,阿司匹林的使用与心血管事件的显著减少有关。 另外,在一项针对接受膝关节、髋关节或脊柱手术且有阿司匹林使用史的冠心病患者的观察性研究中,围手术期继续服用阿司匹林与术后心血管不良事件发生率降低相关(阿司匹林治疗下发生心肌损伤的比例为13.5% vs.未经治疗的比例为19.3%,P=0.05)。同时,在出血风险方面,阿司匹林也表现出了一定的安全性(阿司匹林治疗下的红细胞输注率为37.2%,未经治疗的比例为44.2%,P<0.001)。然而, 根据现有的证据,我们不建议将阿司匹林作为围手术期MINS一级预防的常规治疗。但在高危患者中,可以继续使用阿司匹林, 并且应考虑用于以下情况:治疗确诊为 MINS 的患者。
一旦MINS诊断成立,达比加群是唯一经过研究可以减少长期血管事件的抗血栓药物。 每天服用两次110mg的达比加群可以减少心血管并发症,但出血风险略有增加。然而,由于MANAGE试验提前终止,达比加群在当代临床实践中并不被常规使用。这一发现尚未在第二次随机对照试验中得到证实。
2.4.3.心率调节剂:β受体阻滞剂
根据之前所述,心动过速被视为MINS的一个风险因素。一项评估围手术期使用β受体阻滞剂(美托洛尔)的研究试图显示其可能的有益效果。然而,研究结果显示, 在术前和术后6小时以及术后30天口服缓释美托洛尔,会导致死亡风险和中风发病率增加。在预防MINS和MI方面,这些风险超过了心动过速抑制带来的益处。 因此,β-受体阻滞剂不能作为高危患者的常规治疗。对于长期使用者来说,在围手术期继续使用β受体阻滞剂仍然是一种有效的方法。
2.4.4.麻醉类型和麻醉药物
在评估MINS的研究中,大多数研究并未明确区分麻醉类型。显然,低血压是MINS的最大危险因素之一,与麻醉类型以及用于诱导和维持麻醉的麻醉药物高度相关。有趣的是,有报道称区域麻醉患者中MINS的发生率较高。然而,尚不清楚这一发现是否仅归因于区域麻醉,与接受手术的患者相比,区域麻醉组中合并症患者数量较多。
关于全身麻醉,目前对最常见静脉麻醉剂丙泊酚和吸入七氟烷的研究并未发现MINS发生率存在任何差异,在经改良的RCRI确定的高心血管风险患者中也没有发现任何差异,适用于患有CAD的患者或特定老年(65-80岁)患有CAD的特定患者群体。因此,尽管先前描述了七氟醚通过心肌预处理具有心脏保护作用,但这种有利的结果尚未针对MINS进行科学验证。尽管如此,七氟醚的使用改善了接受全身麻醉的65至80岁患者群体的血流动力学稳定性,因此在某些情况下它可能仍然是有益的。
另外,心脏保护作用归因于右旋美托咪定,一种在术中用作镇静剂或辅助镇痛剂的药物。目前的证据对其益处是相互矛盾的。一些研究报告显示,血流动力学稳定性更好,心动过速发作率更低,同时缩短了住院时间。其他研究者发现整个围手术期心动过缓和低血压事件有所增加。右美托咪定的另一个好处可能是其假定的抗炎特性,这可能有助于减轻与围手术期促炎状态相关的MINS风险。 总体而言,术中使用右美托咪定不太可能减少心脏并发症、心肌梗死、房性心律失常、术后谵妄或死亡率。 然而,一些作者报告了稍好的结果(全因死亡率、非致命性心梗和心肌缺血),并强调了反对右美托咪定心脏保护作用的结论是从右美托咪定主要用于以下领域的研究中得出的:术前或术中情况,而不是术后脆弱阶段,在该阶段,长时间的心动过速仍可能促进MINS的发展。需要进一步研究来阐明不同类型的麻醉、镇静和辅助镇痛药物对一般和特定患者群体中 MINS 的影响。
2.4.5.辅助吸入麻醉剂:术中 N2O
一氧化二氮 (N2O) 可作为呼吸和血流动力学稳定的辅助吸入麻醉剂和镇痛剂。 术中 N2O 暴露会增加心血管短期和长期发病率甚至死亡率。 N2O会使蛋氨酸合成酶失活,导致术后至少一周持续维生素B缺乏和高同型半胱氨酸血症。维生素B缺乏可能导致内皮功能障碍。ENIGMA 试验将2050名进行持续>2 小时的非心脏手术的手术患者随机分为 N2O 麻醉或无 N2O 麻醉。中位随访时间为 3.5 年(范围0 至 5.7)年。N2O 不会增加死亡风险[OR=0.98(95% 置信区间:0.80至1.20;P=0.82)],也不会增加中风风险[调整后OR:1.01(95%CI:0.55至1.87;P=0.97)]。然而,N2O 患者心肌梗死的调整后OR轻微升高至1.59(95%CI:1.01至 2.51;P = 0.04)。
有趣的是,术后 6-12 小时和术后前 3 天的 cTnT 监测没有提供心肌损伤任何短期的证据。因此,目前没有证据表明 N2O 对 MINS 的发展有恶化作用,但其使用受到其他麻醉相关有害作用的限制,例如增加术后恶心和呕吐的风险。
2.4.6.抗炎剂
(维生素C、N-乙酰半胱氨酸、秋水仙碱)
目前正在研究 MINS 的许多替代预防和治疗方案: 术前应用抗炎药维生素C和N-乙酰半胱氨酸不会影响接受重大非心脏手术的患者的心血管风险。不应将其用作MINS的预防剂。 另外,秋水仙碱是一种主要用于治疗和预防痛风发作的药物,以其抗炎特性而闻名,并已用于治疗心包炎和CAD患者。在手术患者中,秋水仙碱主要在心脏手术的围手术期进行研究。有一些证据表明,在接受体外循环冠状动脉旁路移植术的患者中,围手术期给予秋水仙碱可以降低hsTnT和CK-MB,并且在术前接受经皮冠状动脉介入治疗的患者中,hsTnI水平的升高显着降低秋水仙碱治疗与未接受术前治疗的患者进行比较。虽然秋水仙碱在概念上对接受非心脏手术的患者很有吸引力,但目前没有足够的数据推荐其用于预防 MINS。进一步正在进行的随机对照试验的结果,例如COP-AF(秋水仙碱用于预防胸外科患者围手术期心房颤动;NCT03310125)、COPMAN(秋水仙碱预防非心脏手术后心肌损伤试点研究;NCT04139655)和 POPCORN(围手术期秋水仙碱减少负面事件;NCT NCT05618353)应在不久的将来指导有关围手术期使用秋水仙碱的决策。
主要信息:
1.目前,尚无证据表明术前他汀类药物、抗血栓药物、抗凝或β受体阻滞药物的使用、某种类型麻醉或麻醉剂的选择、术中N2O或N2O及抗炎药物的应用具有有益效果, 可降低 MINS风险。
2.高危患者术前应继续服用阿司匹林
3.长期治疗的患者应在术前继续使用β受体阻滞剂
4.β受体阻滞剂和阿司匹林均不应常规使用以预防围手术期 MINS
5.七氟醚可改善血流动力学稳定性,对于特别虚弱的老年人群仍可考虑使用
6.一旦做出 MINS 诊断,应考虑阿司匹林和达比加群,同时记住,通过使用达比加群观
3. 麻醉医师的未来前景和作用
在未来的临床实践中,通过整合大数据集,包括临床数据、人口统计学和生物标志物,我们将能够实现更为个性化的预测评分,这可能会在最佳筛查和高端治疗方面树立新的里程碑。现代技术简化术前信息获取过程,并在围手术期早期自动识别风险因素,这将有助于我们主动接触有发生MINS风险的患者。同时, 个性化的术中和术后治疗计划对于MINS的管理具有特别重要的意义。 在术中环境,技术进步可以帮助临床医生预测低血压事件或在麻醉期间提供最佳的血流动力学控制。术后安全性技术应通过使用创新技术进行更密切的监测,例如针对普通病房患者的移动警报系统或更容易跟踪血流动力学变化的现代技术以及系统计划的后续行动以实现最佳二级预防。然而,目前关于MINS最佳管理的数据仍然有限,围手术期cTn监测并未得到广泛实施。为了改变这一现状,我们需要新的医学疗法来预防和治疗MINS。 治疗指南的制定和研究的推广应基于跨学科合作,并包括一系列护理和多维方法。麻醉提供者作为围手术期专家,应在多学科环境中充当调解人,保护患者安全并提供高端护理。
围手术期医生可以推广预康复计划或个性化的术前工具来筛查虚弱,使用先进的监测和技术工具来协助术中的血流动力学管理,最后在术后提供高标准的护理和监测,例如通过远程监测外科病房、术后监护室或重症监护室。
4.结论
MINS 是一种常见的心血管事件,与非心脏手术后的短期和长期死亡率密切相关。尽管围手术期常规 cTn 监测具有成本效益并且得到了一些专家小组的推荐,但许多中心并未进行常规围手术期 cTn 监测。麻醉医师需要认识到识别有 MINS 风险的患者的重要性。 至关重要的是要认识到不可改变和优化可改变的术前风险,提供安全且血流动力学稳定的术中护理,并至少在高风险患者和患者中至少在术后前 2 至 3 天内通过 cTn 测量进行系统性术后随访。 与 MINS 一起实施心血管治疗以进行二级预防,包括他汀类药物和抗血栓药物。强烈鼓励早期跨学科参与、关于 MINS 相关风险的患者教育以及实施生活方式改变的建议,以对这一致命的围手术期实体产生真正的影响。 麻醉医师可以在心脏病专家、外科医生、护士和患者等跨学科网络中充当围手术期调解人,以期为所有患者提供最佳结果。
本文译者:曹香华
文献来源: Perioperative strategies to reduce risk of myocardial injury after non-cardiac surgery (MINS): A narrative review . Journal of Clinical Anesthesia 87 (2023) 111106.
有奖投稿
1.欢迎同行原创投稿,稿酬200元/篇
2.投稿>3篇以上,优先加入新青年高级技术群
3.投稿10篇以上成为新青年特约撰稿专家,获得新青年终身VIP

▼ 点击「











