1
. 静息(Quiescence)
静息是限制naive T细胞对tonic信号(自身抗原等)产生反应,此时细胞处于G0期,维持小细胞形态,处于基础代谢状态,不会向效应表型分化。
意义:
防止Naive T细胞扩增,使之维持在一定数量范围之内。
克隆选择:确保大部分结合特定抗原的T细胞repertoire受到限制,限制高亲和力的克隆扩增。
静息的阈值是固定的还是一个动态范围,仍然不是很清楚。但是对阈值的精准调节,有助于发挥适度的抗感染或者抗肿瘤免疫反应,但是不引起自身免疫性疾病。
TGF-β和TOB1是重要的静息调控因子,他们通过SMAD通路下调IL-2的产生及抑制T细胞活化。TOB1是APRO基因家族的成员,编码抗增殖的蛋白质(包括BTG1和BTG2)。
转录因子RUNX1调控KLF2,FOXO1,FOXP1,他们都是静息T细胞的关键转录因子。
TSC1 和 TSC2通过抑制mTORC1活性,下调静息T细胞的代谢。
2. 忽视(Ignorance)
忽视是Naive T细胞阶段的另外一种外周耐受的模式。
尽管特定的自我抗原存在,自反应T细胞不能激活和引起自身免疫性疾病,这些T细胞仍处于Naive的状态。
内在机制
:抗原和TCR亲和力过低,不能引起T细胞反应。
外在的机制
:包括抗原密度低或者解剖位置限制了抗原识别的发生,导致T细胞无法激活。
忽视不是T细胞功能不全
,在特定刺激(如病毒感染,促炎症因子等)情况下,T细胞会克服忽视状态,成为效应细胞。
静息和忽视的区别:
静息是
所有Naive T细胞的
通用标志,
与抗原特异性无关
。
忽视是
避免激活
自身反应性T细胞,
可能是进化上依旧不完美的中枢耐受的补充。
3. 无能(Anergy)
Naive T细胞的TCR结合抗原,但是低反应或者无反应。它作为T细胞启动过程中的早期检查点,以防止在T细胞进入效应阶段前出现潜在的T细胞致病性。
分子机制是
缺乏共刺激分子
,不能激活NFAT1和AP1,不引起细胞分化和效应功能,反而通过RAS-MAPK通路抑制AP1入核。无能的特征是IL-2,IFN-γ,TNF-α等因子减少,mTORC1活性被抑制,代谢被抑制。此外,无能细胞高表达CD73,FR4,LAG3等抑制性受体,但是不同于Treg,它不表达FoXP3.
和静息细胞不同,无能细胞的细胞周期
停滞在G1进入S期
,而静息细胞停滞在G0期。
无能是一个长时间的状态,但是可以被反复抗原暴露,以及加入IL-2等细胞因子状态下被逆转。
4. 耗竭(Exhaustion)
耗竭主要因素是慢性感染或者肿瘤,产生的持续抗原暴露,引起的T细胞功能损坏。与无能的区别是,耗竭T细胞不缺少共刺激分子,但是
大量抑制性免疫检查点表达
。更多内容可阅读:T细胞耗竭(Exhaustion)
5. 衰老(Senescence)
衰老是生长和增殖停滞状态。与耗竭的慢性
持续
抗原暴露不同,衰老是TCR接受
反复
刺激或者淋巴细胞老化,引起
端粒损伤
或者
DNA损伤
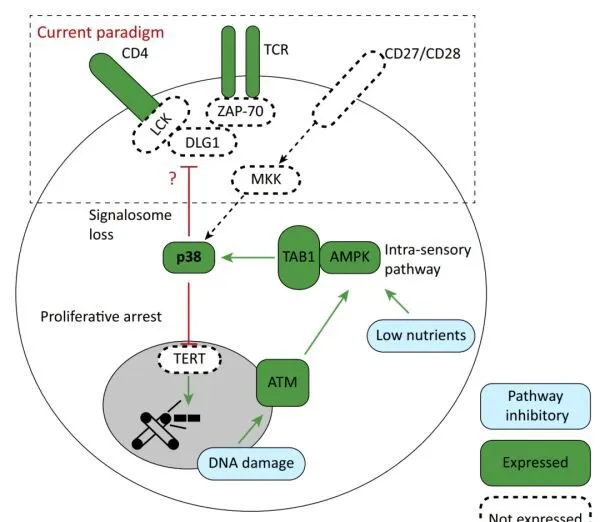
,在遭遇抗原刺激时,T细胞复制能力丢失,多发生在效应或记忆分化阶段。从进化的角度讲,衰老可以避免DNA损伤的T细胞过度增殖,避免形成淋巴瘤。
一些引起端粒损伤的因素(活性氧ROS,电离辐射,生长因子剥夺),影响端粒酶活性,也可以加速淋巴细胞衰老。
缺乏增殖能力的衰老细胞表达CD45RA,KLRG1和CD57,不表达CD27,CD28等共刺激因子。和耗竭细胞不同的是,衰老细胞虽不能增殖,但是
效应功能并不受影响
,可以分泌促炎症因子和炎症抑制因子(
衰老分泌表型
)。
和经典的p38激活不同,此时p38激活时通过细胞内感受器AMPK,通过TAB1激活p38,产生后续功能。
衰老引起对的增殖能力丢失,会引起对疫苗接种的低应答,这也是老年人疫苗接种应答率低的一个因素。
6.外周清除耐受(Peripheral deletional tolerance (death))
在免疫反应结束的阶段(收缩期),通过凋亡清除过多的免疫细胞。
机制:
Bcl-2家族线粒体凋亡途径:促凋亡的BIM和抗凋亡Bcl-2家族分子维持着凋亡平衡,外周清除耐受时促凋亡作用为主。
AICD:活化诱导的细胞死亡(activation- induced cell death,AICD)是清除发挥完功能的效应T细胞的主要机制。FasL-Fas及TRAIL-TRAILR1 TRAILR2凋亡通路为主。
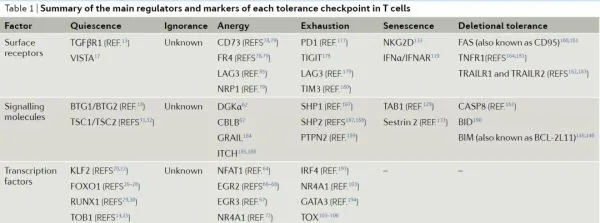
外周耐受的主要调控因子
主要参考文献
Mohamed A. ElTanbouly and Randolph J. Noelle,Rethinking peripheral T cell tolerance: checkpoints across a T cells journey,Nat Rev Immunol . 2020 Oct 19.
Akbar, A. N., Henson, S. M. & Lanna, A. Senescence of T lymphocytes: implications for enhancing human immunity. Trends Immunol. 37, 866–876 (2016).











