膽道惡性腫瘤(biliary tract cancers,BTC)是來源於膽管及膽囊上皮的一組高度異質性惡性腫瘤,具有早期診斷困難、進展迅速、解剖部位復雜等特點。流行病學數據顯示,BTC每年約占全球癌癥相關死亡人數的2%。近年來發病率呈持續上升趨勢,以亞洲國家最為常見。臨床上僅30%~40%的患者在初診時具有根治性手術的機會,且術後復發率高。雖然BTC整體發病率不高,但其惡性程度高,容易復發轉移,且大多數患者在確診時已經處於晚期,導致治療效果和預後極差。
BTC診療現狀
手術切除一直以來都是BTC的根治性治療方法,盡管手術切除可以達到根治的目的,但研究發現大約50%的患者在根治性手術切除之後因復發而影響長期生存。
2017年的一項回顧性研究發現,復發後再次進行手術治療的BTC患者3年及5年生存率明顯高於復發後接受化療或最佳支持治療者(3年生存率分別為38%、5.3%和0,5年生存率分別為19%、5.3%和0,P<0.0001)。
手術是目前BTC唯一可能治愈的方法,但大多數患者在診斷時處於晚期,失去手術機會,而放療在膽系腫瘤中的作用有限,大多數晚期患者均以內科治療為主。多項研究顯示,化療為BTC患者帶來12個月左右的中位OS,為進一步延長患者生存,尋找新的治療手段和方法亦成為BTC亟待解決的問題。
免疫治療推進膽道惡性腫瘤治療新突破
吉西他濱聯合順鉑(GP方案)的化療方案作為晚期BTC的標準一線治療已經超過十年。免疫臨床研究在BTC領域也大放異彩,為晚期BTC患者帶來了新的治療策略。以下是兩項重要的研究結果,為晚期膽道惡性腫瘤患者的一線治療提供了新的方案及健康相關生活品質分析。
一、TOPAZ-1研究
研究背景:
該研究是一項隨機、雙盲、安慰劑對照、全球多中心Ⅲ期臨床試驗⁵, 旨在評估度伐利尤單抗聯合吉西他濱和順鉑(D+GC)對比安慰劑聯合吉西他濱和順鉑(PBO+GC)用於晚期BTC一線治療的療效和安全性。主要終點為OS,關鍵次要終點包括PFS、ORR和安全性。
研究結果:
D+GC組與PBO+GC組的中位OS分別為12.9個月和11.3個月(HR=0.76,95% CI:0.64-0.91),2年OS率分別為23.6%和11.5%。安全性分析中,3-4級不良事件發生率和治療相關不良事件導致任何研究藥物中斷的發生率方面,D+GC組均低於PBO+GC組,分別為60.9%和63.5%、8.9%和11.4%。此外,本研究的亞組分析結果顯示,亞洲人群中度伐利尤單抗聯合吉西他濱和順鉑降低死亡風險28%(HR=0.72,95%CI:0.56-0.94)⁶。
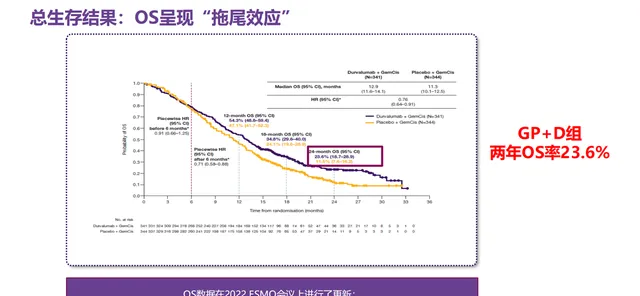
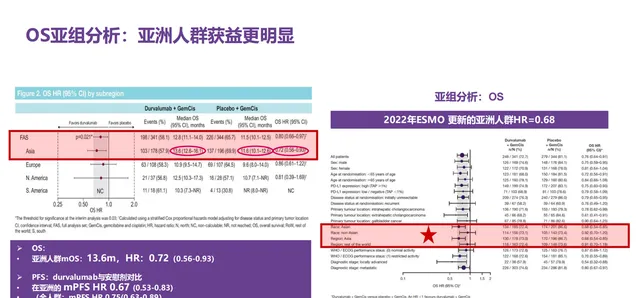
2023年11月7日,基於TOPAZ-1研究成果,中國國家藥品監督管理局批準度伐利尤單抗聯合吉西他濱和順鉑適用於局部晚期或轉移性BTC成人患者的一線治療。
二、KEYNOTE-966研究
研究背景:
該研究是一項國際多中心、隨機、安慰劑對照的一線膽管癌Ⅲ期註冊性臨床研究⁷, 旨在評估帕博利珠單抗對比安慰劑,聯合吉西他濱+順鉑一線治療晚期BTC的療效和安全性。主要終點為OS,次要終點包括PFS、ORR、DoR和安全性。
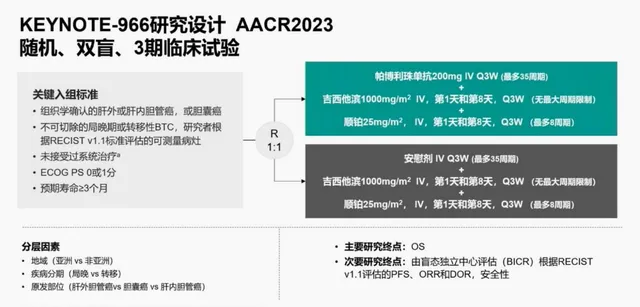
研究結果:
帕博利珠單抗聯合化療和安慰劑聯合化療的中位OS分別為12.7個月(95% CI, 11.5-13.6)和10.9個月(95% CI, 9.9-11.6),死亡風險降低了17%。在試驗預先設定的PFS和ORR最終分析中,與安慰劑聯合化療相比,帕博利珠單抗聯合化療可將疾病進展或死亡風險降低14% (HR=0.86 [95% CI, 0.75-1.00])。安全性方面,兩組間3-4級不良反應發生率無臨床意義差異⁸。
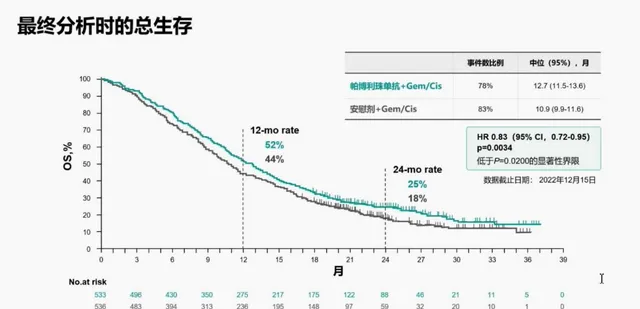
2023年11月1日,美國食品藥品監督管理局(FDA)批準帕博利珠單抗聯合化療(吉西他濱和順鉑)一線治療局部晚期不可切除或轉移性BTC,目前還未獲中國國家藥品監督管理局(NMPA)批準。
2023 CSCO指南更新
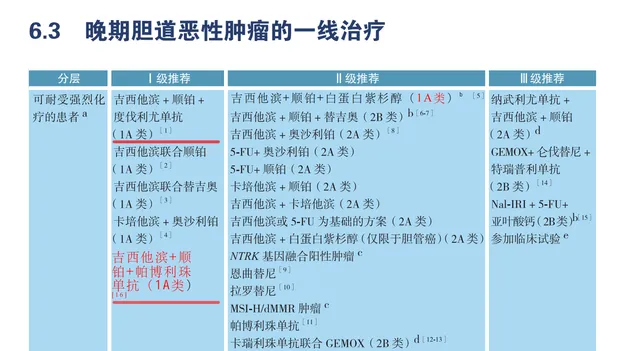
2022 CSCO 度伐利尤單抗+GP方案獲得1A類推薦
2023 CSCO 帕博利珠單抗+GP方案獲得1A類推薦⁹
結語
隨著腫瘤精準診療理念的發展,圍繞BTC的治療逐步轉向靶向、免疫、化療的聯合治療方案。TOPAZ-1和KEYNOTE-966研究為晚期BTC患者的治療提供了新的方案和證據,也希望這些新型治療策略進入臨床實踐後幫助BTC患者獲得更為長久的生存獲益。











