前言
2023年欧洲肿瘤协会亚洲年会(ESMO ASIA)于2023年12月1日-3日在新加坡盛大召开。会议展示了肿瘤学领域的最新研究进展,继续年底的学术热潮。由 江苏省肿瘤医院冯继锋教授 牵头的恒瑞自主研发的抗PD-L1/TGF-β双靶点抗体SHR-1701治疗晚期非小细胞肺癌(NSCLC)的I期研究亮相本次大会(摘要号:511MO)。
冯继锋 教授
主任医师,教授,博士生导师
江苏省肿瘤医院/南京医科大学附属肿瘤医院党委书记
江苏省肿瘤专业质控中心主任
国家卫生健康委合理用药专家委员会委员
中国抗癌协会肿瘤临床化疗专业委员会主委
中国抗癌协会淋巴瘤专委会候任主委
中国医师协会第一、二届肿瘤分会副会长
中国临床肿瘤学会罕见病专委会副主委
江苏省医学会肿瘤化疗与生物治疗分会主任委员
江苏省医师协会肿瘤多学科诊疗专委会主任委员
江苏省预防医学会肿瘤学分会主任委员
江苏省老年医学会肿瘤学分会主任委员
SHR-1701治疗晚期NSCLC患者疗效优异,安全可控
SHR-1701是恒瑞医药自主研发并具有知识产权的抗PD-L1/TGF-β双功能融合蛋白 ,其中PD-L1抗体为阿得贝利单抗,Fc端链接上TGF-β trap,TGF-β除了可以促进肿瘤的进展和转移之外,还能进一步上调抗原递呈细胞(APC)上的PD-L1表达。SHR-1701在抑制PD-1/L1通路基础上,同时抑制TGF-β通路,促进效应性T细胞的活化,增强免疫应答,发挥免疫系统对肿瘤细胞的杀伤作用。
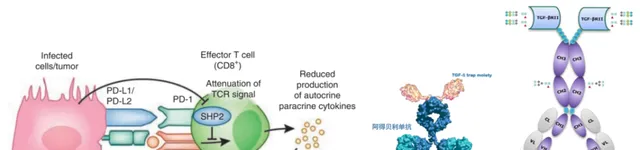
图1 SHR-1701(PD-L1/TGF-β双功能融合蛋白)
SHR-1701 治疗晚期NSCLC I期研究设计和基线特征
该I期研究分为剂量递增和剂量扩展2部分试验,随后在不同肿瘤类型、基因突变或既往经治的多个队列中进行临床扩展研究。本次ESMO ASIA大会中展示了3个NSCLC临床扩展队列的结果。队列1纳入未接受全身化疗,PD-L1 TPS≥1%的患者;队列2纳入既往接受至少一线EGFR TKI标准治疗失败的EGFR敏感突变患者,接受标准治疗耐药或没有有效标准治疗的方案的EGFR突变患者;队列3纳入既往接受抗PD-1/PD-L1单抗治疗后进展且最多接受3线治疗的患者。符合条件的患者给予SHR-1701 30 mg/kg,每3周1次。截至2023年6月6日数据截止,共纳入131名患者(队列1共57例,队列2共41例,队列3共33例)。三个队列的中位随访时间分别为20.3个月、14.3个月和14.8个月。主要终点为ORR (RECIST v1.1)。次要终点为:安全性、MTD和RP2D。

图2 SHR-1701治疗晚期或转移性NSCLC患者研究设计

图3 SHR-1701治疗晚期或转移性NSCLC患者基线特征
疗效优异,SHR-1701在晚期NSCLC患者中显示出优秀的抗肿瘤活性和生存获益
SHR-1701在3个队列中均显示出令人鼓舞的抗肿瘤活性。根据研究者评估,3个队列的ORR分别为36.8%、19.5%和9.1%,DCR分别为66.7%、46.3%、54.5%,CBR分别为40.4%、22.0%和15.2%。截止数据更新时,3个队列的中位DoR分别为19.4个月、5.2个月和未达到。


图4-5 SHR-1701治疗晚期或转移性NSCLC患者ORR和DoR
SHR-1701在晚期或转移性NSCLC患者中同样显示出令人鼓舞的生存获益。截止数据更新时,队列1、队列2和队列3中患者中位PFS分别为5.3个月、1.4个月和2.1个月。中位OS分别为24.2个月、14.4个月和16.1个月。
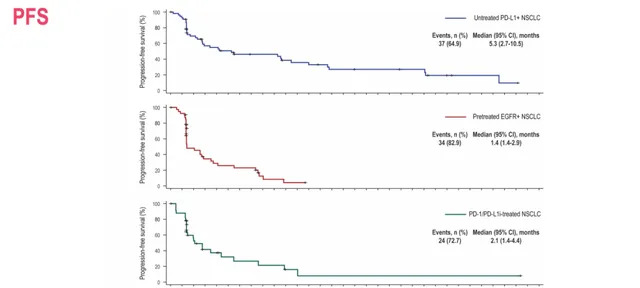

图6-7 SHR-1701治疗晚期或转移性NSCLC患者PFS和OS
安全可控,SHR-1701在晚期或转移性NSCLC患者中显示出可接受的安全性
SHR-1701在晚期或转移性NSCLC患者中显示出可接受的安全性。在3个队列中,分别有84.2%、75.6%和63.6%的患者出现TRAE。在3个队列中,≥3级TRAE的发生率分别为31.6%、17.1%和15.2%。

图8 SHR-1701治疗晚期或转移性NSCLC患者安全性结果
SHR-1701在晚期PD-L1阳性,EGFR TKIs耐药和既往PD-(L)1治疗失败的NSCLC患者均显示出令人鼓舞的抗肿瘤活性和安全性,为初治NSCLC,EGFR TKIs耐药和免疫耐药患者提供了新的治疗思路。作为恒瑞自主研发的双抗抑制剂,SHR-1701多项临床试验也在不断开展中。
卡瑞利珠单抗一线治疗晚期NSCLC,中位总生存超越27个月
恒瑞自主研发的PD-1抑制剂,卡瑞利珠单抗联合化疗一线治疗NSCLC患者实现长生存获益,达到「临床治愈」。
卡瑞利珠单抗联合化疗治疗晚期非鳞和鳞状NSCLC的两项大型III期注册临床研究CameL、CameL-sq研究也取得了PFS和OS的双阳性结果。 中位OS均超越27个月,是目前OS最长且唯一双OS阳性的国产PD-1抑制剂。
CameL研究显示,卡瑞利珠单抗联合化疗一线治疗非鳞NSCLC 患者, mOS达27.1个月 ,与对照组(19.8个月)相比延长了7.3个月,显著延长了总生存期。4年长生存数据也重磅发表于JTO,结果显示 卡瑞利珠单抗联合化疗4年OS率高达37.2%,使超1/3患者生存突破4年。 3年OS率为39.3%,相较4年OS率, 一年的时间OS率仅下降2.1%,意味着这些患者很可能生存突破5年,达到临床治愈。

图9 PFS OS曲线和4年OS率
CameL-sq研究显示,卡瑞利珠单抗联合化疗治疗鳞状NSCLC患者, mOS达27.4个月 ,与化疗组相比,mOS延长了接近1年,死亡风险显著降低43%, 是目前唯一鳞状NSCLC中位OS超越27个月的国产PD-1抑制剂 。3年的OS率高达42.8%,超过2/5患者活过3年,体现了强效PD-1的长拖尾效应,让更多鳞癌患者获得长生存。

图10 PFS OS曲线
卡瑞利珠单抗联合化疗一线治疗非鳞和鳞状NSCLC患者, 是目前唯一取得双OS阳性且mOS最长,均超越27个月的国产PD-1抑制剂 。非鳞癌中,4年OS率37.2%,使超1/3患者生存突破4年。 CameL和CameL-sq相互印证 ,给患者带来 长生存获益,达到「临床治愈」。
参考文献:
1. Jifeng Feng et al. 2023 ESMO ASIA.
2. Zhou C et al. J Thorac Oncol. 2023.
3. Zhou C et al. 2022 ELCC 3MO.
排版:Babel
执行:Babel
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。











