
2024年7月3日,對於阿爾茨海默病(AD)的治療領域而言,是具有裏程碑意義的一天。美國FDA批準了禮來(Eli Lilly and Company)的Kisunla(donanemab)用於治療出現早期癥狀的AD成年人,這一突破性的進展為無數患者和家庭帶來了新的希望。
AD,這個困擾人類健康的難題,一直以來都缺乏有效的治療手段。而此次獲批的Kisunla療法,為AD的治療帶來了全新的思路和可能性。
Kisunla療法的獲批是基於TRAILBLAZER-ALZ 2試驗的出色結果。在2023年的阿爾茨海默病協會國際會議(AAIC)上,禮來公布的試驗數據令人矚目。Donanemab在減緩具有AD早期癥狀患者的認知與功能下降、延緩疾病進展方面表現出了顯著的效果。亞群分析更是揭示了一些關鍵的發現,處於疾病最早階段的受試者從這種療法中獲益更為顯著,其認知與功能下降相較於安慰劑組減緩達60%。同時,75歲以下的患者也顯示出了更大的受益。
在對澱粉樣斑塊的影響方面,donanemab展現出了強大的作用。在18個月的治療期間,所有受試者中,donanemab治療使澱粉樣斑塊平均減少84%,而安慰劑組患者中這一數值僅為1%。這一顯著的差異表明,donanemab能夠有效地清除大腦中的澱粉樣斑塊,為阻止疾病的進展發揮了關鍵作用。當患者達到預定的澱粉樣斑塊清除標準,便能夠停止使用donanemab。其中約一半的受試者在12個月時達到這一閾值,約每10名受試者中有7名在18個月時可達到此閾值。這一特性不僅為患者提供了更靈活的治療選擇,也有望降低治療成本和減少輸液次數。
Donanemab是一款靶向β澱粉樣蛋白(Aβ)的單複制抗體,它能與名為N3pG的澱粉樣蛋白亞型特異性結合。這種特異性的結合使得donanemab能夠精準地與大腦中的澱粉樣斑塊相結合,進而促進其清除。這種靶向治療的策略,為AD的治療開辟了新的途徑。
根據禮來公布於2023年阿爾茨海默病協會國際會議(AAIC)中的數據,donanemab可顯著減緩具有阿爾茨海默病早期癥狀患者的認知與功能下降、延緩疾病進展。 亞群分析顯示,處於疾病最早階段的受試者獲益更為顯著,與安慰劑相比,其認知與功能下降減緩達60%。 亞群分析還顯示, 75歲以下的患者從donanemab中受益更大。 此外,無論患者基線的病理分期為何,donanemab治療皆能顯著降低其澱粉樣斑塊水平。
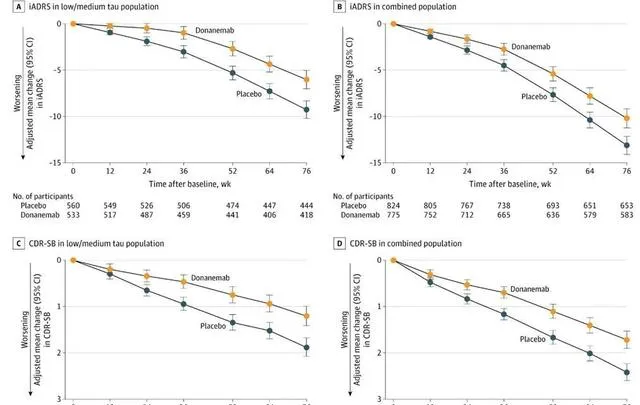
▲試驗患者自基線至76周的iADRS與CDR-SB變化(圖片來源:參考資料[3])
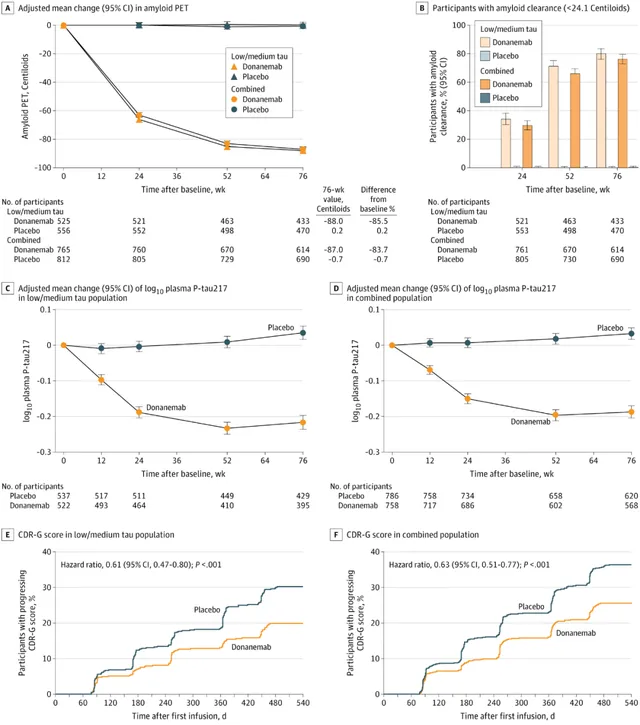
▲試驗患者腦澱粉樣蛋白、血漿磷酸化tau(P-tau 217)和疾病進展風險結果(圖片來源:參考資料[3])
在18個月時,在所有受試者中,donanemab治療使澱粉樣斑塊平均減少84%,而此數值在安慰劑組患者中僅為1%。 當患者達到預定的澱粉樣斑塊清除標準,受試者能夠停止使用donanemab。其中約一半的受試者在12個月時達到這一閾值,而約每10名受試者中有7名在18個月時可達到此閾值。
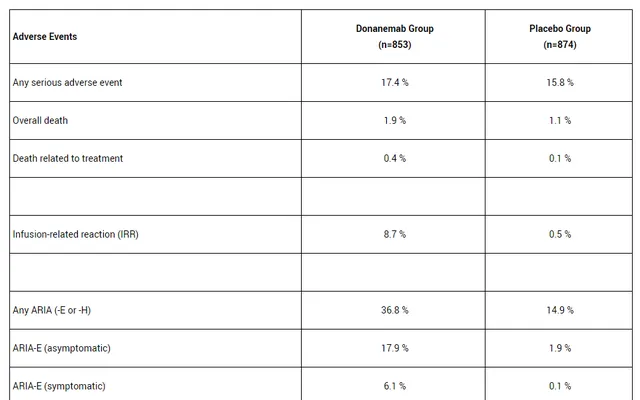
▲試驗安全性結果摘要(圖片來源:參考資料[2])
然而,任何新的療法都並非完美無缺。在安全性方面,TRAILBLAZER-ALZ 2試驗也揭示了一些需要關註的問題。澱粉樣蛋白相關成像異常(ARIA)是與澱粉樣斑塊清除抗體類療法有關的不良反應,在donanemab組中發生率相對較高。具體而言,在donanemab組與安慰劑組中,分別有205位(24.0%;52例有癥狀)與18位元(2.1%;試驗期間0例有癥狀)患者發生ARIA-E。此外,donanemab組與安慰劑組分別有3例與1例死亡被認為與治療相關。盡管存在這些風險,但透過嚴格的監測和管理,有望將不良反應的影響控制在可接受的範圍內。
目前,全球在AD治療的研發領域正處於活躍階段。在針對Aβ靶點的療法中,已有3款單複制抗體療法在美國或日本獲批上市。除了已獲批的療法,還有眾多在研的創新藥物正在努力探索中。預防和/或治療性疫苗、小分子藥物等不同類別的療法都在不斷推進。其中,禮來的兩款單複制抗體療法進展較快,均已進入3期臨床階段。
隨著科學技術的不斷進步和研究的深入,我們對AD的認識也在不斷深化。從過去認為AD是一種不可逆轉的退行性疾病,到如今發現透過靶向澱粉樣斑塊等策略有可能延緩甚至阻止疾病的進展,這是醫學領域的巨大進步。然而,我們也清醒地認識到,AD的治療仍然面臨諸多挑戰。
一方面,雖然Kisunla等療法在清除澱粉樣斑塊方面取得了顯著成效,但對於AD患者認知和功能的改善程度仍有待進一步觀察和評估。澱粉樣斑塊的清除是否能夠真正轉化為患者生活質素的顯著提高,以及這種效果能否長期維持,都是需要長期隨訪和研究的重要問題。
另一方面,AD的發病機制復雜,除了澱粉樣蛋白的沈積,tau蛋白的異常聚集、神經炎癥、氧化應激等多種因素也可能參與其中。因此,單一的靶向治療可能難以完全解決問題,未來可能需要綜合多種治療策略,從多個靶點入手,才能更有效地控制疾病的進展。
此外,藥物的安全性和耐受性也是不容忽視的問題。像ARIA這樣的不良反應雖然在一定程度上可控,但仍可能給患者帶來不適和風險。在藥物研發過程中,如何在保證療效的同時最大程度地降低不良反應的發生,是研發者需要不斷探索和最佳化的方向。
盡管面臨諸多挑戰,但Kisunla的獲批無疑為AD的治療註入了強大的動力。它不僅為患者提供了新的治療選擇,也激勵著科研人員繼續深入研究,探索更多更有效的治療方法。相信在不久的將來,我們能夠在AD的治療領域取得更多突破性的進展,為患者帶來更多的希望和福音。
總之,禮來Kisunla的獲批是AD治療領域的一個重要突破,但這只是漫長征程中的一步。我們期待著未來有更多的創新療法湧現,共同攻克AD這一頑疾,讓更多的患者能夠擺脫疾病的困擾,重享健康和美好的生活。同時,也希望社會各界能夠持續關註AD的研究和治療,為推動這一領域的發展貢獻力量。











