導語
日前,諾和諾德向中國國家藥品監督管理局遞交了一份關於其新型長效生長激素制劑——帕西生長素註射液(Sogroya)的申報檔。
Sogroya的上市申請一經送出,就引起了人們對於這款新藥熱切的期盼,畢竟,這款藥物的療效備受期待,同時患者也無需像以往一樣,每天都要註射生長激素。
然而,帕西生長素註射液的上市申請究竟會迎來怎樣的結果呢?
諾和諾德又為何會鐘意於這款藥物?
與此同時,全球生長激素市場又呈現出什麽樣的態勢?
生長激素缺乏癥的危害。
生長激素缺乏癥(GHD)又被稱為生長激素缺乏癥或者生長激素缺乏性侏儒癥,主要是由於多人下丘腦或者垂體部位發生病變,導致大腦不分泌足夠量的生長激素,從而使個體的身體發育受到極大的影響。
GHD在兒童中尤為常見,發病率為每4000至10000名兒童中有一人。
生長激素在兒童的發育階段發揮著至關重要的作用,它能夠促進兒童的骨骼發育、肌肉生長,並促進身體細胞的代謝和再生,因此,兒童的健康成長離不開生長激素。
如果兒童缺乏生長激素,就會影響他們的生長速度,同時身體機能也會受到更嚴重的影響,也可能導致心理方面的問題,例如社交障礙。
早在1537年,偶然就有醫生發現,粘液性水腫病的患者在各個方面都有較小的身材,一些瘦弱矮小的孩子也在等待著治療,這些人身上都有一個共同點,那就是人體內缺乏生長激素。
1944年,被認為是生長遲緩最有效、最有效的方法,成為世界上第一個被人類用於臨床治療的生長激素制劑。
然而,由於這些名貴的人才短缺,這項工作並沒有進展太快。
20世紀50年代,有一名叫做小Richard的小男孩,僅僅10歲就被診斷為牧羊犬,父母決定不再等傳統治療方法,他們選擇將他送入一家大學進行實驗,以期他能夠透過實驗獲得好運。
最終,小Richard在他們的幫助下獲得了一種療法,而且這種療法是好的,所以小Richard恢復了正常身高。
盡管GrowthHormone是有效的,但由於名貴而短缺,許多患者仍未得到有效治療,因此臨床僅占25%至50%之間
20世紀70年代末80年代初,由於可重組DNA技術的發展,各種重組生長激素藥物應運而生。
1985年11月14日,基因重組人胰島素被批準為美國第一個基因重組產品,第一個人胰島素是1978年制成的。
經過FDA批準後,Genentech公司於1985年開始生產。
1986年,「人胰島素」成為第一個由中國企業研發、生產和出口的原料藥。
90年代初,中國開始研發出口重組人生長激素產品,並以這項技術為新契機進入到國際E3市場。
1996年,中國獲得批準重組人生長激素制造專利,這標誌著中國開始慢慢走上世界制藥前列。
隨著中國生物醫藥技術的不斷突破,中國GDP逐年增加,人民生活水平逐年提高,醫療器材逐年更新,為中國帶來了巨大的發展潛力。
近年來,中國作為一個新興市場發展迅速,在這一領域表現不俗。
根據市場分析政策研究所的數據,中國是全球第二大Josephine市場,僅次於美國。
在2020年,中國Josephine市場達到約17億美元,僅占全球Josephine市場份額的27%。
這個數據說明了什麽?
說明作為Josephine的新興市場,中國的Josephine市場仍然有很大的增長空間。
帕西生長素註射液?
1999年和2000年,有兩名患者分別發生了嚴重的水腫,其原因被診斷為使用GH生物制劑後的副作用,其中一名患者差點陷入危機。
這兩起事件引起了廣泛關註,一些患者因此不再服用GH生物制劑,並開始尋找替代產品來避免這些副作用。
然而,GH是唯一可以起到作用的產品之一,是唯一可以維持生命的重要產品之一,因此這些患者面臨著嚴重的困境。
由於GH療法風險高、療效差,尤其在安全性和患者依從性方面存在重大不足,因此行業內迫切需要一種新的療法來取代這種舊療法。
對於這些患者而言,如果不能及時找到新的替代品,就可能面臨生命危險,因此新的療法顯得尤為重要。
在這種背景下,多年來一直致力於替代GH的新療法終於露出曙光,人們希望這種新療法能夠不僅具有效果,還能夠擺脫舊療法存在的一系列問題。
在這樣的歷史背景下,「Sogroya」作為一種新的療法應運而生,並為行業的人們帶來了新希望。
然而,「Sogroya」又是一種什麽藥物呢?
它能否滿足這些患者的預期?
同樣也引起了人們的廣泛關註。
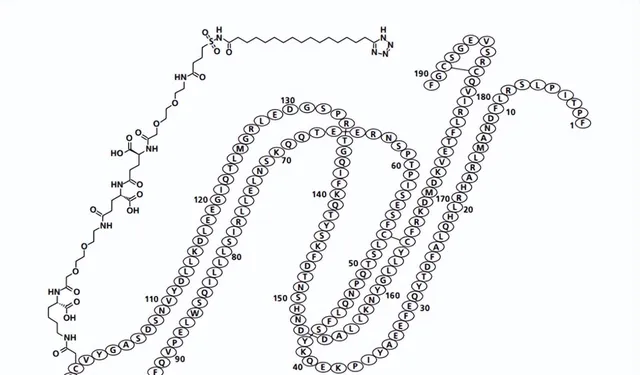
「Sogroya」作為一種新型的長期治療方案,透過DNA重組技術生產,並采用獨特的藥代動力學特性,使其成為一種與眾不同的產品。
與傳統生長激素產品相比,」Sogroya「具有獨特之處,因為它允許患者每周僅需用藥一次,而傳統產品則要求患者每日註射一次。
「雖然這看似很小,但這其中蘊含著巨大價值」一名醫生解釋道。
「想象一下,一個患者要每天堅持註射,我們只需要每周進行一次註射,這對於許多家庭來說具有重要意義。」
「我親眼目睹了一位患者在使用Sogroya後眼中流露出感動之情,說:‘我能過上正常人的生活了’。」

「Sogroya」獲得FDA批準後,其主要競爭對手「Skytropin」也成為同類產品中的一員,與「Sogroya」展開競爭。
許多人認為,當「Sogroya」上市後,它將引領整個行業進入一個新的發展階段,因為其優勢顯而易見,在保證治療效果的同時,提高了患者依從性,大大方便了患者和家庭。

「Sogroya」這一新產品在市場上的表現備受矚目,行業中的專家和醫學界普遍對於其潛力和前景持樂觀態度,因為它不單單讓治療變得更加靈活方便,更重要的是還大幅提高了患者接受治療的可能性,這無疑為廣大患者帶來了福音,讓他們終於可以過上正常人的生活。
讓我們對此充滿期待,同時也為「Sogroya」的未來發展充滿信心。
諾和諾德時刻把握市場動態。
在評估長期緩釋型生長激素制劑時,將要關註以下一些重要點:
第一,全球範圍內,對於GHD和相關情況下的公認發病率數據以及相關指南進行了評估,確保對疾病的重要性以及對創新治療需求進行了充分認識。
第二,需要向監管機構提供高質素的數據,以支持緩釋型生長激素制劑相對於目前主要市場參與者所需優越性,並解決了客戶利益相關者之間日益增長的聲望沖突。
第三,對於緩釋型生長激素制劑潛在市場影響進行評估:使用真實世界數據透過非幹預研究或臨床開發設計(PAL)進行評估。
透過這些關鍵點,醫生和研究者能夠更全面地理解長期緩釋型生長激素制劑對患者管理的重要意義,並能夠更有針對性地評估其對市場和臨床實踐的潛在影響,從而推動更好的患者護理和改善生活質素。
諾和諾德公司始終專註於GHD領域,並致力於透過嚴謹的數據分析和科學研究,提升公司在市場上的競爭地位,以應對歐洲日益增加的競爭壓力。
同時,公司還積極透過本科學術研究主導,以進一步鞏固其全球領先地位,為GHD領域帶來更多創新和突破。
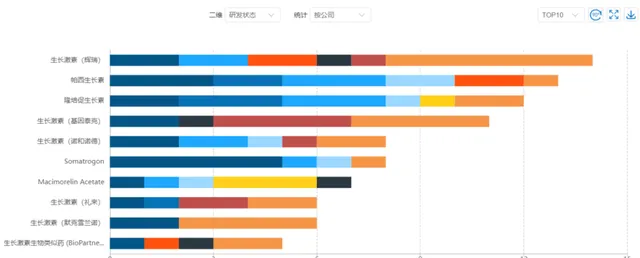
諾和諾德公司在GHD領域所占有份額顯著,其次是艾爾建公司的Genotropin,其它第3代已成為主流趨勢,競爭更為集中在這一領域,並且還可能出現後續競爭,甚至新競爭者加入。
根據報告顯示,2020年全球約有9000名兒童接受了第3代生長激素治療,而預計這一數碼將在2030年達到18,000名,其中中國將成為推動增長的重要因素之一。
到2030年,中國兒童GHD治療市場預計將達到約32億美元(約合2400億元),而當前市場僅為7.4億美元(約合56億元),年復合增長率為15.7%。
按照這個速度增長的話,有可能會成為全球最大的Josephine消費市場之一。
諾和諾德公司目前擁有已經上市產品Omnitrope以及正在開發的NNC0195-0092都處於專利保護期內,因此,如果沒有新的技術出現,其他競爭者將不能進入這個領域。
諾和諾德擁有除了NNC0195 -0092之外,還有另外兩個候選藥物進入待審批階段,因此從目前來看,其領先地位尚未受到威脅,不存在短期內出現風險或暗示的問題。
結語
綜上所述,在GHD領域面臨越來越多挑戰時,諾和諾德始終維持領先優勢,其多項創新增強了公司在GHD領域的戰略地位,同時也進一步鞏固了諾和諾德作為GHD先鋒者的位置。
諾和諾德在GHD領域所取得成果無疑為廣大GHD患者帶來了希望,也代表著未來更美好的前景。
讓我們期待諾和諾德繼續引領醫學創新,為更多患者改善生活質素。











