心源性休克(CS)是由於各種原因導致的心臟功能減退,可導致組織灌註不足,嚴重時可導致多器官衰竭和死亡。正性肌力藥物和血管收縮藥物仍然在CS治療中發揮著重要作用。近日,European Journal of Heart Failure發表的一篇綜述回顧了CS藥物治療的證據,並討論了其適用的具體臨床環境。
心源性休克概述
CS是一種以原發性心臟病為特征的臨床症候群,患者的心輸出量不足,組織灌註不足,可能導致多器官衰竭和死亡。
低灌註的臨床癥狀(即四肢冰冷、少尿、意識障礙、頭暈和脈壓窄)和/或生化表現(即血清肌酐升高、代謝性酸中毒和血清乳酸升高)對診斷CS至關重要。
低血壓(收縮壓<90mmHg)通常是CS的主要臨床表現,但其並非CS的關鍵特征,因為收縮壓可透過代償性的血管收縮(使用或不使用血管收縮藥物)來代償,盡管代價是組織灌註和氧合進一步受損。
美國心血管造影和介入學會(SCAI)將CS分為5期(表1):風險期(at risk)、開始期(beginning)、典型期( classic)、惡化期(deteriorating/doom)和終末期(extremis)。值得註意的是,SCAI分期是一個動態過程,與初始評估相比,CS發作後24h進行評估更適合預測患者的死亡率。
表1 CS的SCAI分級
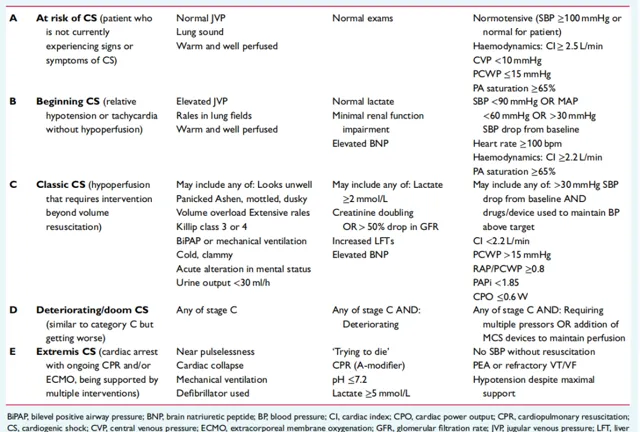
CS患病率因其定義和臨床環境而異,約占有心衰表現患者的2%-5%。急性心梗後心室衰竭仍然是CS最常見的原因,盡管在過去20年中急性心梗導致的CS發生率有所下降,但其仍是CS最主要的原因。
無論是急性心梗導致的CS還是非急性心梗導致的CS,均應進行正性肌力藥物和血管收縮藥物治療,以解決心肌功能下降和低血壓的問題。
正性肌力藥物療法
兒茶酚胺類藥物和磷酸二酯酶III(PDE-III)抑制劑均可透過增加細胞內Ca²⁺濃度來增加心肌收縮力,鑒於此,它們又被歸為靶向鈣離子的正性肌力藥物。

註:α-和β-腎上腺素能受體刺激之間的平衡決定了兒茶酚胺的主要作用。壓力-容量環說明了先前心臟功能正常的患者發生CS時的血流動力學情況,可導致心室容量和充盈壓力增加,收縮力和每搏量減少(右移)。心臟功能正常,導致心室容積和充盈壓力增加,收縮力和每搏量減少(右移)。主要透過增加平均動脈壓(MAP)(血管升壓藥)、增加左心室後負荷(Ea′)的藥物可導致曲線進一步右移(藍線)。相反,具有純變力特性(增加Ev′)的藥物可使曲線左移,同時增加收縮力和每搏量(紅線)。
01
多巴胺
多巴胺是一種內源性中樞神經遞質,在生物合成過程中是去甲腎上腺素的前體,自20世紀70年代以來一直被用於CS治療(靜脈註射)。
低劑量多巴胺(<3μg/kg/min)可促進冠脈、腎臟和腸系膜等的血管擴張並增加流向這些組織的血流量。
中等劑量多巴胺(3–10μg/kg/min)可啟用β腎上腺素受體,促進去甲腎上腺素的釋放,抑制突觸前交感神經末梢的再攝取,從而增加心臟收縮性和時變性,系統血管阻力(SVR)輕度增加。
在較高的輸註速率(10-20μg/kg/min)下,多巴胺主要作為α-腎上腺素能激動劑,導致外周血管收縮。
多巴胺使用或導致一些副作用,尤其是高劑量多巴胺套用,包括誘發快速心律不整,減少內臟及腎臟灌註,以及更罕見的並行癥,如抑制垂體前葉激素的釋放,T細胞活性的紊亂,以及化學反射敏感性和呼吸活動的改變。
02
去甲腎上腺素
去甲腎上腺素是一種交感神經合成、儲存並釋放的內源性兒茶酚胺,可作用於α₁-腎上腺素能(強效)和β₁-腎上腺素能受體(中效),是一種非強效的血管收縮劑。去甲腎上腺素可能會因後負荷增加而降低心臟功能障礙患者的心輸出量,並且具有變時特性。
去甲腎上腺素主要套用於嚴重的膿毒性休克和CS,常規劑量為0.02-1.0 μg/(kg·min)的速度輸註,並以0.1 μg/kg/min/h的速度開始逐漸減量。
與所有其他兒茶酚胺類藥物相同,去甲腎上腺素也可能發生心動過速、心肌缺血和心律不整等不良反應,但由於去甲腎上腺素的血漿半衰期較短(5-10 min),因此很容易以濃度依賴的方式進行控制。
基於現有循證證據,ESC指南及ACC/AHA指南推薦,去甲腎上腺素作為CS和顯著低血壓時的血管升壓藥。
03
腎上腺素
腎上腺素是一種內源性兒茶酚胺,可透過α₁-受體依賴性血管收縮,及其與β₁-受體結合增加血管阻力指數(SVR)。
低劑量時,腎上腺素對β-腎上腺素能受體的作用占主導地位,隨著劑量的增加,對α₁-受體的作用增強。當劑量達到0.3–0.5μg/kg/min時,被認為是高劑量,但並未強制定義休克的腎上腺素最大劑量。
高劑量和長程腎上腺素套用可透過損傷動脈壁或刺激心肌細胞雕亡,導致心臟毒性的發生。除此之外,腎上腺素還可促進房性心律不整和室性心律不整的發生,導致乳酸水平升高,從而對患者造成損傷。
OptimaCC試驗顯示,與去甲腎上腺素相比,腎上腺素與更高的難治性休克發生率相關。觀察性研究也顯示,腎上腺可增加死亡風險。鑒於此,不推薦腎上腺素作為CS的一線藥物。
盡管如此腎上腺素仍在心臟驟停中發揮關鍵作用。PARAMEDIC2試驗顯示,腎上腺素套用可顯著提高院外心臟驟停患者的30天生存率。
04
多巴酚丁胺
與其他兒茶酚胺類藥物不同,多巴酚丁胺是一種人工合成的β₁、β₂-腎上腺素能受體激動劑,也是一種強效的促血管收縮劑,且具有較弱的變時活性。
在低劑量(≤5μg/kg/min)下,多巴酚丁胺可具有輕微的血管舒張作用;在劑量較高(≥15μg/kg/min)時,其可增加心臟收縮力,但不會對外周阻力產生很多的影響。然而,在更高的輸註速率下,多巴酚丁胺的血管收縮功能逐漸占據主導地位。多巴酚丁胺通常以每小時0.1μg/kg/min或6小時0.5μg/kg/min的速率開始減量。
在多巴酚丁胺套用中,同樣可觀察到心動過速、心肌缺血、心律不整的發生,特別是在劑量≥15 μg/(kg·min)時。除此之外,其還可導致嗜酸性球增多和發熱,但由於血漿半衰期短,這些不良反應通常快速改善。
05
磷酸二酯酶III抑制劑
米力農是一種非兒茶酚胺類正性肌力藥物,在20世紀90年代初引入臨床,用於晚期心衰和CS治療。
米力農可透過抑制PDE-III[負責降解環磷酸腺苷(CAMP)的酶],來增加細胞內cAMP的數量,從而增強心肌收縮力。另外,米立農還具有松弛心肌的特性,可改善舒張功能;還可增加心率,但程度不如多巴酚丁胺。
米力農的劑量範圍為0.0625-0.5μg/kg/min,半衰期較長,如果出現低血壓或心律不整等不良反應可持續數小時。
米力農經腎臟代謝,嚴重腎損傷患者應謹慎使用,但值得註意的是,現有證據不但不顯示米力農可損傷腎功能,且提示米力農治療可改善腎功能。
與米力農類似,依諾昔酮也可抑制PDE-III,使細胞內的cAMP水平升高。依諾昔酮也可用於CS治療,且除具有腎上腺素能作用外,還可增加心臟指數。
由於PDE-III抑制劑具有協同血管舒張的作用,因此不應聯合使用,也不能與左西孟旦聯合使用。
06
左西孟旦
左西孟丹是一種鈣增敏劑,可透過對心肌肌鈣蛋白C的直接作用來增加心臟收縮力,但並不影響心室舒張功能;其為具有心肌保護作用。除此之外,左西孟旦還具有變力作用,對心室-動脈耦合、外周血管舒張也具有積極作用,從而增加組織灌註、抗暈厥作用和抗炎作用。
左西孟旦相關研究多集中於晚期心衰患者,在治療CS中的經驗有限。研究顯示,左西孟旦的耐受性良好,但左西孟旦對CS患者生存率影響的數據尚不明確。相關研究證據的總體質素有限,存在很高的偏倚和不精確風險,因此無法得出任何療法優於其他療法的結論。
其它潛在治療藥物
01
Istaroxime(伊司他肟)
伊司他肟是雄烯二酮的衍生物,可透過雙重機制發揮作用:① 透過抑制Na⁺/K⁺-ATP酶活性,導致細胞內Ca²⁺和心肌細胞收縮性增加,產生變力作用(與洋地黃類藥物相似);②透過啟用SERCA2a的促松弛作用,促進Ca²⁺再攝取,改善心肌松弛,並潛在地降低心律不整風險。
動物試驗顯示,伊司他肟在晚期心衰的狗中可產生強大的松弛-正性變力作用。與經典的cAMP依賴性正性變力藥物不同,伊司他肟可在不增加心肌耗氧量或心率的情況下發揮其作用。HORIZON-HF研究在急性心衰患者中證實了這些結果。
嘔吐和輸液部位疼痛是伊司他肟用藥主要的副作用。
02
血管緊張素II
血管緊張素II是腎素-血管緊張素-醛固酮系統的組成部份,具有多種生理作用,包括直接血管收縮、心臟重塑、增強交感神經系統、釋放血管加壓素、調節口渴機制和醛固酮釋放等。
在近期發表的CS相關試驗中,血管緊張素II展示了令人鼓舞的數據。Bansal等的研究也表明,血管緊張素II與平均動脈壓(MAP)改善、血管升壓藥需求減少和不良事件減少相關。在急性失代償性心衰相關CS患者中,院前套用血管緊張素II還可能與腎素-血管緊張素-醛固酮系統抑制劑的作用逆轉相關。
血管緊張素II的不良反應發生率較低,常見副作用包括頭痛、胸部壓迫感、消化不良、停藥後直立性低血壓及哮喘發作期間支氣管收縮加重。
血管緊張素II可快速降解,其在迴圈中的半衰期約30s,在組織中的半衰期可延長至15-30 min。
03
血管加壓素
血管加壓素在感染性休克中已被廣泛研究,但幾乎沒有證據支持其在CS患者中的套用。
在CS患者中,血管加壓素可作為心動過速、肺動脈高壓及左心室流出道梗阻患者的替代藥物,但由於心臟收縮力增加可加重左心室流出道梗阻,並進一步損害正向血流,因此使用具有變力特性的血管升壓藥(如去甲腎上腺素)可能是有害的。
然而,由於缺乏血管加壓素在CS患者中使用的可靠數據,因此暫時不建議其在CS患者中套用。
04
Procizumab
迴圈二肽基肽酶3(cDPP3)是一種參與血管緊張素II和腦啡肽降解的蛋白酶。近年來,有學者發現其與炎癥、血壓調節和疼痛調節等病理生理過程相關。動物試驗也表明,cDPP3可顯著改善心臟收縮力,具有負性變力作用。
Procizumab是一種靶向cDPP3的特異性抗體,在急性心衰小鼠模型中進行的試驗顯示,其可迅速改善心臟功能和腎臟血流動力學狀況,同時降低氧化應激和炎癥風險;但其在CS患者中的潛在作用仍有待進一步評估。
05
一氧化氮合成酶抑制劑
一氧化氮(NO)合成酶活性過高,可導致NO水平,從而引起不適當的全身血管舒張、進行性全身和冠脈灌註不足及心肌抑制。
NO合酶抑制劑可抑制NO合酶活性,已被證明在難治性AMI-CS患者中有效。然而,在TRIUMPH試驗中,盡管進行了血運重建,但tilarginine並沒有降低難治性AMI-CS患者的休克持續時間、30天和6個月的死亡率。
亞甲藍(MB)是一種血管內皮細胞中的NO合酶抑制劑,可導致NO釋放減少和系統血管阻力指數(SVR)增加。目前認為,對標準治療無反應及合並分布性休克的CS患者,可以考慮使用MB。MB給藥劑量可為1-2 mg/kg,高劑量用藥(通常>7mg/kg)時,可產生不良反應,如高鐵血紅蛋白血癥、急性溶血性貧血及對肺功能的有害影響等。
醫脈通編譯自:Mauro Riccardi, Matteo Pagnesi, Ovidiu Chioncel, et al. Medical therapy of cardiogenic shock: Contemporary use of inotropes and vasopressors. European Journal of Heart Failure (2024). doi:10.1002/ejhf.3162.
醫脈通是專業的線上醫生平台,「感知世界醫學脈搏,助力中國臨床決策」是平台的使命。醫脈通旗下擁有「臨床指南」「用藥參考」「醫學文獻王」「醫知源」「e研通」「e脈播」等系列產品,全面滿足醫學工作者臨床決策、獲取新知及提升科研效率等方面的需求。











