編者按: 嚴冬十二月,積雪亙千古。 本期【文獻薦讀】欄目由肺癌主編中國醫學科學院腫瘤醫院胡興勝教授進行肺癌領域的相關文獻薦讀。醫者「勝」也,共赴一場思想之約。
專家簡介

胡興勝 教授
中國醫學科學院腫瘤醫院內科主任醫師、碩士生導師
中國醫藥教育協會腫瘤化療專業委員會副主委/秘書長
中國醫療保健國際交流促進會腫瘤內科分會常委
中國老年腫瘤學會微生物專業委員會常委
中國中醫藥研究促進會腫瘤專業委員會常委

史慧洋
北京協和醫學院2022級碩士研究生
研究方向:胸部腫瘤的化療、靶向治療、免疫治療等。
01
研究背景
靶向治療的獲得性耐藥仍然是個尚未解決的臨床問題。雖然已經確定了許多獲得性耐藥的驅動突變,但治療期間腫瘤前進演化的潛在分子機制尚不完全清楚。患者腫瘤基因組分析提示載脂蛋白B信使RNA編輯催化多肽樣(APOBEC)胞苷脫氨酶參與腫瘤前進演化。然而,它與療效和獲得性耐藥的關系尚不明確。APOBEC可催化胞苷脫氨水解為尿苷,導致基因組中TpC基序上的C→T或C→G。由APOBEC引起的突變已經在數十種癌癥中被發現,且幾個APOBEC家族成員與腫瘤的發生發展密切相關。之前的研究表明,一些病例中預先存在的耐藥複制可能在治療選擇壓力下占主導地位,然而在另一些病例中,癌細胞可能產生短暫的中間狀態——耐藥永續性細胞(DTPs),從而產生適應和前進演化。
02
研究方法及結果
一
APOBEC突變與複制前進演化
酪胺酸激酶抑制劑(TKIs)治療的NSCLC患者可透過耐藥複制的線性前進演化逐步獲得耐藥突變。作者利用非負矩陣分解(NMF)對1例含有復合耐藥ALK突變的NSCLC患者的不同複制在序貫TKI治療期間的突變過程進行分析,發現多數新突變涉及TpC基序上的C→T和C→G的替換,這與APOBEC胞苷脫氨酶活性相關,稱之為「APOBEC突變」。有趣的是,每個獲得性耐藥的ALK突變均為APOBEC突變。此外,7個TKI耐藥細胞系的基因組測序(WGS)觀察到不同程度的APOBEC突變。在吉非替尼耐藥細胞系中,與GR2細胞(預先存在EGFRT790M)相比,GR3細胞(獲得性EGFRT790M) APOBEC突變富集。PC9複制的WGS結果也提示晚期耐藥複制(來自耐藥永續性細胞)單核苷酸變異(SNV)數量和APOBEC突變明顯高於早期耐藥複制(預先存在EGFRT790M突變)。上述結果均表明APOBEC突變富集與TKI治療期間DTP的前進演化有關。
隨後,作者構建了PC9單細胞複制庫和異質族群,用吉非替尼處理三個復制池,直至出現一個完全耐藥複制。發現耐藥複制與敏感複制基線APOBEC突變頻率沒有明顯差異,表明APOBEC突變是受治療誘導產生的,基線APOBEC突變負荷並不影響DTP的複制選擇。
二
靶向治療可誘導APOBEC3A
在11種APOBEC中,A3A和A3B都與人類癌癥相關。之前的研究表明經典APOBEC突變可能由 A3A、A3B或兩者共同引起。雖然A3B常高表達,但A3A是一個更強大的突變體,它在體內具有更強的致癌能力,並在細胞系中主導APOBEC突變。RNA測序數據集(RNA-seq)提示TKI治療期間A3A表達增加。作者利用數位PCR區分A3A和A3B活性,發現TKI治療開始後,EGFR突變NSCLC細胞系DDOST mRNA A3A發卡基序上的C→U編輯短暫升高,14天後在DTP中持續存在。在小鼠體內,用奧希替尼治療EGFR突變的NSCLC細胞系異種移植物(CLX)或患者來源的異種移植物(PDX)直至其恢復至穩定的微小殘留病竈(MRD)狀態後,發現TKI治療後殘留腫瘤的DDOST mRNA編輯較未治療組更高。此外,ALK融合抑制劑、KRASG12C和MEK抑制劑具有類似的作用,表明A3A的誘導是肺癌細胞在接受靶向治療時的常見反應。作者使用一或三代TKIs和MEK/PI3K抑制劑分別處理初治和EGFRT790M耐藥的NSCLC細胞系,發現A3A僅在EGFR和/或下遊MEK-ERK訊號通路被抑制時才被誘導,表明A3A啟用與致癌訊號受抑制相關。
三
APOBEC3A增加耐藥永續性細胞(DTPs)的基因組不穩定性
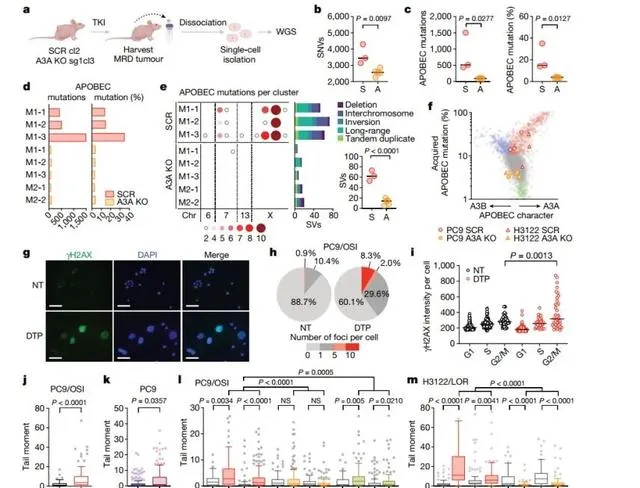
為了探索DTP細胞A3A突變與靶向治療的因果關系,作者構建了A3A缺陷複制(KO) 和對照(SCR)PC9複制,並在免疫缺陷小鼠中構建移植瘤,用奧希替尼治療22周。除了兩個SCR腫瘤復發之外,A3A KO和SCR腫瘤對奧希替尼治療均表現為消退並保持穩定的MRD狀態。采集治療22周後的MRD並構建單細胞複制,WGS顯示治療期間總SNVs和APOBEC突變在SCR腫瘤中增加,而在A3A KO腫瘤中顯著減少,且A3A KO腫瘤中不存在Kataegis突變和彌散性超突變簇。體外蘿拉替尼處理ALK融合陽性p122 DTPs細胞系的WGS提示APOBEC突變在SCR複制中富集,在A3A KO複制中減少,而在沒有蘿拉替尼處理的SCR複制中幾乎沒有觀察到APOBEC突變。以上結果均表明TKI可誘導A3A,從而導致DTPs中APOBEC突變積累。
在PC9細胞系中,與A3A KO MRD腫瘤相比,SCR的SVs(如易位、倒置和大片段插入/缺失)發生率明顯更高。DNA損傷反應標記物γpAX的免疫熒光在部份G2/M期永續性細胞中顯著增加。此外,TKI處理的DTP細胞和未經TKI處理的A3A過表達細胞均存在雙鏈斷裂(DSB)積累,而A3A敲除後的PC9 和p122細胞中TKI誘導的DSBs減少。以上結果表明TKI誘導的A3A會促進DTP細胞DNA損傷,這也解釋了TKI處理細胞中的染色體畸變現象。(下圖)
四
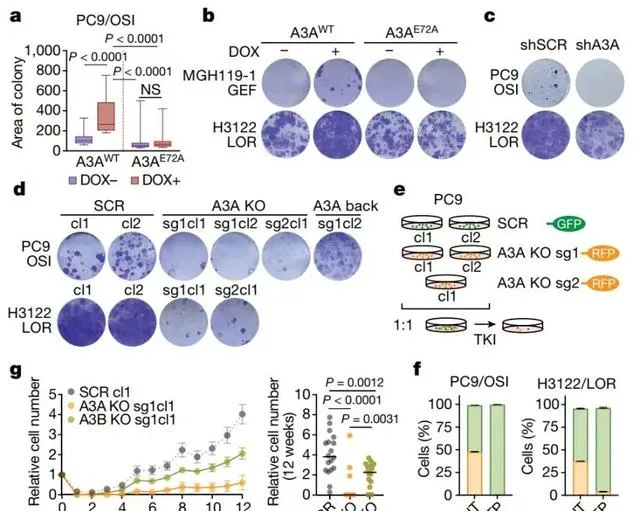
APOBEC3A促進DTPs的出現
在評估A3A對耐藥複制前進演化的影響時,作者構建了A3A過表達的PC9、MGp19-1和p122細胞系。脫氧羥四環黴素誘導的野生型A3A異常表達增大了DTP複制群落。相反,shRNA敲低或A3A敲除可抑制DTP群落的出現,而在A3A敲除的PC9細胞中重新表達野生型A3A可恢復其在奧希替尼處理下DTP群落的形成。此外,作者對多個A3A KO和SCR複制的競爭實驗表明TKI處理後SCR複制產生了大量DTPs,而A3A KO複制幾乎完全沒有DTPs,提示TKI誘導的A3A對DTPs群落的形成至關重要。最後,作者研究了TKI長期治療對A3A缺失耐藥複制的影響,發現治療12周後A3A缺失的PC9細胞中耐藥複制顯著減少。因此,TKI誘導的A3A促進了耐藥永續性細胞的存活和耐藥複制出現。(下圖)
03
結論
該研究報道了肺癌靶向治療誘導的胞苷脫氨酶APOBEC3A (A3A) 可促進雙鏈DNA斷裂,增加基因組不穩定性並驅動DTPs前進演化,從而導致治療期間耐藥細胞突變。A3A的缺失減少了永續性細胞的APOBEC突變和結構變異,延緩了耐藥的發生。此外,APOBEC突變特征在靶向治療產生持久療效後進展的肺癌患者中富集。總之,靶向治療誘導的A3A驅動耐藥永續性細胞前進演化,這表明抑制A3A的表達或活性可能是預防或延緩肺癌靶向治療獲得性耐藥的潛在治療策略。
主編評語
該研究證明臨床肺癌靶向治療可以誘導A3A的表達,從而促進耐藥永續性細胞的前進演化。多數接受靶向治療的NSCLC患者(尤其是長時間和多線TKI治療的患者)存在APOBEC突變富集。這種APOBEC獲得性突變可能代表了耐藥複制的前進演化途徑。該研究表明,對致癌訊號的抑制可以誘導APOBEC驅動突變,即靶向治療可能會反常地增加癌細胞的適應力突變。
盡管該研究支持A3A在這個過程中起主導作用,但其他一些APOBEC家族成員也在實驗模型中共表達,也可能促進靶向治療過程中腫瘤的前進演化。研究發現,在TKI治療期間A3B的缺失抑制了部份DTPs的出現,因此其他APOBEC蛋白在腫瘤前進演化中可能與A3A產生協同作用。多數NSCLC治療後樣本的A3A常見位點YTCA和莖環發夾基序中存在APOBEC突變富集。越來越多的證據表明部份腫瘤型別(如乳癌、肺腺癌、肺鱗癌、黑色素瘤和頭頸鱗癌)中彌散型超突變與A3A相關。該研究也觀察到TKI處理的細胞和小鼠移植腫瘤中小簇APOBEC突變累積,支持 A3A在NSCLC靶向治療期間促進腫瘤前進演化。
該研究描述了一例ALK融合陽性非小細胞肺癌產生的經典APOBEC突變基序上的多重抗性突變。然而,臨床上最常見的EGFR和ALK獲得性耐藥突變(如EGFRT790M、EGFRC797S和ALKG1202R)是由APOBECs常見核苷酸序列之外的堿基替換造成,不太可能直接由APOBEC突變引起。此外,作者在mRNA轉錄本中檢測到的多數A3A相關RNA編輯都是同義替換,不會改變蛋白質序列。對PC9早/晚期耐藥複制以及具有治療前後配對樣本的15例患者中獲得性驅動突變分析發現已知的APOBEC驅動突變(PIK3CA, PIK3CB, CTNNB1, KLF5, NFE2L2和ALK)僅存在於在部份患者中。其他患者和模型沒有明確可能的驅動因素,表明 APOBEC3A並不會在所有病例中驅動復發性耐藥突變產生。此外,該研究註意到TKI治療後腫瘤中A3A表達和APOBEC突變積累並不是普遍存在的,這表明治療誘導APOBEC突變的其他機制仍需進一步探索。一項一線奧希替尼治療後進展的EGFR突變肺癌的研究報告提示僅部份患者的APOBEC突變頻率增加,這也證實了上述觀點。
該研究表明抑制A3A可作為一種預防或延緩肺癌靶向治療獲得性耐藥的潛在治療策略,但迄今為止還沒有報道過相關高效或高選擇性的小分子。雖然已經發現NF-κB是TKI誘導A3A表達的關鍵轉錄因子,但最適合靶向治療的上遊節點仍需進一步確定。總之,該研究提出了一種驅動靶向治療耐藥的新機制,為後續進一步開發靶向非小細胞肺癌APOBEC3A的治療策略提供了理論依據。
醫悅匯月度關註榜
2023年11月,看看你上榜了嗎?

版權聲明
本文版權歸醫悅匯所有。歡迎轉發分享,其他任何媒體如需轉載或參照本網版權所有內容,須獲得授權,且在醒目位置處註明「轉自:醫悅匯」。












