
來 源:衛博凱,胡 靜.基於中醫傳承輔助平台與網路藥理學探析中藥幹預新型冠狀病毒感染後遺癥肺纖維化的作用機制 [J]. 中草藥, 2024, 55(1): 190-204.


肺纖維化(pulmonary fibrosis)是以上皮細胞受損、正常的肺泡組織受損、成纖維細胞增殖活化、細胞外基質異常沈積為特點,以特發性肺纖維化(idiopathic pulmonary fibrosis,IPF)為代表的多種肺間質性疾病的病理改變[1]。肺纖維化的發展過程中常伴隨有幹咳、咳少量白色泡沫樣痰、食欲減退、消瘦乏力、進行性呼吸困難,晚期則多見杵狀指、發紺等癥狀,部份患者可發展為肺心病,最終因呼吸衰竭死亡[2]。美國IPF的平均發病率為每10萬人10~60例,並且在65歲以上的老年人群中發病率是平均值8~50倍,國內尚無相關流行病學統計[3]。
新型冠狀病毒(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)感染導致的肺纖維化是其最主要後遺癥之一[4]。現有藥物如吡非尼酮及尼達尼布不僅無法完全逆轉肺纖維化的進展,並且對因SARS-CoV-2感染而導致的肺纖維化,學界僅建議二者可能是潛在治療藥物,尚無二者介入的時間點推薦以及相關臨床研究證明其幹預的有效性[5]。近年來中醫藥在肺纖維化的治療中展現了2項獨特的優勢,即單用中藥制劑可顯著延緩患者肺纖維化行程以及中藥復方與化學藥合用能有效減少具有強副作用的化學藥用量[6-7]。
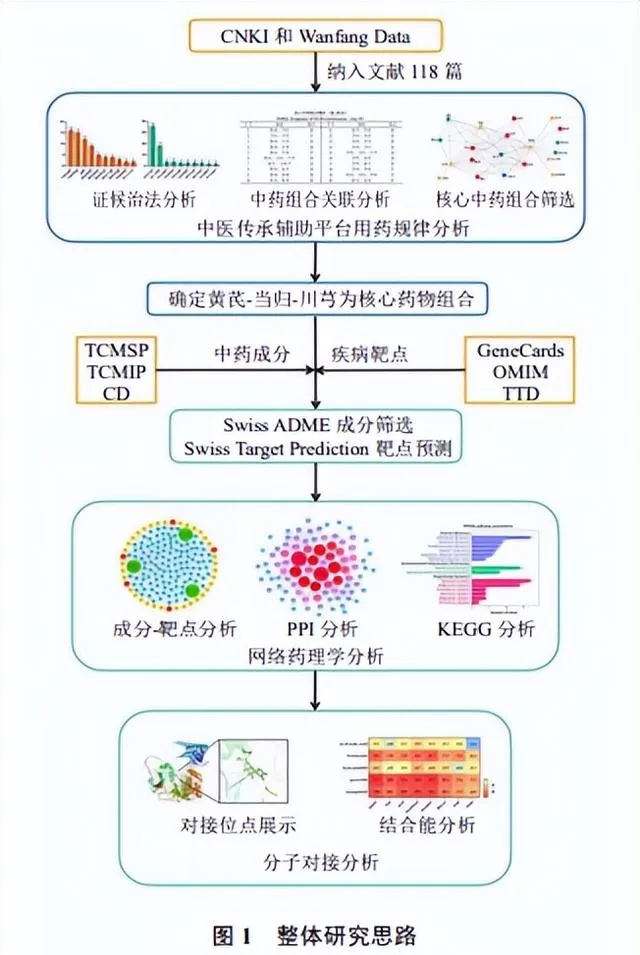
目前中醫藥幹預SARS-CoV-2感染後遺癥肺纖維化已有初步理論及臨床研究成果,但仍缺乏大範圍病例研究及學界公認的方劑組合[8-9]。因此,本研究透過中醫傳承輔助平台V3.0檢索2000年1月—2023年6月納入具有明確療效的中醫藥治療肺纖維化的臨床研究,探析其組方規律與用藥特點,並運用網路藥理學方法探析核心藥物組合的有效成分、作用靶點及訊號通路,為幹預SARS-CoV-2感染後遺癥肺纖維化提供思路,整體研究思路見圖1。
1 資料與方法
1.1 資料來源與篩選
自中國知識資源總庫(CNKI)、萬方數據知識服務平台(Wanfang Data)的檢索欄中以「肺纖維化」「間質性肺病」「矽肺」「塵肺」為關鍵詞,檢索2000年1月—2023年6月公開發表且可瀏覽全文的文獻,納入中醫藥參與治療的臨床論文共118篇。
1.2 納入標準
(1)文獻均為臨床試驗論文;(2)病例符合肺纖維化的診斷標準;(3)具有明確中藥組成的方劑、中成藥或具有中醫特色的其他制劑;(4)文獻中證明有良好的臨床療效。
1.3 排除標準
(1)非臨床試驗的文獻;(2)患者分組治療不明確;(3)患者少於30例;(4)適用證型治法分類不明確。
1.4 數據規範化處理
以【中國藥典】2020年版為標準,將中藥名稱數據進行規範化處理,如「麥門冬」規範為「麥冬」、「山萸肉」規範為「山茱萸」、「全瓜蔞」規範為「瓜蔞」等。
1.5 數據錄入及分析
使用中醫傳承輔助平台V3.0建立中藥治療肺纖維化資料庫,並進行證候分型-治則治法統計、用藥頻次統計、藥物四氣五味及歸經統計、組方規律分析。
1.6 中藥化合物篩選及靶點預測
透過對中醫藥臨床治療肺纖維化的用藥頻次統計、關聯規則分析獲取最佳藥物組合,將相關中藥輸入中藥系統藥理學分析平台(TCMSP)、中藥成分資料庫(TCMID)、化學專業資料庫(CD),得出最佳藥物組合的有效成分及靶點。將所檢索到的中藥主要化合物代入SwissADME資料庫分析,以藥動學中GIabsorption滿足high,以及類藥性中「Lipinski、Ghose、Veber、Egan、Muegge」5項篩選原則滿足至少2項為條件篩選有效化合物。將篩選後的化合物代入SwissTarget Prediction資料庫進行靶點預測。
1.7 疾病靶點收集及共同靶點構建
透過GeneCards資料庫、OMIM資料庫以及TTD資料庫以「pulmonary fibrosis」「COVID-19」為關鍵詞,獲取相關疾病的關鍵靶點以及靶點在疾病中的相關性評分(relevance scores),並與中藥有效化合物共有的靶點取交集為研究物件。
1.8 基因互作網路分析
基於核心藥物組合的化合物及靶點,利用Cytoscape 3.72軟體構建「化合物-靶點」網路,依據參數度值(degree)、中心度值(betweenness centrality)及親中心度值(closeness centrality)篩選核心化合物。透過STRING資料庫進行共靶點的蛋白互作分析(protein-protein interaction,PPI),並將結果匯入Cytoscape 3.72執行視覺化,透過omicShare進行京都基因與基因組百科全書(Kyoto encyclopedia of genes and genomes,KEGG)通路富集分析並視覺化。根據KEGG通路富集分析的結果,結合「1.5」項篩選出的核心中藥組方中不同功效的中藥類別,采用累加計演算法,在不同的重要訊號通路下累加計算每類中藥與疾病交集靶點的相關性評分。
1.9 中藥核心成分與關鍵靶點分子對接分析
從PubChem資料庫檢索中藥成分化學式,並使用ChemDraw19.0進行3D化。從PDB資料庫下載關鍵靶點的3D結構格式,運用PyMOL軟體對蛋白質進行去水、加氫等操作,利用Auto Dock軟體將化合物及靶蛋白格式轉換,執行Autodock Vina進行對接分析並視覺化。結合能小於0 kcal/mol(1 kcal=4.2 kJ)說明配體與受體可以自發結合,結合能小於−5 kcal/mol說明結合度良好。
2 結果
2.1 疾病分類與辨證論治
中醫藥治療肺纖維化的研究主要集中在IPF 63篇,其後依次為肺纖維化(未註明具體病名)34篇、塵肺病11篇、放射性肺纖維化8篇、百草枯中毒2篇。其中涉及合病研究19篇,分別為社群獲得性肺炎與肺纖維化合病4篇、慢性阻塞性肺疾病與肺纖維化合病4篇、類風濕關節炎與肺纖維化合病3篇、結締組織病與肺纖維化合病3篇、幹燥症候群與肺纖維化合病2篇、肺癌與放射性肺纖維化合病1篇、焦慮癥與肺纖維化合病1篇,肺源性心臟病與塵肺病合病1篇。在用藥劑型上主要以湯劑為主(82篇),其後依次為顆粒劑14篇、註射液10篇、膠囊9篇、丸劑2篇、離子匯入1篇。
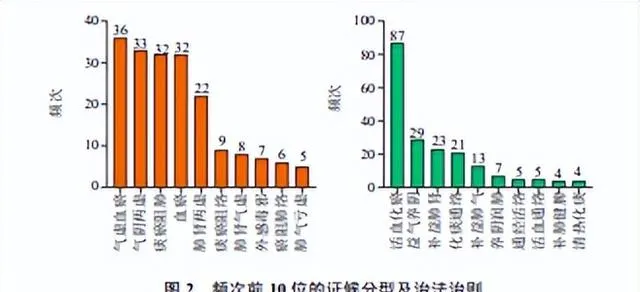
在辨證方面,證候分型前10位依次為氣虛血瘀證、氣陰兩虛證、痰瘀阻肺證、血瘀證、肺腎兩虛證、痰瘀阻絡證、肺腎氣虛證、外感毒邪證、瘀阻肺絡證以及肺氣虧虛證。而在治法治則方面以活血化瘀為主,前10位其余治法治則依次為益氣養陰、補益肺腎、化痰通絡、補益肺氣、養陰潤肺、通經活絡、活血通絡、補肺健脾以及清熱化痰,見圖2。
2.2 用藥規律及性味歸經
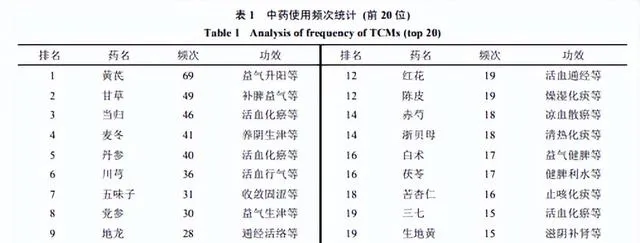
對納入的118篇中醫藥治療肺纖維化方劑中的185味中藥(使用頻次1 078次)進行統計分析(表1)。使用頻次前20位的藥物主要包括4大類:補氣類(黃芪、甘草、黨參、白朮、茯苓)、活血化瘀類(當歸、丹參、川芎、地龍、桃仁、紅花、赤芍、三七、莪術)、養陰類(麥冬、五味子、生地黃)以及止咳化痰類(半夏、陳皮、浙貝母、苦杏仁、桔梗)。在功效上,上述藥物依次以補虛類(424次)、活血化瘀類(179次)、化痰止咳平喘類(155次)、清熱類(87次)、平肝熄風類(47次)等為主。
在性味上,上述藥物的四氣排序依次為溫(456次)、寒(323次)、平(268次)、涼(17次)、熱(14次);五味排序依次為甘(619次)、苦(530次)、辛(308次)、鹹(80次)、酸(54次)。在藥物歸經上排序依次為肺經(624次)、脾經(465次)、心經(442次)、肝經(430次)、胃經(256次)、腎經(228次)、大腸經(74次)、膽經(59次)、膀胱經(29次)、小腸經(17次)、三焦經(3次)、心包經(2次)。
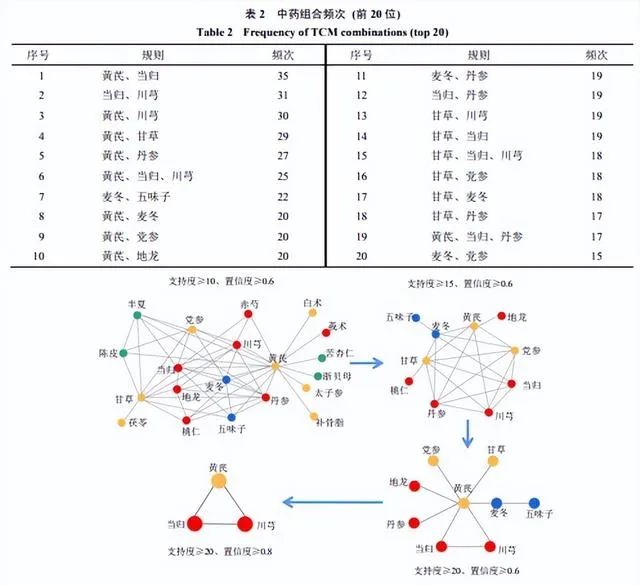
2.3 組方規律分析
設定支持度≥10、置信度≥0.6為初始參數分析用藥規則。支持度=支持度個數/總處方數量,置信度是方劑中A藥出現時,B藥出現的機率。支持度越高,說明方劑用藥越集中;置信度越高,說明用藥配伍關聯性越高。在上述支持度、置信度設定條件下,篩選出頻次前20位中藥組合模式,見表2。在參數設定為支持度≥10、置信度≥0.6時,得出重要中藥組合21味:黃芪、麥冬、川芎、丹參、當歸、甘草、太子參、補骨脂、莪術、赤芍、苦杏仁、陳皮、五味子、茯苓、地龍、半夏、黨參、白朮、紅花、浙貝母、桃仁。
將上述21味中藥按功效可分為補氣類(黃芪、太子參、甘草、茯苓、黨參、白朮)、活血類(川芎、丹參、當歸、紅花、桃仁、地龍、莪術、赤芍)、養陰類(麥冬、五味子)、補陽類(補骨脂)、止咳化痰類(半夏、陳皮、苦杏仁、浙貝母)共5類。將參數設定為支持度≥15、置信度≥0.6時,得出核心中藥10味:黃芪、當歸、甘草、川芎、丹參、麥冬、黨參、五味子、桃仁、地龍。將參數設定為支持度≥20、置信度≥0.6時,得出核心中藥9味:黃芪、當歸、甘草、川芎、丹參、麥冬、黨參、五味子、地龍。將參數設定為支持度≥20、置信度≥0.8時,得出核心中藥組合3味:當歸、川芎、黃芪,見圖3。
2.4 確定黃芪-當歸-川芎為核心藥物組合
透過中藥使用頻次分析得出,黃芪使用頻次位居第1位(69次),當歸使用頻次位居第3位(46次),川芎使用頻次位居第6位(36次);透過不同支持度下組方規律分析得出,當歸、川芎、黃芪組合的頻次為25次;透過中藥組合關聯規則分析得出,川芎→當歸、川芎→黃芪、黃芪、川芎→當歸、當歸、川芎→黃芪組合的置信度均≥0.8。綜上分析結果,確定「黃芪-當歸-川芎」為臨床上中醫治療肺纖維化核心藥物組合。
2.5 黃芪-當歸-川芎有效成分-疾病靶點構建
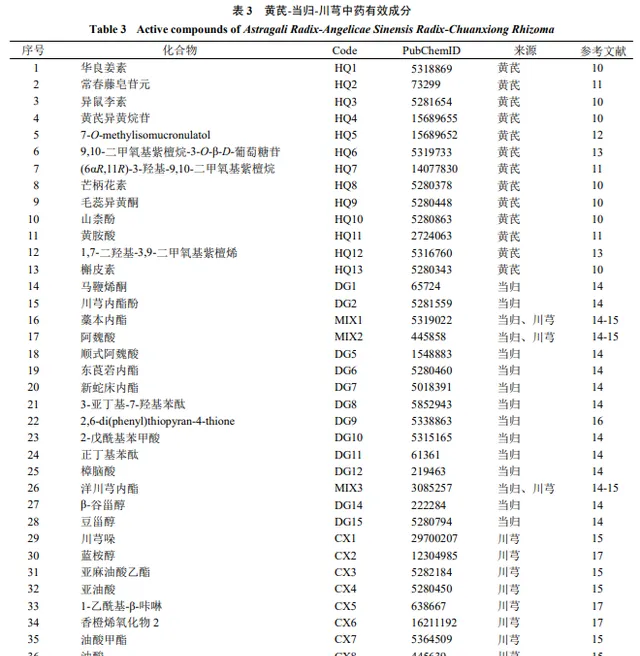
透過TCMSP、TCMID、中藥證候關聯資料庫、CD資料庫及文獻檢索共收集黃芪有效成分48種、當歸有效成分37種、川芎有效成分28種。經過SwissADME資料庫篩選出黃芪有效成分13種、當歸有效成分15種、川芎有效成分13種,其中共有成分3種,見表3。將以上有效成分代入SwissTargetPrediction資料庫整理後篩選出黃芪潛在治療靶點427個、當歸潛在治療靶點399個、川芎潛在治療靶點264個,刪除重復值後共獲得黃芪-當歸-川芎潛在治療靶點501個。
從GeneCards資料庫收集整理肺纖維化與COVID-19共病的關鍵靶點2 911個,與黃芪-當歸-川芎潛在治療靶點取交集獲得共同靶點121個。可以初步認為黃芪-當歸-川芎透過121個靶點對SARS-CoV-2感染後遺癥肺纖維化產生幹預作用。將共同靶點與中藥有效成分代入Cytoscape 3.72進行視覺化分析,透過Network Analyzer分析度值、中心度值及親中心度值,篩選出前5位中藥有效成分為核心成分:山柰酚(kaempferol,HQ10,來源於黃芪)、槲皮素(quercetin,HQ13,來源於黃芪)、順式阿魏酸( cis -ferulic acid,DG5,來源於當歸)、洋川芎內酯(senkyunolide,MIX3,來源於當歸、川芎)、川芎哚(perlolyrine,CX1,來源於川芎),見圖4。

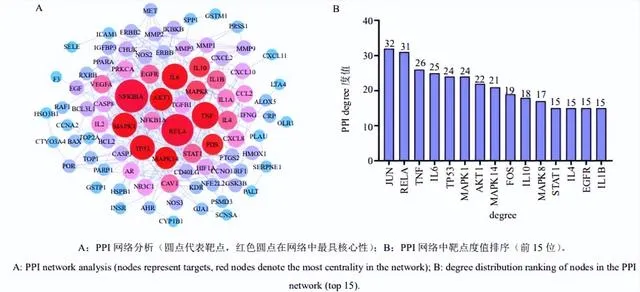
2.6 PPI網路分析
基於STRING資料庫對黃芪-當歸-川芎幹預SARS-CoV-2感染後遺癥肺纖維化的121個共同靶點進行蛋白互作分析,設定interaction score為hightest confidence(0.900)並將結果匯入Cytoscape 3.72軟體進行進一步拓撲分析,按照度值由大到小,結合中心度值及親中心度值綜合判斷篩選出前8位元靶點為AP-1轉錄因子亞基(AP-1 transcription factor subunit,JUN)、核因子-κB亞基(NF-κB subunit,RELA)、腫瘤壞死因子(tumor necrosis factor,TNF)、白血球介素6(interleukin 6,IL6)、腫瘤蛋白p53(tumor protein p53,TP53)、絲裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)1、蛋白激酶B1(protein kinase B1,AKT1)、MAPK14,如圖5所示。
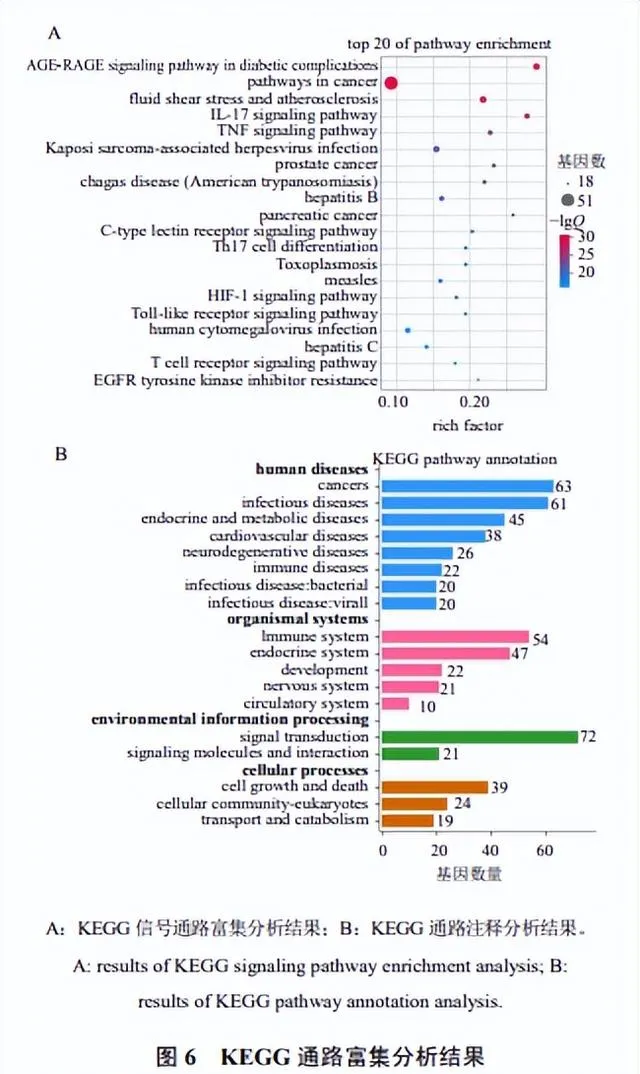
2.7 KEGG通路富集分析
將上述共同靶點進行KEGG通路富集分析,結果提示黃芪-當歸-川芎對SARS-CoV-2感染後遺癥肺纖維化的幹預作用主要集中在晚期糖基化終末產物-晚期糖基化終末產物受體(advanced glycation end products-receptor for advanced glycation end products,AGE-RAGE)訊號通路、白血球介素-17(interleukin-17,IL-17)訊號通路、腫瘤壞死因子(tumor necrosis factor,TNF)訊號通路、流體剪下力與動脈粥樣硬化等訊號通路上。進一步對KEGG通路進行註釋分析發現,在人類疾病方面主要涉及包括病毒感染、細菌感染在內的感染性疾病,此外包括癌癥、心血管疾病、內分泌與代謝性疾病、免疫性疾病等;在環境資訊處理方面涉及訊息傳遞、訊號分子與交互作用;在組織系統方面主要涉及免疫系統,此外還包括內分泌系統、迴圈系統等,見圖6。
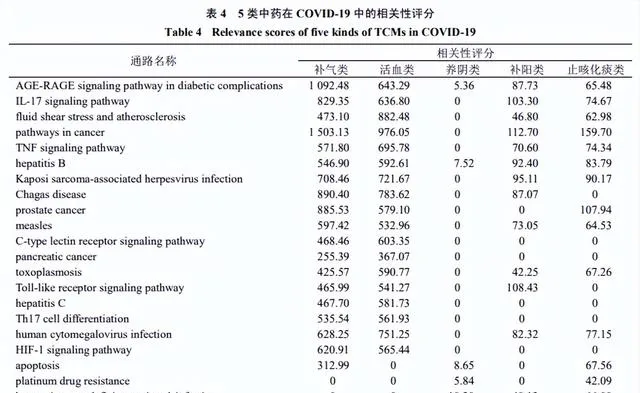
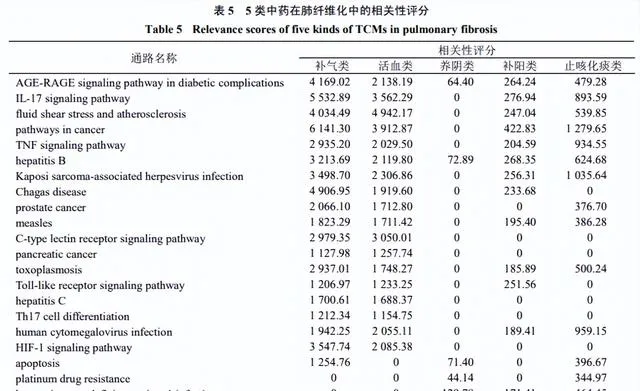
為進一步探索中醫藥治療肺纖維化的用藥特點,結合組方規律分析結果,以118篇中醫藥治療肺纖維化方劑中的185味中藥的前10%,即核心組方中(中藥21味)按照中藥功效分類可分為補氣類、活血類、養陰類、補陽類及止咳化痰類共5類,進行進一步的KEGG通路富集分析,以探明每類中藥在治療SARS-CoV-2感染後遺癥肺纖維化的共性與特點。Relevance scores是GeneCards資料庫基於Elasticsearch 7.11對蛋白靶點與疾病的相關性的評分,評分越高說明該靶點在該疾病中具有越重要的作用。
在共性上,將5類中藥與SARS-CoV-2感染後遺癥肺纖維化的共靶點分別進行KEGG通路富集分析,取每類中藥KEGG通路富集前20位的共有通路進行relevance scores評價,結果提示補氣類與活血類中藥在COVID-19及肺纖維化中的相關性評分相對最高,其治療SARS-CoV-2感染後遺癥肺纖維化的作用通路主要富集在AGE-RAGE訊號通路、IL-17訊號通路、流體剪下力與動脈粥樣硬化通路、癌癥相關訊號通路與TNF等訊號通路上,見表4、5。
在特點上,將5類中藥各自的獨有靶點與SARS-CoV-2感染後遺癥肺纖維化的共靶點進行分析,發現補氣類的獨有靶點5個:OLR1、MAPK10、HSD3B1、ATP5F1B與FASLG;活血類的獨有靶點19個:TGM2、TNFRSF1A、TNFRSF1B、ABCC4、EDN1、ALB、EDNRA、SELP、TLR2、NPM1、MMP10、G6PD、CD14、KCNK2、NFKB1、ECE1、ITGB3、TRPV1與CTNNB1;補陽類的獨有靶點3個:CD80、CD40與CD86;養陰類的獨有靶點24個:GPI(CM000681.2)、LDHA、OAT、ASNS、CPT2、GPI(KI270866.1)、SHMT2、SLC25A13、ARG1、GLUD1、GPT、F13A1、PFAS、TPI1、SDHA、LDHB、GOT2、MMP12、PDHB、LTF、MTR、PC、LDHA與KYNU;止咳化痰類的獨有靶點4個:CYCS、EPHB2、CD163與CREB1。
將上述獨有靶點分別進行KEGG通路富集分析,結果發現補氣類獨有靶點主要富集在神經營養因子訊號通路、麻疹、B型肝炎等訊號通路上;活血類獨有靶點主要富集在流體剪下力與動脈粥樣硬化通路、沙門氏菌感染、TNF等訊號通路上;補陽類獨有靶點主要富集在Toll樣受體訊號通路、產生IgA的腸道免疫網路、病毒性心肌炎等訊號通路上;養陰類獨有靶點主要富集在碳代謝、胺基酸合成、精胺酸生物合成等訊號通路上;止咳化痰類獨有靶點主要富集在肺結核、卡波西肉瘤相關皰疹病毒感染、人巨細胞病毒感染等訊號通路上,見表6。

2.8 中藥核心成分與關鍵靶點分子對接
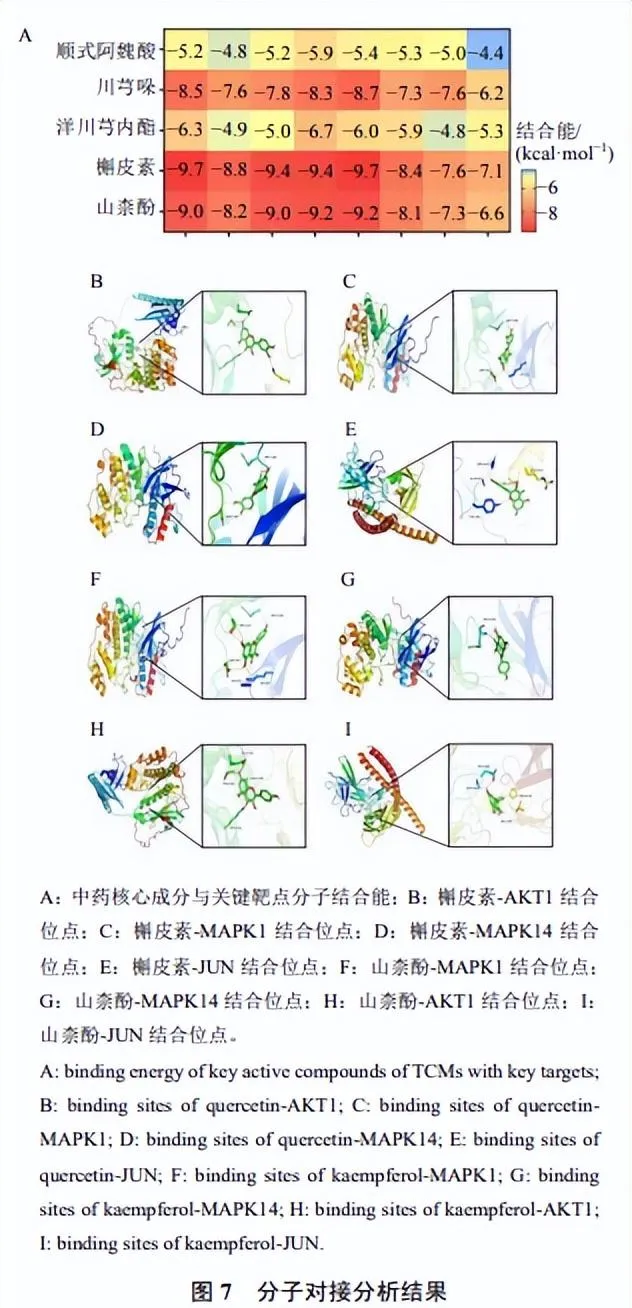
根據「2.5「項所篩選出的中藥核心成分山柰酚(kaempferol)、槲皮素(quercetin)、順式阿魏酸( cis -ferulic acid)、洋川芎內酯(senkyunolide)、川芎哚(perlolyrine)及「2.6」項篩選出的關鍵靶點JUN(PBD ID: 5FV8)、RELA(PBD ID: 3QXY)、TNF(PBD ID: 5UUI)、IL6(PBD ID: 1ALU)、TP53(PBD ID: 3ZME)、MAPK1(PBD ID: 5BVE)、AKT1(PBD ID: 1UNQ)、MAPK14(PBD ID: 5XYY)進行分子對接分析。
結果表明,中藥核心成分與關鍵靶點的總體結合能良好,一定程度上體現了黃芪-當歸-川芎多成分、多靶點幹預SARS-CoV-2感染後遺癥肺纖維化的潛在機制,見圖7-A。其中結合能最低的成分-靶點分別為槲皮素-AKT1與槲皮素-MAPK1,結合能均為−9.7kcal/mol;隨後為槲皮素-MAPK14與槲皮素-JUN,結合能均為−9.4 kcal/mol;之後為山柰酚-MAPK1與山柰酚-MAPK14,結合能均為−9.2 kcal/mol;最後為山柰酚-AKT1與山柰酚-JUN,結合能均為−9.0 kcal/mol,見圖7-B~I。槲皮素和山柰酚與多數核心靶點結合能總體最佳,川芎哚與多數核心靶點結合能總體較好,提示黃芪-當歸-川芎藥物組合中槲皮素、山柰酚與川芎哚是其多靶點幹預SARS-CoV-2感染後遺癥肺纖維化的最關鍵核心成分。
3 討論
肺纖維化是現代病理學名稱,是以IPF為代表的多種肺間質性疾病的病理表現,與中醫經典著作中疾病的命名無直接對應。目前學界認為肺纖維化的致病因素以痰、毒、瘀、虛為重,病機以本虛標實為多,病位涉及肺、脾、腎為主,在病名上多從「肺痹」「肺萎」論治[1,18-19]。目前臨床上各家針對肺纖維化具體的辨證治法尚無定論,故本研究對2000年1月—2023年6月具有明確療效的中醫藥治療肺纖維化的118篇臨床研究文獻進行整理歸納以探求其特點與共性。
上述臨床研究在辨證方面多從氣虛血瘀證、氣陰兩虛證、痰瘀阻肺證、血瘀證而論,在治法上多從活血化瘀、益氣養陰、補益肺腎而治。其中涉及的185味中藥中,使用頻次前20味的高頻中藥中補氣類中藥占據5味,且黃芪、甘草的使用頻次最高,此外活血化瘀類中藥占據9味,主要以當歸、川芎、丹參為主,余以養陰、止咳化痰之藥,這與目前學界對肺纖維化「本虛標實」的認識相符。
在組方規律分析方面,設定支持度≥10、置信度≥0.6為參數分析用藥規則後,隨著支持度提高,補氣類與活血化瘀類中藥在頻次上所占比重逐漸提升,而當支持度≥20、置信度≥0.8時僅剩「黃芪-當歸-川芎」組合。該結果表明臨床上補氣類與活血化瘀類中藥廣泛用於肺纖維化的治療,且具有益氣活血特點的「黃芪-當歸-川芎」是最核心、最常用的藥物組合。
正如【讀醫隨筆】中「氣虛不足以推血,則血必有瘀」與【醫林改錯】中的「元氣既虛,必不能達於血管,血管無氣,必停留而為瘀。」強調了氣對血的推動作用,氣虛推動無力而導致血瘀,無氣則必瘀。中醫經典中「黃芪-當歸-川芎」的配伍廣泛出現,如【濟陰綱目】中黃芪四物湯、【醫林改錯】中補陽還五湯、【外科正宗】中調和營衛湯等治療各類瘀血內阻而正氣已虛之疾病,因此對於肺纖維化治療當註重補氣與活血並用而促進瘀血的消散。
目前國內SARS-CoV-2感染流行的Omicron變異株主要引起無癥狀感染和輕癥感染,但對於免疫力低下人群、老年人群患者仍有較大患重癥的風險而危及生命[20-21]。SARS-CoV-2感染患者與凝血功能異常關系密切,在住院的患者中靜脈栓塞和肺動脈栓塞的發生率分別為17%和7.1%[22],並且在重癥患者中靜脈栓塞的發生率更高(28%)[23]。研究表明,腫瘤壞死因子-α(tumor necrosis factor-α,TNF-α)和IL-6等炎癥因子是SARS-CoV-2感染患者血栓形成的重要因素[24-25],而早期使用抗凝療法與更好的預後相關[26]。此外SARS-CoV-2感染可導致多種嚴重的後遺癥,尤其是肺纖維化的發生。
1項英國的研究分析發現超過11%的患者在出院240 d內的肺CT顯示出纖維化樣改變[27]。另1項對出院2年後患者的佇列研究發現39.7%的患者有不同程度的纖維化樣改變[28]。對重癥SARS-CoV-2感染患者康復半年後的CT中發現超過三分之一的患者發生肺纖維化[29],並且在30例因SARS-CoV-2感染去世患者的屍檢中發現有43%發生嚴重的肺纖維化[30]。
近期1項研究發現老年SARS-CoV-2感染患者發生包括肺纖維化在內的嚴重後遺癥的比例更高,其發生機制與其較弱的免疫應答相關,而適度的免疫啟用有助於對SARS-CoV-2的清除[31]。上述結果表明SARS-CoV-2感染後遺癥肺纖維化在重癥及老年患者中發生比例更高,因此盡早使用抗凝療法,適當提升機體免疫力與減少重癥發生率,降低SARS-CoV-2感染後遺癥肺纖維化的發生及更好的預後相關,這與中醫學界對肺纖維化用藥選擇及治法不謀而合。
透過對「黃芪-當歸-川芎」核心藥物組合進行網路藥理學分析發現槲皮素、山柰酚、川芎哚、洋川芎內酯與順式阿魏酸是其核心藥物成分,AKT1、MAPK14、MAPK1、JUN等是其主要幹預靶點。AKT1是一種絲/蘇胺酸激酶,主要透過磷脂酰肌醇-3-羥激酶(phosphatidylinositol-3-hydroxykinase,PI3K)/AKT訊號通路介導炎癥反應、血管生成及細胞增殖雕亡等,研究發現SARS-CoV-2感染患者肺臟中更高的AKT1表達與更嚴重的肺損傷及肺纖維化相關[32],並且AKT1是連花清瘟膠囊及清肺排毒湯幹預SARS-CoV-2感染的重要靶點之一[33-34]。JUN、MAPK1及MAPK14均屬於MAPK訊號通路,該通路的啟用與SARS-CoV-2感染及肺纖維化關系密切。
SARS-CoV-2的感染能促進MAPK14的磷酸化[35],並且SARS-CoV-2感染患者外周血中表現出更高水平的MAPK1與JUN[36]。PI3K/AKT訊號通路及MAPK訊號通路的啟用對肺纖維化具有顯著的促進作用,在博來黴素造模的肺纖維化大鼠模型中AKT1的表達顯著上升[37],p38 MAPK(MAPK14)可啟用轉錄因子JUN,促進巨噬細胞及嗜中性球的聚集從而促進肺纖維化的發展[38]。
此外,分子對接結果提示槲皮素、山柰酚與川芎哚可能是「黃芪-當歸-川芎」核心藥物組合多靶點幹預SARS-CoV-2感染後遺癥肺纖維化的最關鍵核心成分,順式阿魏酸與洋川芎內酯同樣具有一定的藥用潛力。槲皮素廣泛存在於黃芪、三七、連翹等多種中藥中,具有廣泛的抗炎、抗病毒及抗氧化功效[39]。目前已有多項生物資訊學研究提示槲皮素對SARS-CoV-2具有潛在的抑制作用,但仍未見詳細的機制研究[33,40-41]。
在臨床研究中,槲皮素聯合抗病毒藥物有效地降低了患者血清中堿性磷酸酶、乳酸去氫酶及C反應蛋白水平,減少患者住院時間[42]。相似的是,近期的一項薈萃分析發現槲皮素能有效降低患者的住院率以及重癥率[43]。
在抗肺纖維化的相關研究中,槲皮素的作用機制研究較為成熟,在動物模型中能有效減少肺臟TNF-α、IL-6等炎癥因子的表達及羥脯胺酸含量,減少膠原纖維面積,其機制與抑制轉化生長因子β1(transforming growth factor beta 1,TGF-β1)/p38 MAPK/核因子-κB(nuclear factor-κB,NF-κB)訊號通路,減少氧化應激反應,抑制菸鹼醯胺腺嘌呤二核苷酸磷酸氧化酶4(nicotinamide adenine dinucleotide phosphate oxidase 4,NOX4)-p62訊號途徑等有關[44-46]。但目前未見槲皮素抗肺纖維化的相關臨床研究,因此進一步探究槲皮素抗SARS-CoV-2感染的機制與特點,以及開展抗肺纖維化的臨床研究是其未來的重要研究方向。
山柰酚同樣存在於包括黃芪在內的多種中藥中,藥理學研究表明其具有抗炎、抗氧化、抗抑郁等功效,對癌癥及心腦血管疾病具有一定治療作用[47]。目前未見山柰酚幹預SARS-CoV-2的臨床及機制研究,而其抗纖維化的機制主要與恢復E-鈣黏蛋白水平,抑制上皮細胞間充化(epithelial-mesenchymal transition,EMT)的發生等有關[48],因此仍需進一步基礎與臨床研究以闡明其作用機制。
川芎哚主要存在於川芎、當歸之中,目前除早期文獻報道其抗血小板、抗血栓、改善血流動力學的作用外,近期尚無相關抗炎、抗凝作用的研究報道,這可能與其代謝快、藥效維持時間較短有關[49-50]。結合分子對接分析結果,如何解決川芎哚代謝快、藥效維持時間較短的弊端,以及探索川芎哚在抗炎、抗纖維化的潛能可能是其未來重點研究方向。洋川芎內酯是當歸、川芎的主要活性成分之一,能透過抑制NOD樣受體熱蛋白結構域相關蛋白3(NOD-like receptor thermal protein domain associated protein 3,NLRP3)、胺基末端激酶(jun kinase,JNK)、細胞外訊號調節激酶(extracellular signal-regulated kinase,ERK)訊號通路發揮抑制炎癥的作用[51-52]。雖然目前未見其幹預SARS-CoV-2及抗肺纖維化的研究,但分子對接的結果提示具有良好的研究前景。
阿魏酸廣泛存在於當歸、阿魏、升麻等中藥中,具有良好的抗炎、抗凝作用。在體內,阿魏酸能降低小鼠炎癥模型中IL-1β、IL-6的表達水平,抑制大鼠凝血酶的活性、延長出血時間、抑制軔靜脈血流旁路血栓的形成[53-54];在體外,阿魏酸可降低SARS-CoV-2的病毒滴度發揮抗病毒的功效[55]。總體而言,「黃芪-當歸-川芎」核心藥物組合中核心藥物成分均具有一定幹預SARS-CoV-2及抗肺纖維化的功效,但缺乏深入的機制研究及臨床研究結果加以驗證。
KEGG通路富集分析是一種從復雜調控網路角度對生物的基因集合進行通路富集歸納的分析手段,是研究生物功能的重要方法之一[56]。「黃芪-當歸-川芎」核心藥物組合幹預SARS-CoV-2感染後遺癥肺纖維化的共同靶點主要富集在IL-17訊號通路、TNF訊號通路、AGE-RAGE訊號通路、流體剪下力、動脈粥樣硬化通路等與感染性疾病、免疫系統關聯性較強的訊號通路,一定程度說明了抗感染、抗凝血與免疫調節是其最重要的機制。
結合組方規律分析結果,發現21味中藥組合中補氣藥與活血藥在基於KEGG通路富集分析的肺纖維化與COVID-19相關性評分遠超補陽類、養陰類與止咳化痰類中藥,進一步說明了補氣藥與活血藥的聯用是學界最常用的藥物選擇。
同時在5類中藥獨有靶點的KEGG通路富集分析上,補氣類中藥主要富集在神經營養因子訊號通路,養陰類中藥則富集在胺基酸合成與精胺酸生物合成等訊號通路上,從一定程度體現了這2類中藥「補虛」的特點;活血類中藥主要富集在流體剪下力與動脈粥樣硬化這一與中醫理論中「血瘀」概念極其相關的通路,彰顯了其活血化瘀的功效;止咳化痰類中藥主要富集在肺結核通路等與呼吸系統密切相關的訊號通路上;而補陽類中藥主要富集在與免疫啟用密切相關的Toll樣受體訊號通路,體現了陽氣溫煦推動、抵禦外邪之特色。上述研究結果為中醫藥幹預SARS-CoV-2感染後遺癥肺纖維化提供了訊號通路的參考,尤其針對不同中藥功效上的特點,為後續相關藥物研究提供部份證據支持。
本研究受限於研究方法仍存在許多不足。首先,中醫藥治療肺纖維化學界尚無治法方藥的標準與定論,因此納入文獻在方藥種類選擇上較分散,需在組方規律分析初步篩選中納入更多藥味進行全面的分析,但限於網路藥理學的分析手段,如無法區分如生甘草與炙甘草、生地黃與熟地黃,本研究僅能透過納入前10%中藥作為初步篩選條件,最大化避免上述的限制,導致在進行KEGG通路富集分析的相關性評分時所能納入的補陽類與養陰類中藥種類較少。其次,由於所納入的臨床文獻存在包括湯劑、顆粒劑、註射液等多種劑型,且部份文獻未公布中藥用量,無法對中藥進行全面的劑量區間統計。最後,受限於分子對接技術特點,目前僅能確定中藥成分對核心靶點的結合能高低,無法確定對結合靶點的抑制或啟用,未來需結合轉錄組學及實驗驗證進一步闡釋。
4 結論
綜上所述,本研究基於中醫傳承輔助平台與網路藥理學,發現中醫藥治療肺纖維化臨床研究中辨證以氣虛血瘀證、氣陰兩虛證、血瘀證居多,治法以活血化瘀法為重,用藥以補氣藥和活血化瘀藥為主,在組方規律上「黃芪-當歸-川芎」是核心藥物組合,其核心成分包括槲皮素、山柰酚、川芎哚等,核心靶點包括AKT1、MAPK14、MAPK1、JUN等,透過AGE-RAGE訊號通路、IL-17訊號通路、TNF訊號通路、流體剪下力與動脈粥樣硬化等訊號通路發揮幹預SARS-CoV-2感染後遺癥肺纖維化的作用。











