
撰文 | 王聰
編輯 | 王多魚
排版 | 水成文
多細胞生物在發育過程中,存在著多種預定的、受到精確控制的 細胞程式性死亡 ,例如細胞雕亡(Apoptosis)、程式性壞死(Necroptosis)、細胞焦亡(Pyroptosis),以及 鐵死亡 (Ferroptosis)等。
鐵死亡 是2012年由哥倫比亞大學 Brent Stockwell 實驗室發現的一種鐵依賴性的新型細胞程式性死亡方式【1】,由過度堆積的 過氧化脂質 (peroxidized lipids)誘導發生,其形態特征,作用方式以及分子機制與其他程式性死亡方式截然不同。
β-螺旋蛋白相關神經退行性疾病 (BPAN)是一種罕見的X連鎖顯性遺傳病,主要影響女性。它是幾種表現出神經退行性和大腦鐵積累的疾病之一。在BPAN疾病中,編碼 WIPI4 蛋白的基因WDR45發生功能喪失突變,但這種突變如何觸發該疾病病理的細胞機制尚不清楚。
由於WIPI4參與細胞自噬,因此,之前的研究普遍認為BPAN病理主要是由於細胞內自噬功能障礙導致的。
2024年3月7日,劍橋大學的研究人員在 Nature Cell Biology 期刊發表了題為:Loss of WIPI4 in neurodegeneration causes autophagy-independent ferroptosis 的研究論文。
該研究表明, WIPI4 功能缺失透過一種自噬非依賴性機制導致 鐵死亡 ,這一機制與經典的鐵死亡誘導因素極少有重疊,為 β-螺旋蛋白相關神經退行性疾病 (BPAN)的病因提供了新見解,並可能為治療策略提供新線索。

在這項研究發表之前,已有個別研究表明WDR45基因的缺失會導致鐵死亡,但認為這些鐵死亡是由於自噬依賴性缺陷。
而在這項最新研究中,研究團隊透過體外細胞實驗和體內動物模型實驗發現, WIPI4 蛋白缺失導致的鐵死亡是不依賴於自噬的,這是一種以前沒有被考慮過的可能性。
具體來說,該研究發現,BPAN疾病中可能發生WIPI4缺失導致的自噬非依賴性鐵死亡,其依賴於ATG2介導的磷脂酰絲胺酸(PS)運輸,從而導致更多的線粒體磷脂酰乙醇胺(PE)合成。在正常條件下,WIPI4透過蛋白質間直接相互作用將ATG2的羧基(C)末端穩定在自噬小體上,並允許脂質從內質網轉移到自噬小體。在WIPI4缺失的情況下,ATG2的C末端定位到線粒體上增加,導致PS從內質網轉移到線粒體的增加,並透過線粒體PE合酶 PISD 向PE的轉化水平提高。
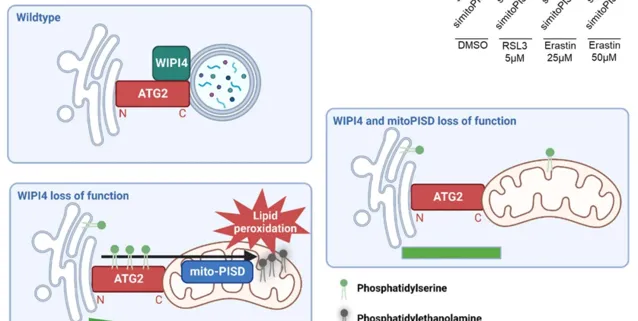
線粒體PE水平的增加促進了鐵死亡,可能是因為多不飽和PE是鐵死亡的主要受質。當線粒體PISD被抑制時,內質網-線粒體PS濃度梯度消失,這減緩了內質網-線粒體PS轉移和鐵死亡。這些數據強調了線粒體PE生成在鐵死亡中的重要性。盡管這是WIPI4缺陷的主要驅動因素,但對於其他刺激引起的鐵死亡,其限制速率的程度仍需要詳細評估。
更重要的是,由於PISD可透過藥物進行抑制,這為治療BPAN疾病帶來了新的可能性。除了BPAN之外,該研究也提示了阿爾茨海默病、帕金森病和亨廷頓病等神經退行性疾病都與鐵死亡有關。
論文連結 :












