文 | 科誌康 作者:胰島素
11月22日,CDE官網公示,賽諾菲的BIVV020註射液納入突破性治療品種,擬用於治療慢性炎性脫髓鞘性多發性神經根神經病(CIDP)。

CIDP是一組免疫介導的炎性脫髓鞘罕見疾病,呈慢性進展或復發性病程。通常表現為隱襲起病,癥狀進展至少達8周以上。主要表現為符合周圍神經分布的肢體無力和感覺異常,腦神經受累較少,極少累及自主神經或呼吸功能。根據【慢性炎性脫髓鞘性多發性神經根神經病診治中國專家共識2022】,糖皮質激素、IVIG和血漿置換均為CIDP的一線治療用藥,約80%的患者對一線治療有效;但仍有少部份患者對治療反應差,或開始有效,而病程後期對治療反應變差,而導致嚴重殘疾。
公開資料顯示,BIVV020(SAR445088)是一款靶向補體C1s蛋白的單複制抗體。補體作為連線先天性和適應力免疫的橋梁,補體系統在啟用之後參與機體的防禦反應及免疫調節,包括增強抗體反應並具有免疫記憶,裂解外來細胞,清除免疫復合物和雕亡細胞等。補體C1s是補體系統中的一個重要成分,是補體系統經典途徑的發起因子。但是,補體若一旦失衡或過度啟用也會導致多種自身免疫性疾病。阻斷C1s蛋白的功能有望治療多種該類疾病。

BIVV020於2020年12月16日被CDE受理其IND申請,2021年3月已被臨床默示特許。CDE藥物臨床試驗登記與資訊公示平台顯示,BIVV020正在開展一項國際多中心的2期研究(NCT04658472、CTR20210677)。擬目標入組數為國際110例,其中國內11例。2021年5月,該試驗入組第一例患者。目前國際已入組80例,國內入組9例。
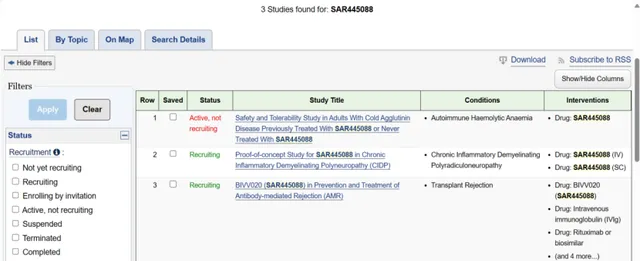
Clinical trials上顯示,與BIVV020相關有3項臨床研究。除針對CIDP的2期國際多中心研究外,1項1期研究(NCT04802057)已招募完成,用於治療冷凝集素病(CAD)患者。1項2期研究(NCT05156710)進行中,用於治療腎移植排斥反應(AMR)的預防和治療。
歷史文章:
禮來的Zepbound替爾泊肽——全球第二款減肥藥,最快2024年中在中國上市
國研肺癌新藥「伏美替尼」獲FDA突破療法
全球第二個FDA批準的核酸適配體Izervay的CMC解讀
降低感染風險!新型長效G-CSF藥物ROLVEDON的非臨床總結
END

掃碼關註
科誌康
關於科誌康
上海科誌康醫藥科技有限公司,成立於2016年,是一家以藥品監管科學為特色的研發咨詢公司,致力於為客戶客製法規解決方案,減少和避免在註冊申報時「少做、漏做、重做、多做」的風險。
在藥品註冊時,公司提供高品質的一站式註冊申報和模擬現場檢查服務,為客戶提高藥品註冊成功率。在研發過程中,公司提供第三方專案管理服務,法規前置,過程管理,協助制藥企業提升藥品研發效率。
目前,公司已與國內外79個知名制藥企業建立合作,取得了100多項IND/NDA/ANDA佳績。
公司使命: 為制藥企業提供專家解決方案,提升藥品全生命周期合規性
公司願景: 助力制藥企業研發和生產,讓老百姓吃上放心藥











