器官芯片是利用微芯片制造方法建立的微流控細胞培養裝置,該裝置包含持續灌流的腔室,腔室內有按組織和器官級別生理學排列的活細胞。透過再現體內的多細胞結構、組織-組織界面、物理化學微環境和血管灌流,這些裝置能夠實作傳統二維或三維培養系統無法達到的組織和器官功能水平。此外,它們還能實作對活細胞在功能性組織和器官環境中的生化、遺傳和代謝活動的高分辨率、即時成像和體外分析。這項技術在推動組織發育、器官生理學和疾病病因學研究方面具有巨大潛力。在藥物發現與開發的背景下,尤其在研究分子作用機制、優先選擇候選化合物、毒性測試和生物標誌物辨識方面,它將具有特別重要的價值。相關論文 「Microfluidic organs-on-chips」 由美國麻省劍橋市科赫研究所電氣工程與電腦科學系和麻省理工學院醫學工程與科學研究所和布羅德研究所的 Sangeeta N Bhatia 和美國麻省波士頓哈佛大學Wyss生物啟發工程研究所的 Donald E Ingber 於 2014年8月5日發表於【Nature Biotechnology】上。
器官芯片是什麽?
器官芯片是一種微流控裝置,其設計目的在於在微米級腔室中培養活細胞,模擬組織和器官的生理功能。它們旨在構建最小的功能單元,以再現特定組織或器官的功能,而非完整的活體器官。最簡單的器官芯片系統包含一個微流控腔室,用於培養特定類別的細胞並展示特定組織類別的功能。更復雜的設計則涉及多個微通道和多孔膜,用於模擬不同組織之間的界面,例如肺泡-毛細血管界面或血腦屏障。這些系統結合了物理力學,如流體剪下應力、迴圈應變和機械壓縮,並允許研究藥物、毒素或其他環境因素對細胞反應的影響。器官芯片可由不同器官細胞排列並透過流體連線的芯片或模擬不同器官之間生理相互作用的間質組織區域制成。 制造器官芯片通常采用軟光刻技術,該技術利用液態聚合物在矽基板上形成橡膠狀材料(圖1b),以建立微米級腔室或通道。 關鍵特征包括光學透明性,使得對細胞響應的即時高分辨率成像成為可能。透過微尺度制造方法,如微模塑、微蝕刻和激光蝕刻,使用各種材料制造了類似的裝置(圖1a)。用於培養細胞的微型灌註生物反應器是透過在中央通道表面塗覆 ECM 分子,讓細胞流入通道使其粘附在 ECM 基質上,然後用培養基持續灌註通道而制成的(圖 2a)。
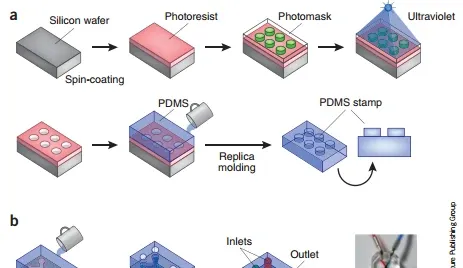
圖1 微流控芯片的制造方法。(a) 復制成型可制作形狀與光刻蝕刻在矽片上的圖案互補的印章。將一層均勻的感光材料 (光刻膠) 薄膜旋塗在矽片上,然後用光掩模 (例如,用不透明鉻層圖案化的透明玻璃板) 覆蓋矽片,光掩模上帶有用電腦輔助設計軟件生成的微尺度圖案。光掩模在高強度紫外線 (UV) 光照射期間保護光刻膠的某些區域並暴露其他區域。紫外線照射的材料會溶解在顯影劑溶液中,從而使微尺度圖案蝕刻在光刻膠中。表面形貌與蝕刻表面互補的彈性印章是透過復制成型技術建立的,其中 PDMS 的液態預聚物被澆鑄在蝕刻的光刻膠圖案之上,然後聚合並剝離。PDMS 印章可用於在任何基底上微接觸打印 ECM 分子,包括微流體裝置內的 ECM 分子(未顯示)。(b)單鍊結微流體裝置是透過制作具有兩個入口、一個主通道和一個出口的 PDMS 印章並將其保形密封到平板玻璃基底上來制造的。右側顯示了雙室微流體培養裝置的照片,其中紅色和藍色染料透過上下通道灌註。透明側通道用於施加周期性吸力,以有節奏地扭曲柔性中心膜和粘附細胞。
系統參數的控制
微流控芯片的套用可以控制在傳統的三維靜態培養或生物反應器中難以控制的系統參數,從而推動了對廣泛生理現象的研究。這些裝置完全微工程化,能與微傳感器整合,以監測培養的細胞或微環境條件,這在自組織的三維培養中通常不可行。微傳感器已整合到芯片上,用於分析組織屏障的完整性、細胞遷移和流體壓力,未來還可能檢測其他化學和培養條件。
流體流動控制在微流控芯片中被證明非常有用。微流控通道的層流流動使得生成物理和化學梯度成為可能,已被用於研究細胞遷移、心臟組織形成、神經軸突生長等,透過調整流速或通道尺寸,以及使用微工程支柱分離細胞與流動路徑,可以獨立控制流體剪下應力與物理和化學梯度。
細胞圖案化的控制是微流控芯片的另一個優勢。透過在微通道中以不同圖案接種不同類別的細胞,可以實作多樣化的細胞排列 (圖2b)。更新的芯片設計還允許在三維ECM凝膠中嵌入細胞(圖3),以及建立多細胞結構(圖2c和圖4a)。
將多孔基底整合以分隔微通道,使得分析組織屏障功能和跨細胞運輸成為可能。此外,芯片還可以模擬復雜的機械微環境,如迴圈機械應變和流體剪下應力(圖4b,c,d)。
盡管大多數研究是在已建立的細胞系或原代細胞上進行的,但微流控芯片的技術原則上適用於各種細胞類別,包括植物和昆蟲細胞。使用幹細胞,特別是iPS細胞,有望實作個人化的「芯片上的人」,其中所有的器官芯片都源自單個患者。
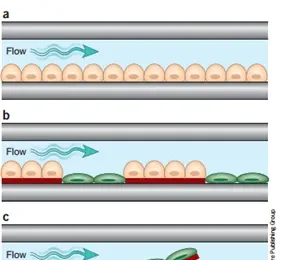
圖 2 日益復雜的單鍊結器官芯片設計範例。(a) 單一類別的細胞以單層形式培養在微流體通道一側的平面剛性(例如玻璃)或柔性(例如 PDMS)基底上,培養基透過微流體通道灌註。(b) 兩種類別的細胞透過在微流體室內微圖案化 ECM 粘合島直接並列培養,這些粘合島優先支持一種細胞群(例如肝細胞)。首先輸送這些細胞,然後用第二種細胞群(例如成纖維細胞)填充空白處。(c) 在微流體通道中培養用 ECM 設計的組織構造中的細胞。在此範例中,在塗在基底上的薄 PDMS 層上以線性圖案微接觸打印 ECM 用於定向肌肉細胞以建立各向異性的肌肉組織層。當 PDMS 薄膜的部份從基底上釋放出來時,細胞收縮時它們會彎曲起來,從而可以測量流動狀態下的細胞收縮力。
器官芯片能否模擬器官級功能和疾病?
器官芯片在研究器官生理和疾病的基本機制方面具有巨大潛力。 它們特別適合研究依賴於組織微觀結構和灌流的生物現象,以及涉及相對急性(持續時間小於1個月)的病理生理過程。 過去十年中,研究人員已經制造了用於研究肝臟、腎臟、腸道、肺、心臟、平滑和橫紋肌、脂肪、骨骼、骨髓、角膜、皮膚、血管、神經和血腦屏障等的芯片。這些裝置中,許多不能被視為完整的器官模型,因為只在一個微通道中培養了一種細胞類別。然而,它們揭示了流體流動和剪下應力對細胞形態和功能的強大影響。例如,在動態流動下的24小時內,微流控腔室中的混合初級肝細胞群形成了兩個門戶區樣和靜脈樣細胞區。流動造成的可溶性物質的消耗產生了溶解氧和可溶性生長因子的梯度,氧張力被證明是「分區」反應的主要決定因素。
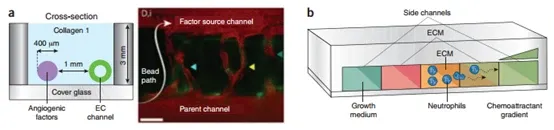
圖 3 結合 ECM 凝膠的血管生成和免疫細胞侵襲的微流控芯片模型。(a) 犧牲材料以線性模式沈積在 ECM 凝膠中,然後被移除以建立兩個通道(左)。一個通道中充滿血管內皮 (EC) 細胞,另一個通道用於遞送血管生成因子。血管生成刺激誘導內皮細胞進行發芽血管生成,然後功能性地連線到源通道,形成支持液體流動的新微血管(右)。紅色表示在培養基中流動的微粒。(b) 一種梯度產生微流控培養裝置,用於分析免疫細胞在受到趨化梯度刺激時透過 ECM 凝膠的遷移
透過微結構提高芯片功能
細胞間的相互作用對於維持組織結構和功能至關重要。 在肝臟芯片中,透過將高密度同質細胞環境中的初級人肝細胞與活性流通道分離,可以模擬異質相互作用。這種設計使得維持肝細胞的代謝活性超過7天成為可能,並且允許對依賴於功能性肝細胞的藥物雙氯芬酸(伏特加)的肝毒性進行分析。盡管在沒有流動的情況下,異質細胞間相互作用可以穩定人肝細胞的功能,並改善藥物代謝和毒性測試的預測性,但基於流動的芯片能夠動態監測代謝產物的生成。
在器官芯片中,氧張力的動態變化被用於引發疾病狀態,如心臟缺血或鐮狀細胞病中由去氧化的血紅蛋白S聚合引起的血管阻塞。 這種模型提供了觀察發生在活體器官深處的病理生理學的視窗,使得可以評估治療這些危及生命的疾病的藥物候選物。
另一方面,低水平的流體剪下應力在與活體腎臟的集合管和近端小管中觀察到的剪下應力類似,增強了分化並增加了分子和藥物的運輸功能。最近的研究表明,透過使用腎臟芯片,可以重建在蛋白尿性腎病發展過程中導致腎間質纖維化的上皮-間質轉化。
微通道的形狀也可以被改變以模擬紊流, 例如,在內皮細胞襯裏的微通道中的一個狹窄或狹窄區域可提供對異常血流動力學如何促進動脈粥樣硬化斑塊周圍的血栓形成的見解。
結合與體內類似的流體流動和機械強制方案可以改善組織和器官的特異性功能。 比如,對人骨髓和脂肪細胞芯片施加動態液壓壓縮能增加骨分化,這透過成骨基因表現和骨誘導ECM成分的產生來衡量。此外,將Caco-2細胞在柔性、多孔的ECM塗層膜上培養,並暴露於類似於腸腔中的滴流和模仿活腸蠕動運動的周期性機械變形時,它們可以重新組織成為類似於小腸絨毛結構的三維起伏組織結構。
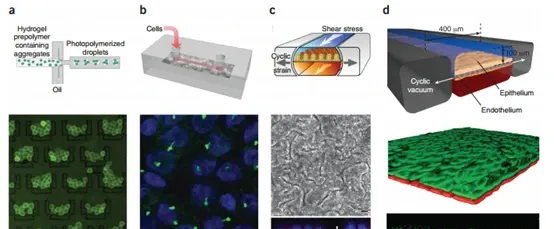
圖 4 日益復雜的器官芯片設計範例。(a) 肝臟芯片,其中由含有肝細胞和成纖維細胞的微尺度水凝膠組成的肝臟微組織在一個微流體系統中進行微工程設計(頂部),然後用於填充另一個芯片進行培養和即時多路復用分析(底部)(b) 腎臟芯片,其中人類腎臟近端小管上皮細胞在分隔兩個通道的多孔膜頂部培養,從而能夠分析跨細胞運輸、攝取和分泌 (c) 腸道芯片,其中人類 Caco-2 腸上皮細胞培養在 ECM 塗層的多孔 PDMS 膜上,該膜將兩個通道隔開。(d) 一個「呼吸」肺芯片,重現了肺泡-毛細血管界面。人類肺泡上皮細胞培養在柔性多孔 ECM 塗層膜上,人類毛細血管內皮細胞培養在底部。
建模器官水平的生理學和疾病模型
細胞培養在模擬芯片上組織微環境方面已取得一定進展,但單一細胞類別的套用通常無法完全復制器官的功能。關鍵在於結合多種不同類別的組織。最近的研究顯示,已經在這個領域取得了顯著進展。
舉例來說,人類血腦屏障芯片透過在多孔的聚碳酸酯膜上培養人類腦微血管內皮細胞和星形膠質細胞,成功地模擬了部份血腦屏障的功能。這種芯片具有更高的跨上皮電阻(TEER)和更強的大分子滲透性,相比傳統的培養系統有顯著的優勢,可用於研究中樞神經系統滲透屏障和藥物透過血腦屏障的效果。類似地,建立了包含多種不同類別腦細胞的神經血管單元微流體模型,使得在芯片上模擬神經系統的復雜反應成為可能。這種模型不僅保持了內皮細胞的屏障功能,還模擬了神經炎癥和神經元突觸形成等生理過程。
另一方面,研究還利用芯片模型來探索神經系統疾病的機制。例如,透過在芯片上共培養遺傳改造的神經元和星形膠質細胞,成功模擬了肌萎縮側索硬化癥的氧化應激損傷。而人類「呼吸」肺芯片則透過模擬肺泡毛細血管界面的周期性機械應變,提供了研究肺部疾病發病機制的重要工具。這些研究表明,在芯片上結合不同類別的細胞和組織,可以更好地模擬器官級別的功能,為疾病建模、藥物篩選和基礎生物學研究提供了重要的平台。
器官芯片在藥物開發中展現出巨大前景,特別是在ADMET測試和PK/PD建模領域。這些微工程化器材能夠復制人體器官的復雜互動和功能,提供比傳統體外或動物模型更準確、更符合人類的數據。
ADMET測試
ADMET(吸收、分布、代謝、排泄和毒性)測試對於評估新藥的安全性和有效性至關重要。器官芯片可以顯著改善這一過程:
吸收和分布: 透過模擬人體組織的生理屏障和流體動力學,器官芯片能夠更準確地預測藥物的吸收和分布。例如,血腦屏障(BBB)芯片可以評估藥物的通透性,提供藥物是否能夠穿過這一關鍵屏障的寶貴數據。
代謝: 肝臟芯片模型對於研究藥物代謝特別有用。這些器材可以模擬藥物的肝臟代謝,包括活性或毒性代謝產物的形成。例如,在芯片上使用HepG2/C3A細胞研究抗癌前藥氟他胺及其活性代謝物羥基氟他胺的代謝,揭示了不同的代謝標誌物和肝毒性。
排泄: 器官芯片還可以模擬腎功能以研究藥物代謝產物的排泄。腎臟芯片可以評估藥物及其代謝產物的過濾和排泄,提供關於腎臟清除率和潛在腎毒性的見解。
毒性: 多器官芯片可以用來研究藥物在各種組織中的毒性。例如,肝腎芯片展示了對乙酰胺基酚引起的劑量依賴性肝毒性和谷胱甘肽耗竭,精確模仿了體內反應。
PK/PD建模
藥代動力學(PK)和藥效動力學(PD)建模涉及理解藥物在體內的處理方式及其生物效應(圖5)。器官芯片為PK/PD研究提供了多種優勢:
即時監測: 這些器材允許即時監測藥物對不同組織的影響,提供關於藥物吸收、分布、代謝和排泄的動態數據。
機制性見解: 器官芯片可以幫助闡明藥物作用和毒性的機制。例如,肺芯片被用來研究二氧化矽納米顆粒的運輸以及呼吸運動在增強納米顆粒攝取和誘導血管通透性方面的關鍵作用。
物種特異性差異: 透過使用人類細胞,器官芯片可以克服動物模型中常見的物種特異性差異。例如,腎臟芯片能夠測量靜態培養或動物模型中無法檢測到的OCT2特異性順鉑毒性。
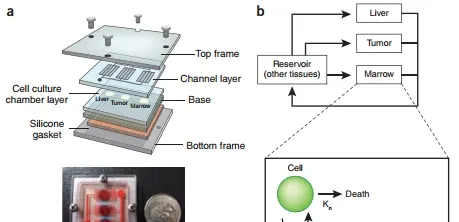
圖 5 用於 PK/PD 建模的多器官微流體框架。(a)三腔芯片的示意圖(頂部)和照片(底部),用於 PK 建模,透過流動培養基流過肝臟、腫瘤和骨髓細胞,這些細胞在單獨的腔中以單層形式培養並透過流體連線。(b)a 中顯示的芯片中肝臟、腫瘤和骨髓區室之間的連線流程圖(頂部),以及每個區室中細胞死亡的藥效學模型(底部)
藥物開發套用
藥物篩選: 器官芯片可用於高通量藥物候選篩選。它們提供了更準確的人體生理模擬,允許更好地預測藥物的有效性和毒性。
個人化醫學: 這些器材可以用患者衍生的細胞客製,建立疾病的個人化模型,從而開發針對性的治療方案和更有效的治療策略。
監管測試: 器官芯片有潛力改進監管測試,提供更可靠的藥物安全性和有效性數據,可能減少動物測試需求並加速藥物審批過程。
案例研究
癌癥藥物測試: 一個涉及肝臟、骨髓和癌細胞的連線腔室的研究表明,聯合使用阿黴素和MDR調節劑對MDR癌細胞變體的抗增殖作用比單獨使用這些化合物更強,而這一結果在傳統靜態培養中無法實作。
BBB芯片: 該模型準確預測了各種藥物的通透性,與體內數據高度相關,提供了藥物穿越血腦屏障的見解。
肝腎芯片: 該模型展示了對乙酰胺基酚對肝臟和腎細胞的影響,顯示了器官系統的相互聯系以及在藥物測試中考慮多器官相互作用的重要性。
總之,器官芯片為藥物開發提供了一個強大的平台,提供了更符合人類生理和動態模型的ADMET測試和PK/PD研究。它們能夠復制復雜的器官功能和互動,可以更好地預測藥物的安全性和有效性,最終改進藥物開發過程並推動個人化醫學的發展。
器官芯片的優點與局限性
細胞定位精準: 器官芯片可以精準地定位不同類別的細胞,使其相對於彼此的位置得以控制,從而能夠在受控環境中研究組織間的相互作用。
高分辨率成像: 由於其小尺寸和受控環境,器官芯片有助於即時高分辨率成像細胞和分子事件。
流體流動控制: 這些系統能夠控制流體流動,增強細胞分化、功能和長期存活。這一特點對模擬生理條件和研究慢性病理生理反應特別有用。
可重復性和可延伸性: 器官芯片提供可重復的實驗條件和可延伸性,使得能夠更容易地進行大樣本量的研究,並增加結果的統計顯著性。
與分析檢測方法的整合: 這些系統可以與各種分析檢測方法(如熒光共聚焦顯微鏡、微流熒光法和TEER測量)整合,實作對細胞反應的全面分析。
模擬器官級功能:雖然不能完全復制整個器官的復雜性,但器官芯片可以模擬某些器官級功能和對化學或電訊號的反應,為理解器官生理和疾病機制提供寶貴的見解。
然而,器官芯片也存在一些局限性:
技術挑戰: 器官芯片的制造需要專業的微工程能力,並且需要解決微流體通道中氣泡形成和矩陣隨時間的降解等技術挑戰。
宏觀結構的有限復制:在微觀尺度上復制較大的3D器官或組織截面的宏觀結構和空間異質性是具有挑戰性的。
模擬復雜器官功能: 由於其宏觀尺度結構,某些器官功能(如大腦的認知功能和骨骼、韌帶和肌腱的機械功能)在芯片上的模擬具有挑戰性。
與迴圈細胞的相互作用: 雖然器官芯片可以模擬與血液、免疫或腫瘤細胞等迴圈細胞的相互作用,但在完全復制這些相互作用的復雜性方面仍然存在挑戰。
總之,器官芯片為研究器官生理、疾病機制和藥物反應提供了一個強大的平台,但需要解決技術挑戰,並提高這些系統的復雜性,以充分發揮其在生物醫學研究和藥物開發中的潛力。
前景
人類器官芯片代表了生物醫學研究的潛在變革。作為傳統細胞培養和動物模型的替代方案,它們有望在多個領域帶來重大影響。這些芯片可用於研究器官發育和疾病的分子機制、器官間的相互作用,以及身體與藥物、環境因素、消費品和醫療器械等刺激物的相互作用。透過結合特定患者的原代或誘導多能幹細胞,甚至基因編輯技術,器官芯片可以用於開發個人化的健康與疾病模型。
然而,目前器官芯片在某些生物醫學研究領域仍存在局限性,如慢性疾病、適應力免疫反應,以及內分泌、骨骼或神經系統的復雜系統級行為。它們主要適用於研究相對短時間內發生的生理和疾病過程(不到1個月),並且依賴於組織或器官特異性的微觀結構。例如,肝臟芯片可用於研究肝臟生理的多個方面,如特異性蛋白的產生、細胞運輸以及應對壓力反應的機制。盡管肝臟芯片展現了在藥物相互作用方面的潛力,但它們仍面臨一些挑戰,如劑量依賴性、種屬特異性和相對急性的藥物相互作用等問題。
除此之外,長期過程和慢性疾病的研究在任何體外模型中都具有挑戰性。盡管一些長期過程的特征可能在芯片上得以復制,但對於一些慢性疾病的研究,如纖維化,肝臟芯片等技術仍然面臨挑戰。然而,即使在面對這些挑戰時,器官芯片也提供了獨特的研究機會,例如模擬特定患者的特異性藥物毒性反應。因此,盡管還有一些問題需要解決,但器官芯片代表了生物醫學研究的一個激動人心的發展方向,為未來的研究和藥物開發提供了新的可能性。











