原創 可頌 米內網
精彩內容
今年以來石藥集團創新研發進展不斷:1類新藥納魯索拜單抗獲批上市、9個品種批產並視同過評(4個首仿)、2款1類新藥申報NDA、9款1類新藥獲批臨床……2023年前三季度公司研發費用36.78億元,大幅增長25.9%。目前石藥集團已有8款1類新藥處於NDA/Ⅲ期臨床階段,上市可期;104個品種過評(28個首家),33個品種國采中選。
研發費用大增25.9%!創新研發進展不斷
11月30日,石藥集團釋出2023年前三季度業績,公司實作收入238.65億元,同比增長1.6%;實作股東應占溢利44.95億元,同比增加0.6%。集團成藥業務實作收入193.38億元,占總收入的81.03%,其中收入最高的三個治療領域分別為神經系統、抗腫瘤和抗感染,銷售收入分別為69.26億元、31.43億元和46.24億元。
作為國內成功完成創新轉型的傳統藥企,石藥集團堅守創新和國際化本心,近年來持續加大研發投入,2022年投入研發費用約40億元;2023年前三季度投入研發費用36.78億元,增長速度高達25.9%,約占成藥業務收入的19%。
石藥集團研發費用情況(單位:億元)

大手筆的研發投入下,石藥集團創新研發穩步推進,不斷迎來重大進展。今年3月,公司合作開發的1類新藥谷美替尼片(c-Met抑制劑)獲批上市;4月,1類新藥普盧格列汀片(DPP-4抑制劑)申報NDA並獲受理,用於治療2型糖尿病;6月,3.3類生物類似藥奧馬珠單抗註射液、1類新藥巴托利單抗註射液送出上市申請並獲受理;9月,1類新藥納魯索拜單抗註射液獲批上市,用於治療不可手術切除或手術切除可能導致嚴重功能障礙的骨巨細胞瘤。
2023年至今石藥集團釋出的新藥研發公告
臨床試驗批準方面,今年以來石藥集團有多款1類創新藥、生物類似藥以及高端制劑相繼獲批臨床。其中,1類新藥有9款,包括SYp053註射液、SYp038片、ALMB-0166註射液、SYS6011、註射用NBL-028、JMT203註射液、SYp051片、SYS6010、NBL-020註射液。值得一提的是,SYp053註射液是一種雙鏈小幹擾RNA(siRNA)藥物,是公司首款獲批臨床的siRNA產品。
拿下10個重磅品種!104個過評品種亮眼
今年以來,石藥集團已有10個品種獲批上市,進一步豐富了公司的產品線。其中,1類新藥納魯索拜單抗註射液是全球首個IgG4亞型全人源抗RANKL單抗;鹽酸伊立替康脂質體註射液、沙庫巴曲纈沙坦鈉片、琥珀酸地文拉法辛緩釋片、阿普米司特片均為國內首仿+首家過評;帕利哌酮緩釋片為國產第2家,米拉貝隆緩釋片為國產第4家。
2023年至今石藥集團獲批產品(不含疫苗)
12月1日,國家藥監局官網顯示,石藥集團的註射用青黴素鈉透過仿制藥一致性評價,為國內第3家家過評。米內網數據顯示,2022年中國城市公立醫院、縣級公立醫院、城市社區中心以及鄉鎮衛生院(簡稱中國公立醫療機構)終端註射用青黴素鈉銷售額突破6億元,同比增長超過50%。
截至目前,石藥集團已有104個品種透過/視同透過一致性評價。其中,28個品種為國內首家過評,瑪巴洛沙韋片、註射用兩性黴素B膽固醇硫酸酯復合物、馬來酸左氨氯地平片、琥珀酸地文拉法辛緩釋片、鹽酸伊立替康脂質體註射液、鹽酸雷尼替丁膠囊、格列美脲分散片、鹽酸決奈達隆片等10個品種為獨家過評。
石藥集團透過/視同透過一致性評價品種
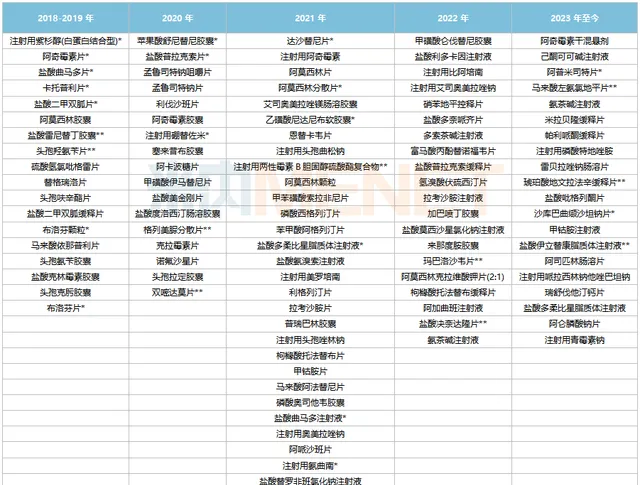
從治療領域上看,104個品種主要集中在全身用抗感染藥物(31個)、抗腫瘤和免疫調節劑(15個)、神經系統藥物(15個)、消化系統及代謝藥(13個)。米內網數據顯示,2022年中國公立醫療機構終端抗腫瘤和免疫調節劑、消化系統及代謝藥、全身用抗感染藥物銷售額均超過1500億元,神經系統藥物銷售額接近1000億元。
11月16日,第九批集采41個品種中選結果正式公布,將於2024年3月實施。此次石藥集團有一個品種註射用磷酸特地唑胺中選,價格為138元(0.2g*1瓶/盒),供應省份為黑龍江、福建、山東、甘肅。公司該品種於6月21日獲批上市,市場尚屬空白,為「光腳」品種。
在已開展的八批化藥集采中,石藥集團分別有1個、3個、8個、6個、3個、9個、2個、1個品種中標,合計33個品種。多個「光腳」品種國采中選後快速放量,為公司業績帶來新的銷售收入貢獻。
8款1類新藥上市可期!3大爆品進攻$178億市場
石藥集團已打造了豐富的產品管線,目前在研創新藥專案110余個,其中大分子約40個、小分子約40個、新型制劑約30個。透過「研發一代、規劃一代」的合理布局,石藥集團創新藥管線已基本形成「上市一批、臨床一批、開發一批」的良性迴圈,構築起強大的研發能力。
4款1類創新藥上市申請在審中,具體為甲磺酸瑞澤替尼膠囊(三代EGFR抑制劑)、普盧格列汀片(DPP-4抑制劑)、恩朗蘇拜單抗註射液(PD-1單抗)、巴托利單抗註射液(FcRn單抗),有望於2024年內陸續獲批上市。
石藥集團處於NDA/Ⅲ期臨床階段1類新藥

SKLB1028膠囊(多靶點蛋白激酶抑制劑)、CM310(IL-4Rα單抗)、KN026(HER2雙抗)、DP303c(HER2 ADC)等1類創新藥已處於Ⅲ期臨床階段,上市可期。此外,公司還有10余款1類創新藥處於Ⅱ期臨床階段。
3款生物類似藥處於NDA/Ⅲ期臨床階段,其中奧馬珠單抗已送出上市申請,原研藥2022年全球銷售額超過35億美元;帕妥珠單抗、烏司奴單抗均處於Ⅲ期臨床階段,原研藥2022年全球銷售額分別超過46億美元、97億美元。
資料來源:米內網數據庫、公司公告
註:米內網【中國公立醫療機構藥品終端競爭格局】,統計範圍是:中國城市公立醫院、縣級公立醫院、城市社區中心以及鄉鎮衛生院,不含民營醫院、私人診所、村衛生室;上述銷售額以產品在終端的平均零售價計算。











